100℃时,把0.5molN2O4通入容积为5L的真空密闭容器中,发生N2O4(g)⇌2NO2(g),立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol·L−1,60s时,体系已达到平衡状态,此时容器内的压强为开始时的1.6倍。下列说法正确的是
| A.0~2s内用N2O4的浓度变化表示的反应速率为0.01mol·L−1·s−1 |
| B.在2s时容器内的压强为开始时的1.1倍 |
| C.平衡时,c(NO2)=0.6mol·L−1 |
| D.若压缩容器体积减小,达新平衡时的红棕色比原平衡时的浅 |
更新时间:2021-11-06 10:17:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下,将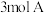 和
和 投入容积为
投入容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: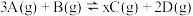 。
。 末测得此时容器中C和D的浓度为
末测得此时容器中C和D的浓度为 和
和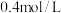 。下列叙述正确的是
。下列叙述正确的是
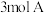 和
和 投入容积为
投入容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: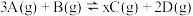 。
。 末测得此时容器中C和D的浓度为
末测得此时容器中C和D的浓度为 和
和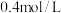 。下列叙述正确的是
。下列叙述正确的是A. |
B. 时,B的浓度为 时,B的浓度为 |
C. 内B的反应速率为 内B的反应速率为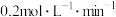 |
D.此时A的转化率为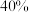 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 的速率方程为
的速率方程为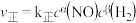 ,在
,在 下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是
下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是
 的速率方程为
的速率方程为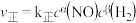 ,在
,在 下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是
下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是
| 实验 | 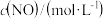 |  |  |
 |  |  |  |
 |  |  | 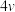 |
 |  |  |  |
 |  |  |  |
A.降低温度, 可能增大 可能增大 |
B.表中的 为8 为8 |
C. 、 、 的值分别为2、1 的值分别为2、1 |
D.若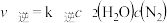 ,则 ,则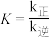 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】温度分别为 T1 和 T2时, 将气体 X 和气体 Y 各 0.16mol 充入 l0L 恒容密闭容器中, 发生反应 X(g)+Y(g) 2Z(g), 一段时间后达到平衡, 反应过程中测定的数据如下表
2Z(g), 一段时间后达到平衡, 反应过程中测定的数据如下表
下列说法正确的是
 2Z(g), 一段时间后达到平衡, 反应过程中测定的数据如下表
2Z(g), 一段时间后达到平衡, 反应过程中测定的数据如下表| 温度/K | t/min n/mol | t1 | t2 | t3 | t4 |
| T1 | n(Y) | 0.14 | 0.12 | 0.10 | 0.10 |
| T2 | n(Y) | 0.13 | 0.09 | 0.08 |
| A.该反应的正反应为放热反应 |
B.温度为T1时,0~ t1时间段用 Z 表示的平均反应速率为 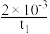 mol•L-1.min-1 mol•L-1.min-1 |
| C.温度为T2时,t3时刻刚好达到平衡状态 |
| D.在 T1下平衡后 , 保持其他条件不变, 再充入 0.2molZ, 平衡时 X 的体积分数不变 |
您最近一年使用:0次
【推荐2】将2 mol N2O5置于2 L密闭容器中,在一定温度下发生反应:①2N2O5(g) 2N2O4(g)+O2(g);②N2O4(g)
2N2O4(g)+O2(g);②N2O4(g) 2NO2(g)。达到平衡时,c(O2)=0.4 mol·L-1,c(NO2)=0.4 mol·L-1,下列说法正确的是
2NO2(g)。达到平衡时,c(O2)=0.4 mol·L-1,c(NO2)=0.4 mol·L-1,下列说法正确的是
 2N2O4(g)+O2(g);②N2O4(g)
2N2O4(g)+O2(g);②N2O4(g) 2NO2(g)。达到平衡时,c(O2)=0.4 mol·L-1,c(NO2)=0.4 mol·L-1,下列说法正确的是
2NO2(g)。达到平衡时,c(O2)=0.4 mol·L-1,c(NO2)=0.4 mol·L-1,下列说法正确的是| A.平衡时,c(N2O5)=0.4 mol·L-1 |
| B.此温度下反应①的平衡常数的数值为3.6 |
| C.平衡时N2O5的分解率为70% |
| D.平衡后混合气体的平均摩尔质量为80 g·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应 aA(g ) +bB ( g ) cC( g ) ∆H 受温度、压强影响如图所示,则下列说法正确的是
cC( g ) ∆H 受温度、压强影响如图所示,则下列说法正确的是

 cC( g ) ∆H 受温度、压强影响如图所示,则下列说法正确的是
cC( g ) ∆H 受温度、压强影响如图所示,则下列说法正确的是 
| A.T1<T2 | B.P1>P2 | C.∆H<0 | D.a+b<c |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容中发生下列反应aA(g)+bB(g)⇌cC(g)+dD(s),反应达到平衡后,将气体体积压缩到原来的一半,达到平衡时,C的浓度为原平衡的1.7倍,下列叙述正确的是
| A.A的转化率变大 | B.a+b<c |
| C.化学平衡常数K减小 | D.平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】法国化学家PaulSabatier较早提出可以利用工业废弃物CO2转化为CH4,其反应原理为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) △H=-165kJ・mol-1。若在密闭容器中充入1molCO2、1mol H2引发该反应进行,下列说法正确的是
| A | B | C | D |
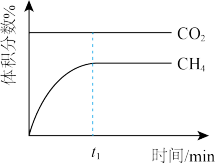 | 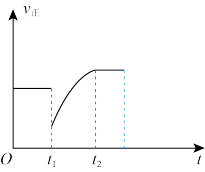 |  | 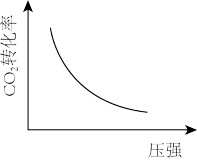 |
| 恒温恒容下,混合气体中CH4与CO2的体积分数变化 | 恒温恒压条件平衡后,t1时改变条件可能是充入少量N2 | 升高温度,平衡常数Kc的变化趋势 | CO2平衡转化率随压强的变化趋势 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是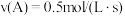
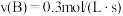
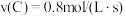

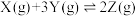 ,若X、Y、Z的起始浓度分别为c1、c2、c3均不为零),达到平衡状态时,X、Y、Z浓度分别为0.1mol·L-1、0.3mol·L-1和0.08mol·L-1,则下列判断合理的是
,若X、Y、Z的起始浓度分别为c1、c2、c3均不为零),达到平衡状态时,X、Y、Z浓度分别为0.1mol·L-1、0.3mol·L-1和0.08mol·L-1,则下列判断合理的是

