某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有_______________________________ ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是__________________________ ;
(3)要加快上述实验中气体产生的速率,还可采取的措施有______________ (答两种);
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=_______ ,V6=________ ,V7=________ ,V9=________ ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:___________________________________________ 。
(1)上述实验中发生反应的离子方程式有
(2)硫酸铜溶液可以加快氢气生成速率的原因是
(3)要加快上述实验中气体产生的速率,还可采取的措施有
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol·L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
更新时间:2020-09-21 19:08:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】铜是与人类关系非常密切的有色金属,人类使用铜及其合金已有数千年历史。某实验小组以铜为原料进行如下实验,回答下列问题:
Ⅰ.制备 并探究其性质
并探究其性质

(1)仪器a的名称为_______ 。若用 和浓硫酸反应制备
和浓硫酸反应制备 ,应选用装置
,应选用装置_______ (填“A”或“B”)。
(2)通入 后,装置C中的现象为
后,装置C中的现象为_______ 。装置D中出现淡黄色浑浊,发生反应的化学方程式为_______ 。
Ⅱ.探究温度对 催化
催化 分解速率的影响
分解速率的影响
实验事实将光洁无锈的铜丝插入装有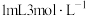 硫酸的试管中,一段时间后铜丝表面未发生变化。再向该试管中加入
硫酸的试管中,一段时间后铜丝表面未发生变化。再向该试管中加入 的
的 溶液,铜丝表面产生气泡并逐渐变多,溶液变成蓝色。经检验产生的气体为
溶液,铜丝表面产生气泡并逐渐变多,溶液变成蓝色。经检验产生的气体为 ,查阅资料发现是
,查阅资料发现是 催化
催化 分解的结果。
分解的结果。
(3)写出该过程中生成 的离子方程式
的离子方程式_______ 。
提出问题 加入 溶液后,铜丝表面产生气泡逐渐变多,即
溶液后,铜丝表面产生气泡逐渐变多,即 分解速率逐渐增大,是什么原因导致的?
分解速率逐渐增大,是什么原因导致的?
提出猜想 实验小组同学提出了一种猜想:反应过程中溶液温度升高, 催化
催化 分解的速率增大。
分解的速率增大。
实验验证 小组同学通过测量相同时间内生成 的体积,来比较不同温度下
的体积,来比较不同温度下 催化
催化 分解速率的大小,实验设计如下。所用试剂为
分解速率的大小,实验设计如下。所用试剂为 溶液、
溶液、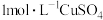 溶液、蒸馏水。
溶液、蒸馏水。
说明:各实验采用排水法,在相同温度和压强下测量 体积。
体积。
实验分析及结论
(4)通过实验测得 。小组同学认为实验
。小组同学认为实验 的结果不能证明猜想成立,理由是
的结果不能证明猜想成立,理由是_______ 。
(5)为进一步验证猜想,小组同学又进行了实验 。
。
①表中
_______ ,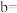
_______ ,
_______ 。
②小组同学结合实验 ,依据
,依据_______ (用含 和
和 的不等式表示)判断猜想成立。
的不等式表示)判断猜想成立。
Ⅰ.制备
 并探究其性质
并探究其性质
(1)仪器a的名称为
 和浓硫酸反应制备
和浓硫酸反应制备 ,应选用装置
,应选用装置(2)通入
 后,装置C中的现象为
后,装置C中的现象为Ⅱ.探究温度对
 催化
催化 分解速率的影响
分解速率的影响实验事实将光洁无锈的铜丝插入装有
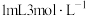 硫酸的试管中,一段时间后铜丝表面未发生变化。再向该试管中加入
硫酸的试管中,一段时间后铜丝表面未发生变化。再向该试管中加入 的
的 溶液,铜丝表面产生气泡并逐渐变多,溶液变成蓝色。经检验产生的气体为
溶液,铜丝表面产生气泡并逐渐变多,溶液变成蓝色。经检验产生的气体为 ,查阅资料发现是
,查阅资料发现是 催化
催化 分解的结果。
分解的结果。(3)写出该过程中生成
 的离子方程式
的离子方程式提出问题 加入
 溶液后,铜丝表面产生气泡逐渐变多,即
溶液后,铜丝表面产生气泡逐渐变多,即 分解速率逐渐增大,是什么原因导致的?
分解速率逐渐增大,是什么原因导致的?提出猜想 实验小组同学提出了一种猜想:反应过程中溶液温度升高,
 催化
催化 分解的速率增大。
分解的速率增大。实验验证 小组同学通过测量相同时间内生成
 的体积,来比较不同温度下
的体积,来比较不同温度下 催化
催化 分解速率的大小,实验设计如下。所用试剂为
分解速率的大小,实验设计如下。所用试剂为 溶液、
溶液、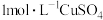 溶液、蒸馏水。
溶液、蒸馏水。| 实验序号 |  溶液体积/ 溶液体积/ | 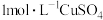 溶液体积/ 溶液体积/ | 蒸馏水体积/ | 水浴温度/℃ |  时生成 时生成 的体积/ 的体积/ |
| 1 | 10 | 1 | 1 | 20 |  |
| 2 | 10 | 1 | 1 | 30 |  |
| 3 | 10 | 1 | 1 | 40 |  |
| 4 | 10 | a | b | 20 | 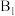 |
| 5 | 10 | c |  | ||
| 6 | 10 | 40 | 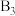 |
 体积。
体积。实验分析及结论
(4)通过实验测得
 。小组同学认为实验
。小组同学认为实验 的结果不能证明猜想成立,理由是
的结果不能证明猜想成立,理由是(5)为进一步验证猜想,小组同学又进行了实验
 。
。①表中

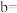

②小组同学结合实验
 ,依据
,依据 和
和 的不等式表示)判断猜想成立。
的不等式表示)判断猜想成立。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】草酸钴用途广泛,可用于指示剂和催化剂的制备。用含钴废料(主要成分为Co,含有一定量的NiO、 、Fe、
、Fe、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的流程如下:
)的流程如下:

已知:①RH难电离; 代表金属离子,
代表金属离子, 。
。
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)酸浸过程中为提高浸出速率,除粉碎外,还可采取的措施有___________ (写出一条即可)。
(2)滤渣Ⅰ的主要成分是___________ (填化学式)。
(3)“除杂Ⅰ”中加入 后发生反应的离子方程式为
后发生反应的离子方程式为___________ 。
(4)“除杂Ⅰ”中加入CoO的目的是___________ 。
(5)操作①在实验室所用的主要玻璃仪器有烧杯、___________ 。
(6)“除杂Ⅱ”中加入有机溶剂的目的是___________ ;可向溶有 的有机层中加入
的有机层中加入___________ 使 从有机相返回水相,实现金属的回收利用。
从有机相返回水相,实现金属的回收利用。
(7)能否先将 转化为
转化为 ,再利用反应
,再利用反应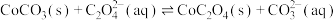 ,将
,将 转化为
转化为 ?
?___________ (填“能”或“不能”),说明理由:___________ 。[已知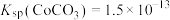 ,
, ]
]
 、Fe、
、Fe、 等)制备草酸钴晶体(
等)制备草酸钴晶体( )的流程如下:
)的流程如下:
已知:①RH难电离;
 代表金属离子,
代表金属离子, 。
。②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 金属离子 |  |  |  |  |  |
| 开始沉淀 | 1.5 | 6.3 | 7.2 | 3.4 | 6.9 |
| 完全沉淀 | 2.8 | 8.3 | 9.1 | 4.7 | 8.9 |
(1)酸浸过程中为提高浸出速率,除粉碎外,还可采取的措施有
(2)滤渣Ⅰ的主要成分是
(3)“除杂Ⅰ”中加入
 后发生反应的离子方程式为
后发生反应的离子方程式为(4)“除杂Ⅰ”中加入CoO的目的是
(5)操作①在实验室所用的主要玻璃仪器有烧杯、
(6)“除杂Ⅱ”中加入有机溶剂的目的是
 的有机层中加入
的有机层中加入 从有机相返回水相,实现金属的回收利用。
从有机相返回水相,实现金属的回收利用。(7)能否先将
 转化为
转化为 ,再利用反应
,再利用反应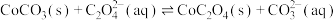 ,将
,将 转化为
转化为 ?
?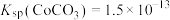 ,
, ]
]
您最近一年使用:0次
【推荐3】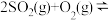
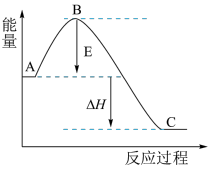
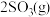 ,反应过程的能量变化如图所示。
,反应过程的能量变化如图所示。
已知1mol 氧化为1mol
氧化为1mol 的ΔH= -99
的ΔH= -99 。请回答下列问题:
。请回答下列问题:
(1)图中E的大小对该反应的反应热________ (填“有”或“无”)影响。该反应通常用 作催化剂,加
作催化剂,加 会使图中B点
会使图中B点___________ (填“升高”还是“降低”)。
(2) 氧化为
氧化为 的热化学方程式
的热化学方程式______________________________________ 。
(3)该反应的平衡常数表达式为______________________________ 。
(4)以下说法能证明恒温恒容条件下该反应已经达到平衡状态的是_________ 。
A.容器内压强保持不变 B.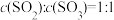
C.各气体百分含量保持不变 D.生成1mol 的同时消耗0.5mol
的同时消耗0.5mol
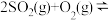
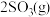 ,反应过程的能量变化如图所示。
,反应过程的能量变化如图所示。
已知1mol
 氧化为1mol
氧化为1mol 的ΔH= -99
的ΔH= -99 。请回答下列问题:
。请回答下列问题:(1)图中E的大小对该反应的反应热
 作催化剂,加
作催化剂,加 会使图中B点
会使图中B点(2)
 氧化为
氧化为 的热化学方程式
的热化学方程式(3)该反应的平衡常数表达式为
(4)以下说法能证明恒温恒容条件下该反应已经达到平衡状态的是
A.容器内压强保持不变 B.
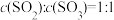
C.各气体百分含量保持不变 D.生成1mol
 的同时消耗0.5mol
的同时消耗0.5mol
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组利用反应:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O H2C2O4来探究“外界条件对化学反应速率的影响”。实验时,先分别量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
(1)该反应是溶液之间发生的不可逆反应,改变压强对其反应速率的影响是______ (填序号)。
A.可能明显加快 B.可能明显减慢 C.几乎无影响,可以忽略
(2)甲同学设计了如下实验
①探究温度对化学反应速率影响的组合实验编号是__________ ,可探究温度对化学反应速率影响的实验编号是__________ 。
②实验a测得混合后溶液褪色的时间为40%,忽略混合前后 体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=______ 。
(3)在其它条件相同的情况下,乙同学用不同浓度的KMnO4酸性溶液实验,测得实验数据如下表所示:
依据表中数据,_____ (填“能”或“不能”)得出“溶液褪色所需时间越短,反应速率越快”的结论,理由是__________________ 。
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO42-该反应有催化作用
丙同学认为假设3不合理,其理由是__________ 。
②丁同学用如下实验证明假设2成立:在A和B两支试管中分别加入4mL0.2mol·L-1草酸溶液,再在A试管中加入lmL0.1mol·L-1MnSO4溶液、B试管中加入1mL蒸馏水,然后在两支试管中同时分别加入1mLO.1mol·L-1KMnO4酸性溶液,A试管溶液褪色的时间明显早于B试管。在B试管中加入1mL蒸馏水的目的是:__ 。
③同学们认为不宜用MnCl2溶液代替MnSO4溶液对该反应进行催化探究,其原因是(用离子方程式表示)_______________ 。
(1)该反应是溶液之间发生的不可逆反应,改变压强对其反应速率的影响是
A.可能明显加快 B.可能明显减慢 C.几乎无影响,可以忽略
(2)甲同学设计了如下实验
| 实验编号 | H2C2O4溶液 | KMnO4溶液 | 温度/℃ | ||
| 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | ||
| a | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| B | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| c | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
②实验a测得混合后溶液褪色的时间为40%,忽略混合前后 体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=
(3)在其它条件相同的情况下,乙同学用不同浓度的KMnO4酸性溶液实验,测得实验数据如下表所示:
| 实验编号 | 温度℃ | H2C2O4溶液 | KMnO4酸性溶液 | 褪色的时间(min) | ||
| 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | |||
| 1 | 25 | 0.10 | 4 | 0.2 | 8 | t1 |
| 2 | 25 | 0.010 | 4 | 0.2 | 8 | t2(t2<t3) |
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO42-该反应有催化作用
丙同学认为假设3不合理,其理由是
②丁同学用如下实验证明假设2成立:在A和B两支试管中分别加入4mL0.2mol·L-1草酸溶液,再在A试管中加入lmL0.1mol·L-1MnSO4溶液、B试管中加入1mL蒸馏水,然后在两支试管中同时分别加入1mLO.1mol·L-1KMnO4酸性溶液,A试管溶液褪色的时间明显早于B试管。在B试管中加入1mL蒸馏水的目的是:
③同学们认为不宜用MnCl2溶液代替MnSO4溶液对该反应进行催化探究,其原因是(用离子方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.在测定空气里氧气含量的实验中,小明采用了如图所用的装置:
装置一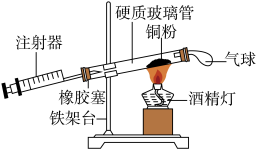 装置二
装置二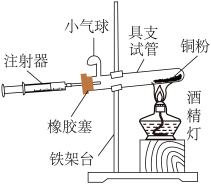
在由注射器和硬质玻璃管组成的密闭系统中留有40mL空气,给装有铜粉的玻璃管加热,观察密闭系统内空气体积变化。
(1)在实验加热过程中,缓慢推动注射器活塞的目的是__________ 。
(2)装置一比装置二更______ (填“合理”或“不合理”),理由是_________ 。
(3)小明测得的实验结果如下:
由此数据可推算出他测定的氧气的体积分数________ 21%(填“>”“<”或“=”),造成该实验出现误差的原因可能是____________ (填序号)。
①推动注射器活塞速度太快 ②未冷却至室温就读数 ③加入铜粉量太少
Ⅱ.H2O2分解速率受多种因素影响。实验测得70 ℃时不同条件下H2O2浓度随时间的变化如图所示。
图甲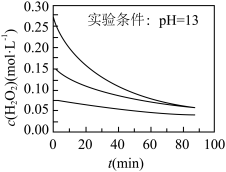 图乙
图乙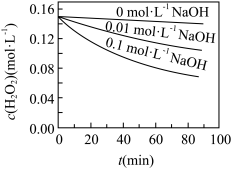
(4)根据上图,将不同条件对速率的影响情况补充完整:图甲表明,____________ ,H2O2分解速率越快;图乙表明,_________ ,H2O2分解速率越快。
装置一
 装置二
装置二
在由注射器和硬质玻璃管组成的密闭系统中留有40mL空气,给装有铜粉的玻璃管加热,观察密闭系统内空气体积变化。
(1)在实验加热过程中,缓慢推动注射器活塞的目的是
(2)装置一比装置二更
(3)小明测得的实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 15mL | 10mL |
由此数据可推算出他测定的氧气的体积分数
①推动注射器活塞速度太快 ②未冷却至室温就读数 ③加入铜粉量太少
Ⅱ.H2O2分解速率受多种因素影响。实验测得70 ℃时不同条件下H2O2浓度随时间的变化如图所示。
图甲
 图乙
图乙
(4)根据上图,将不同条件对速率的影响情况补充完整:图甲表明,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】化学反应中伴随着能量的变化。
(1)下列变化中属于吸热反应的是___________ (填字母)
①液态水汽化②将胆矾加热变为白色粉末③苛性钠固体溶于水④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰⑥干冰升华
A.①② B.②④ C.③ D.①⑥
(2)断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,则1mol N2生成NH3理论上能___________ (填“吸收”或“放出”)能量___________ kJ。
(3)某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
在此5组实验中,速率最快的是___________ (填实验序号);
实验1和2表明___________ 对反应速率有影响;
实验1和3表明___________ 对反应速率有影响。
(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图丙:
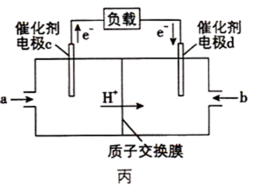
①则电极d是___________ (填“正极”或“负极”),电极c的电极反应式为___________ 。
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为___________ L。
(1)下列变化中属于吸热反应的是
①液态水汽化②将胆矾加热变为白色粉末③苛性钠固体溶于水④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰⑥干冰升华
A.①② B.②④ C.③ D.①⑥
(2)断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,则1mol N2生成NH3理论上能
(3)某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
| 序号 | 锌的质量/g | 锌的状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 反应前溶液的温度/℃ | 其他试剂 |
| 1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
| 2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
| 3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
| 4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
| 5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
在此5组实验中,速率最快的是
实验1和2表明
实验1和3表明
(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图丙:

①则电极d是
②若线路中转移2mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是______ 。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________ 。
(3)已知:Zn(s)+ O2(g)=ZnO(s) △H=-332kJ/mol
O2(g)=ZnO(s) △H=-332kJ/mol
ZnO(s)+ H2SO4(aq)=ZnSO4(aq)+ H2O(l) △H=-112kJ/mol
H2(g)+ O2(g)=H2O(l) △H=-286kJ/mol
O2(g)=H2O(l) △H=-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2时的反应热△H=______ kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______ (填“快”或“慢”),主要原因是_________ 。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_______ 。
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______ 。
(1)该反应的离子方程式是
(2)制H2时,用稀硫酸而不用浓硫酸,原因是
(3)已知:Zn(s)+
 O2(g)=ZnO(s) △H=-332kJ/mol
O2(g)=ZnO(s) △H=-332kJ/molZnO(s)+ H2SO4(aq)=ZnSO4(aq)+ H2O(l) △H=-112kJ/mol
H2(g)+
 O2(g)=H2O(l) △H=-286kJ/mol
O2(g)=H2O(l) △H=-286kJ/mol则Zn与稀H2SO4反应生成1mol H2时的反应热△H=
(4)该同学用如下装置进行实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料α-Fe2O3。其主要实验流程如下:

酸浸:用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁元素浸出率的有___________ (填序号)。
A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间
(2)NO和NO2的处理可用NaOH溶液吸收,主要反应为
NO+NO2+2OH−=2 +H2O
+H2O
2NO2+2OH−= +
+ +H2O
+H2O
下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
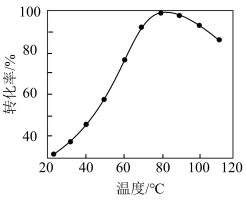
(3)在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO-,其他条件不变,HCO 转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO
转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是___________ 。
(4)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物(铁屑和活性炭的混合物)对水中Cu2+和Pb2+的去除率,结果如图所示。
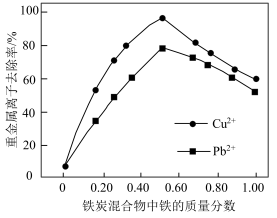
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是___________ 。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加Cu2+和Pb2+的去除率不升反降,其主要原因是___________ 。

酸浸:用一定浓度的H2SO4溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下列措施能提高铁元素浸出率的有
A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间
(2)NO和NO2的处理可用NaOH溶液吸收,主要反应为
NO+NO2+2OH−=2
 +H2O
+H2O2NO2+2OH−=
 +
+ +H2O
+H2O下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
(3)在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO-,其他条件不变,HCO
 转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO
转化为HCOO-的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,HCO 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是
(4)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物(铁屑和活性炭的混合物)对水中Cu2+和Pb2+的去除率,结果如图所示。

①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加Cu2+和Pb2+的去除率不升反降,其主要原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
(1)请完成此实验设计,其中V7=______ ,V9=______ 。
(2)在D组实验中,按照反应发生的先后顺序写出发生反应的离子方程式:①______ 、②_____ 。
(3)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:___ 。
| A | B | C | D | E | F | |
| 4mol/LH2SO4溶液(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
(2)在D组实验中,按照反应发生的先后顺序写出发生反应的离子方程式:①
(3)该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】从矿石中提取金(Au)是获取贵金属的主要来源,工业上常以 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。
已知:① 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。
②几种物质或离子的颜色如表所示:
回答下列问题:
(1) 中提供空轨道的为
中提供空轨道的为_______ (填名称,下同),配体为_______ 。配制过程中氨水需过量,其原因是_______ 。
某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一: 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。
猜想二: 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。
验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:_______ 。据此有人得出结论:猜想二不成立,但有人觉得溶液的酸碱性对物质的性质有一定影响,为验证猜想二是否成立,设计如下实验:
步骤一:用pH试纸测浸金液的pH,其操作为_______ 。
步骤二:配制与浸金液pH相同的 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、_______ 。
步骤三:将一块金片放入配制的 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到_______ ,则猜想二可能成立。
(3)某小组设计如图所示实验验证猜想一。_______ (填锥形瓶中出现的实验现象),则猜想一可能成立;打开瓶塞后的现象用离子方程式表示为_______ 。
 溶液、氨水和
溶液、氨水和 溶液为原料配制浸金液{含
溶液为原料配制浸金液{含 }。
}。已知:①
 在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的
在酸性环境中易分解,在碱性环境中较稳定,能与金形成稳定的 。
。②几种物质或离子的颜色如表所示:
| 物质或离子 | Au | 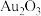 |  |  |  |
| 颜色 | 黄色 | 棕黑 | 蓝色 | 无色 | 无色 |
(1)
 中提供空轨道的为
中提供空轨道的为某科研小组对该浸金液的浸金原理进行探究:
提出猜想:
猜想一:
 吸附在金表面,在
吸附在金表面,在 的作用下生成
的作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 被空气中的氧气氧化成
被空气中的氧气氧化成 参与循环。
参与循环。猜想二:
 吸附在金表面,在氧气作用下生成
吸附在金表面,在氧气作用下生成 和
和 ,
, 迅速被
迅速被 替换成
替换成 ,
, 与
与 生成的
生成的 参与循环。
参与循环。验证猜想:
(2)俗话说“真金不怕火炼”,从化学性质的角度说明:
步骤一:用pH试纸测浸金液的pH,其操作为
步骤二:配制与浸金液pH相同的
 溶液。用
溶液。用 固体配制一定物质的量浓度的
固体配制一定物质的量浓度的 溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、
溶液所用的玻璃仪器包括量筒、烧杯、玻璃棒、步骤三:将一块金片放入配制的
 溶液中,并通入空气,一段时间后,若观察到
溶液中,并通入空气,一段时间后,若观察到(3)某小组设计如图所示实验验证猜想一。
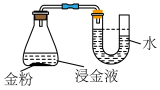
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】云南是有色金属王国。利用云南钛铁精矿(主要成分为TiO2、Fe2TiO3, 还有少量SiO2、MgO等)制备还原铁粉和富钛料(制钛白粉的优质原料)的试验研究工艺流程如下:
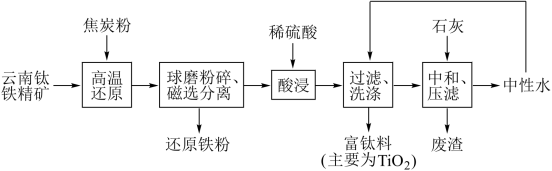
回答下列问题:.
(1) Fe2TiO3可用氧化物的形式表示为_______ (其中铁元素的化合价为+3); Fe2TiO3 被焦炭粉还原的化学方程式为 ________ ; 还原时间对还原铁粉中铁含量的影响如图所示,可确定还原时间为 _________ h较合理。

(2)磁选可分离出还原铁粉,是利用金属铁具有_________ 的物理性质。
(3)若磁选分离不完全,所得尾渣酸浸时会有气泡产生,该反应的离子方程式为__________ ;富钛料.中除TiO2外,还含有 _______ (填化学式)。
(4)已知CaSO4的Ksp=9.1×10-6。中性水中c(Ca2+)=_______ (忽略残留的其它金属离子)。

回答下列问题:.
(1) Fe2TiO3可用氧化物的形式表示为

(2)磁选可分离出还原铁粉,是利用金属铁具有
(3)若磁选分离不完全,所得尾渣酸浸时会有气泡产生,该反应的离子方程式为
(4)已知CaSO4的Ksp=9.1×10-6。中性水中c(Ca2+)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,极易水解,遇潮湿空气会产生白雾。

(1)化合物SO2Cl2中S元素的化合价是________ 。
(2)实验室中制备氯气时为得到干燥纯净的氯气,应将气体依次通过盛有________ 和___________ 的洗气瓶。
(3)用如图所示装置制备SO2Cl2。
①B中冷凝水从________ (填“m”或“n”)口进入。
②C中盛放的试剂是________ 。
(4)向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl-,写出SO2Cl2与H2O反应的化学方程式:_______________ 。
查阅资料:SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,极易水解,遇潮湿空气会产生白雾。

(1)化合物SO2Cl2中S元素的化合价是
(2)实验室中制备氯气时为得到干燥纯净的氯气,应将气体依次通过盛有
(3)用如图所示装置制备SO2Cl2。
①B中冷凝水从
②C中盛放的试剂是
(4)向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl-,写出SO2Cl2与H2O反应的化学方程式:
您最近一年使用:0次



