已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)该实验①、②可探究______________ 对反应速率的影响,因此V1=______________ ,V2=______________ ;
(2)实验①、③可探究硫酸浓度对反应速率的影响,因此V5=______________ 。
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(2)实验①、③可探究硫酸浓度对反应速率的影响,因此V5=
更新时间:2020-11-06 18:24:31
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某同学利用反应: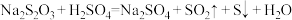 ,探究外界条件对化学反应速率的影响。反应过程中溶液出现浅黄色浑浊和有刺激性气味的气体,得到各组实验数据如下表:
,探究外界条件对化学反应速率的影响。反应过程中溶液出现浅黄色浑浊和有刺激性气味的气体,得到各组实验数据如下表:
(1)实验Ⅰ、Ⅱ探究_______ 对化学反应速率的影响。V=_______ ,加入VmL水的目的是_______ 。
(2)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是_______ 。
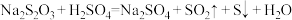 ,探究外界条件对化学反应速率的影响。反应过程中溶液出现浅黄色浑浊和有刺激性气味的气体,得到各组实验数据如下表:
,探究外界条件对化学反应速率的影响。反应过程中溶液出现浅黄色浑浊和有刺激性气味的气体,得到各组实验数据如下表:| 实验 编号 | 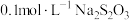 溶液 溶液 | 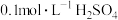 溶液 溶液 | 蒸馏水 | 温度/℃ | ||
| 浓度/(mol/L) | 体积/mL | 浓度/(mol/L) | 体积/mL | 体积/mL | ||
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | V | 20 |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | 20 |
| Ⅲ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | 30 |
(2)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】Na2S2O3用于照相业定影剂、鞣革时重铬酸盐的还原剂等.
(1)Na2S2O3溶液与稀硫酸的反应可探究外界条件对化学反应速率的影响.Na2S2O3溶液与稀硫酸反应的离子方程式为_______ ;表格中H2O的体积x=_______ ,其中探究温度对化学反应速率的影响的实验是_______ (填序号).
(2)工业上可用反应 制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
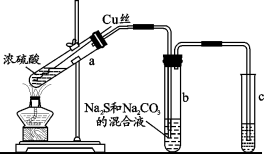
①试管a中的化学方程式为_______ .
②反应结束后,将试管b中溶液水浴加热浓缩,_______ ,经过滤、乙醇洗涤晶体、干燥,得到 。用乙醇而不用水洗涤晶体的原因
。用乙醇而不用水洗涤晶体的原因_______ .
③测定产品纯度:准确称取mg晶体,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol·L-1碘的标准溶液滴定,反应原理为: 。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设
。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设 相对分子质量为M)
相对分子质量为M)_______ (写出计算表达式)
(1)Na2S2O3溶液与稀硫酸的反应可探究外界条件对化学反应速率的影响.Na2S2O3溶液与稀硫酸反应的离子方程式为
| 实验 | 反应温度/℃ | Na2S2O溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| Ⅰ | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| Ⅱ | 20 | 5 | 0.2 | 10 | 0.2 | x |
| Ⅲ | 40 | 10 | 0.1 | 10 | 0.1 | 0 |
 制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
①试管a中的化学方程式为
②反应结束后,将试管b中溶液水浴加热浓缩,
 。用乙醇而不用水洗涤晶体的原因
。用乙醇而不用水洗涤晶体的原因③测定产品纯度:准确称取mg晶体,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol·L-1碘的标准溶液滴定,反应原理为:
 。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设
。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设 相对分子质量为M)
相对分子质量为M)
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大__ min(填0~1、1~2、2~3、3~4、4~5),原因是___ 。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率___ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是___ 。
A.蒸馏水 B.KCl溶液C.KNO3溶液D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
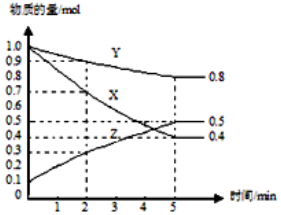
①该反应的化学方程式是___ 。
②该反应达到平衡状态的标志是___ 。
A.Y的体积分数在混合气体中保持不变
B.2v(X)=3v(Z)
C.容器内气体压强保持不变
D.X、Y、Z三种气体的浓度之比为3:1:2
E.生成1molY的同时消耗2molZ
F.容器内气体的平均相对分子质量保持不变
③2min内Y的转化率为___ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段反应速率最大
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是
A.蒸馏水 B.KCl溶液C.KNO3溶液D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.2v(X)=3v(Z)
C.容器内气体压强保持不变
D.X、Y、Z三种气体的浓度之比为3:1:2
E.生成1molY的同时消耗2molZ
F.容器内气体的平均相对分子质量保持不变
③2min内Y的转化率为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
(1)通过实验A、B,可探究出H2C2O4溶液浓度的改变对反应速率的影响,其中V1=___________ ;通过实验___________ 可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是___________ 。
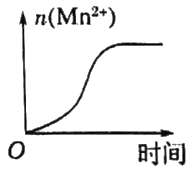
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+,该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并认为造成此种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊的作用,则该作用是___________ ,相应的粒子最可能是___________ 。
| 实验序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间s | ||||
| KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
| V/mL | c(mol/L) | V/mL | c(mol/L) | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | 293 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t1 |
(2)若t1<8,则由此实验可以得出的结论是
(3)该反应中有无色无味气体产生,且锰被还原为Mn2+,该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间变化的趋势如图所示,并认为造成此种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊的作用,则该作用是

您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某实验探究小组用酸性 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性
溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性 溶液的用量均为4mL,
溶液的用量均为4mL, 溶液(0.100mol/L)的用量均为2mL。
溶液(0.100mol/L)的用量均为2mL。
已知 。
。
(1)写出反应的离子方程式:___________ 。
(2)已知部分实验数据如下:
实验目的:
a.实验①和②探究___________ 对该反应速率的影响;
b.实验①和③探究___________ 对该反应速率的影响;
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度___________ K,催化剂用量g,酸性 溶液的浓度
溶液的浓度___________ mol/L。该反应的催化剂应选择___________ (填写“ ”或“
”或“ ”)。
”)。
 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性
溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性 溶液的用量均为4mL,
溶液的用量均为4mL, 溶液(0.100mol/L)的用量均为2mL。
溶液(0.100mol/L)的用量均为2mL。已知
 。
。(1)写出反应的离子方程式:
(2)已知部分实验数据如下:
| 实验编号 | T/K | 催化剂的用量/g | 酸性 溶液的浓度/(mol/L) 溶液的浓度/(mol/L) |
| ① | 298 | 0.5 | 0.010 |
| ② | 298 | 0.5 | 0.001 |
| ③ | 323 | 0.5 | 0.010 |
| ④ |
a.实验①和②探究
b.实验①和③探究
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度
 溶液的浓度
溶液的浓度 ”或“
”或“ ”)。
”)。
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】I.分别取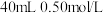 盐酸与
盐酸与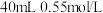 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:
(1)本实验除烧杯、量筒、环形玻璃搅拌棒外还缺少的玻璃仪器名称为_______ ,大小烧杯间需要填满碎泡沫塑料的目的是_______ 。
(2)若某同学通过该实验测定出中和热 偏大,请分析可能的原因是
偏大,请分析可能的原因是_______ (填序号)。
A.用量筒量取盐酸时仰视读数
B.分多次将 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
(3)写出混合溶液中滴入 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(4)表中的V=_______  ,
, 、
、 、
、 由小到大的顺序为
由小到大的顺序为_______ 。
(5)对比实验①②可推测实验结论为_______ 。
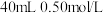 盐酸与
盐酸与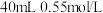 氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热
氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热 。请回答下列问题:
。请回答下列问题:(1)本实验除烧杯、量筒、环形玻璃搅拌棒外还缺少的玻璃仪器名称为
(2)若某同学通过该实验测定出中和热
 偏大,请分析可能的原因是
偏大,请分析可能的原因是A.用量筒量取盐酸时仰视读数
B.分多次将
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中C.将盐酸错取为等浓度的醋酸
Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知
 溶液、
溶液、 溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)
溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)向烧杯中加入的试剂及用量/ | |||||||
0.1 溶液 溶液 | 0.1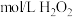 溶液 溶液 | 0.1 溶液 溶液 | 淀粉溶液 |  | 时间/s | ||
| ① | 25℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 |  |
| ② | 40℃ | 20.0 | 10.0 | 5.0 | 1.0 | 0.0 |  |
| ③ | 25℃ | 20.0 | 5.0 | 5.0 | 1.0 | V |  |
 溶液反应的离子方程式为
溶液反应的离子方程式为(4)表中的V=
 ,
, 、
、 、
、 由小到大的顺序为
由小到大的顺序为(5)对比实验①②可推测实验结论为
您最近半年使用:0次



