甲醇是一种重要的有机原料,在催化剂的作用下, 和
和 反应可生成甲醇
反应可生成甲醇 和副产物
和副产物 ,反应如下:
,反应如下:
反应①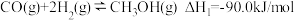
反应②
反应③
反应④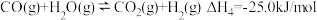
 、
、 、
、 、
、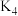 分别表示反应①、②、③、④的平衡常数.
分别表示反应①、②、③、④的平衡常数.
回答下列问题:
(1)反应②的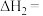
_____  ,
, 与
与 和
和 的关系为
的关系为
______ .
(2)图1中能正确表示反应①的平衡常数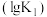 随温度变化的曲线为
随温度变化的曲线为________ (填曲线字母),其判断理由为____________ .
(3)为探究不同催化剂对 和
和 生成
生成 的选择性效果,某实验室控制
的选择性效果,某实验室控制 和
和 的初始投料比为
的初始投料比为 进行实验,得到如下表1数据:
进行实验,得到如下表1数据:
①由表1可知,反应Ⅰ的最佳催化剂为_______________ .
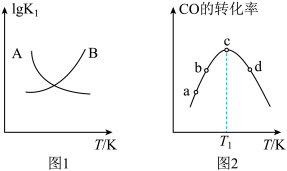
②图2中, 时
时 转化率最大的原因是
转化率最大的原因是_________________ .
③有利于提高 转化为
转化为 的平衡转化率的措施有
的平衡转化率的措施有__________ .
A.使用催化剂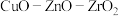
B.适当降低反应温度
C.增大 和
和 的初始投料比
的初始投料比
D.恒容下,再充入 和
和
(4)已知 ,反应
,反应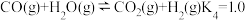 .该温度下,在某时刻体系中
.该温度下,在某时刻体系中 、
、 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时上述反应的
,则此时上述反应的
_______ 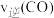 (填“>”、“<”或“=”)达到平衡时
(填“>”、“<”或“=”)达到平衡时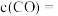
_____  .
.
 和
和 反应可生成甲醇
反应可生成甲醇 和副产物
和副产物 ,反应如下:
,反应如下:反应①
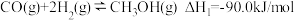
反应②

反应③

反应④
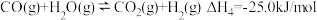
 、
、 、
、 、
、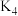 分别表示反应①、②、③、④的平衡常数.
分别表示反应①、②、③、④的平衡常数.回答下列问题:
(1)反应②的
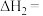
 ,
, 与
与 和
和 的关系为
的关系为
(2)图1中能正确表示反应①的平衡常数
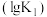 随温度变化的曲线为
随温度变化的曲线为
(3)为探究不同催化剂对
 和
和 生成
生成 的选择性效果,某实验室控制
的选择性效果,某实验室控制 和
和 的初始投料比为
的初始投料比为 进行实验,得到如下表1数据:
进行实验,得到如下表1数据: | 时间/ | 催化剂种类 | 甲醇的含量(%) |
| 450 | 10 |  | 78 |
| 450 | 10 | 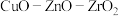 | 88 |
| 450 | 10 |  | 46 |
②图2中,
 时
时 转化率最大的原因是
转化率最大的原因是③有利于提高
 转化为
转化为 的平衡转化率的措施有
的平衡转化率的措施有A.使用催化剂
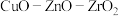
B.适当降低反应温度
C.增大
 和
和 的初始投料比
的初始投料比D.恒容下,再充入
 和
和
(4)已知
 ,反应
,反应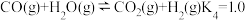 .该温度下,在某时刻体系中
.该温度下,在某时刻体系中 、
、 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时上述反应的
,则此时上述反应的
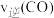 (填“>”、“<”或“=”)达到平衡时
(填“>”、“<”或“=”)达到平衡时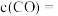
 .
.
更新时间:2020-11-17 00:11:58
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】I、目前我国主要使用肼(N2H4)作为卫星发射所用燃料。
(1)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。
已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol−1K1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol−1K2
写出反应③液体燃料N2H4与液态N2O4反应生成N2和H2O的热化学方程式:___________ ,K1、K2、K3之间的关系:___________
(2)若已知下列数据:
试根据表中数据计算出N-H的键能:___________ kJ·mol−1
Ⅱ、在体积为2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表所示:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表所示:
(3)该反应为___________ 反应(填“吸热”、“放热”),原因为___________
(4)830℃下,若向容器中分别加入2molH2和2molCO2,10s后达到平衡,则这段时间内 (H2)=
(H2)=___________ ,转化率α(CO2)=___________
(5)1200℃时,在某时刻体系中CO2、H2、CO、H2O的物质的量分别为4mol、4mol、8mol、8mol,则此时上述反应的平衡向___________ 移动(填“正向”、“逆向”或“不”)
Ⅲ、已知在不同温度下,甲烷隔绝空气有可能发生如下两个裂解反应:①CH4(g)→C(s)+2H2(g),②2CH4(g)→C2H4(g)+3H2(g)。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:
反应①的ΔH(298K)=+74.848kJ/mol,ΔS(298K)=+80.674J/(mol·K)
反应②的ΔH(298K)=+376.426kJ/mol,ΔS(298K)=+220.211J/(mol·K)
已知,上述反应的焓变和熵变随温度变化很小。请帮助这位同学回答下列问题:
(6)反应①在___________ (填“高温”或“低温”)下能自发进行
(7)为了提高甲烷的炭化程度,下列温度最合适的是___________
(1)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。
已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol−1K1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol−1K2
写出反应③液体燃料N2H4与液态N2O4反应生成N2和H2O的热化学方程式:
(2)若已知下列数据:
| 化学键 | N-N | N≡N | H-O | O=O |
| 键能/kJ·mol-1 | 190 | 946 | 462.8 | 498.8 |
试根据表中数据计算出N-H的键能:
Ⅱ、在体积为2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表所示:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表所示:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(4)830℃下,若向容器中分别加入2molH2和2molCO2,10s后达到平衡,则这段时间内
 (H2)=
(H2)=(5)1200℃时,在某时刻体系中CO2、H2、CO、H2O的物质的量分别为4mol、4mol、8mol、8mol,则此时上述反应的平衡向
Ⅲ、已知在不同温度下,甲烷隔绝空气有可能发生如下两个裂解反应:①CH4(g)→C(s)+2H2(g),②2CH4(g)→C2H4(g)+3H2(g)。某同学为了得到用天然气制取炭黑的允许温度范围和最佳温度,查阅资料,得到如下热力学数据:
反应①的ΔH(298K)=+74.848kJ/mol,ΔS(298K)=+80.674J/(mol·K)
反应②的ΔH(298K)=+376.426kJ/mol,ΔS(298K)=+220.211J/(mol·K)
已知,上述反应的焓变和熵变随温度变化很小。请帮助这位同学回答下列问题:
(6)反应①在
(7)为了提高甲烷的炭化程度,下列温度最合适的是___________
| A.905.2K | B.927K | C.1273K | D.2000K |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】NH3是一种重要的化工原料,其催化分解是制备高纯度氢的有效途径之一、NH3在某金属催化剂表面发生分解时,经历了以下历程:
①NH3(g)=NH2(g)+H(g) ∆H1
②NH2(g)+H(g)=NH(g)+2H(g) ∆H2
③NH(g)+2H(g)=N(g)+3H(g) ∆H3
④N(g)+N(g)=N2(g) ∆H4
⑤H(g)+H(g)=H2(g) ∆H5
回答下列问题:
(1)2NH3(g)=N2(g)+3H2(g)的ΔH=___________ 。
(2)在NH3催化分解过程中,部分历程的相对能量变化如图所示(TS表示过渡态),三步脱氢反应中速率最慢的是第___________ 步,该步反应的活化能为___________ kJ/mol(已知:1eV=1.6×10-19J)。

(3)相同质量的同种催化剂,在载体上的分散度越高,催化作用越强,原因是___________ ;一定条件下,NH3在少量某催化剂作用下分解的实验数据如下表:
分析表中数据可知,随着反应进行,c(NH3)减小,平均反应速率___________ 。(填“增大”“减小”或“不变"),对该变化的合理解释是___________
(4)某温度下,在一容积为1L的刚性密闭容器中,投入一定量的NH3发生催化分解反应,起始压强为P0MPa,若反应达到平衡时,容器内压强为1.75P0MPa,则NH3的平衡分解率α(NH3)=___________ ,该温度下,反应的平衡常数Kp=___________ MPa2(用含p0的式子表示,分压=体积分数×总压)。
①NH3(g)=NH2(g)+H(g) ∆H1
②NH2(g)+H(g)=NH(g)+2H(g) ∆H2
③NH(g)+2H(g)=N(g)+3H(g) ∆H3
④N(g)+N(g)=N2(g) ∆H4
⑤H(g)+H(g)=H2(g) ∆H5
回答下列问题:
(1)2NH3(g)=N2(g)+3H2(g)的ΔH=
(2)在NH3催化分解过程中,部分历程的相对能量变化如图所示(TS表示过渡态),三步脱氢反应中速率最慢的是第

(3)相同质量的同种催化剂,在载体上的分散度越高,催化作用越强,原因是
| 反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| c(NH3)/mol/L | c0 | 0.9c0 | 0.8c0 | 0.7c0 | 0.6c0 | 0.5c0 |
分析表中数据可知,随着反应进行,c(NH3)减小,平均反应速率
(4)某温度下,在一容积为1L的刚性密闭容器中,投入一定量的NH3发生催化分解反应,起始压强为P0MPa,若反应达到平衡时,容器内压强为1.75P0MPa,则NH3的平衡分解率α(NH3)=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如图。
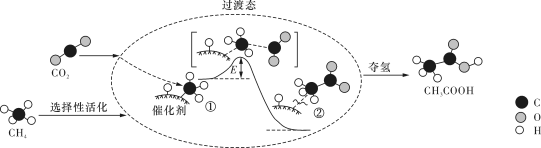
(1)生成 CH3COOH总反应的原子利用率为______ ,该催化剂______ (填能或不能)有效提高反应物的平衡转化率;
(2)如图是1 mol CH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化

①CH4完全燃烧的活化能是______ kJ/mol。
②在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式______ ;
(3)在密闭容器中充入2molCH4(g)和1molO2(g),在不同条件下反应:2CH4(g)+O2(g)⇌2CH3OH(g),实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
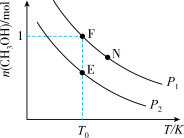
①P1时升高温度n(CH3OH)______ (填“增大”、“减小”或“不变”);
②E、F、N点对应的化学反应速率由大到小的顺序为______ (用v(E)、v(F)、v(N)表示);
③下列能提高CH4平衡转化率的措施是______ (填序号);
a.减小压强 b.增大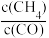 投料比 c.及时分离产物
投料比 c.及时分离产物
④若F点n(CH3OH)=1mol,总压强为2.5MPa,则T0时F点用分压强代替浓度表示的平衡常数Kp=______ 。

(1)生成 CH3COOH总反应的原子利用率为
(2)如图是1 mol CH4完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化

①CH4完全燃烧的活化能是
②在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式
(3)在密闭容器中充入2molCH4(g)和1molO2(g),在不同条件下反应:2CH4(g)+O2(g)⇌2CH3OH(g),实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。

①P1时升高温度n(CH3OH)
②E、F、N点对应的化学反应速率由大到小的顺序为
③下列能提高CH4平衡转化率的措施是
a.减小压强 b.增大
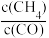 投料比 c.及时分离产物
投料比 c.及时分离产物④若F点n(CH3OH)=1mol,总压强为2.5MPa,则T0时F点用分压强代替浓度表示的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】为了早日实现碳达峰和碳中和,各国科学家研究了多种二氧化碳的捕集与利用途径。
(1)中科院天津工生所宣布实现二氧化碳到淀粉合成只有11步反应的人工合成途径,其中最关键的第一步反应如图所示,该反应的化学方程式为_______ ,图中设计有利于提高 转化效率的方案有
转化效率的方案有_______ (填标号)。

A.使用ZnO—ZrO2催化剂
B.冷凝混合气体分离出CH3OH
C.循环利用CO2和氢气
(2) 催化加氢可以合成乙烯,反应方程式为
催化加氢可以合成乙烯,反应方程式为
 ,起始时将
,起始时将 、
、 按
按 充入
充入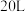 恒容密闭容器中,不同温度下平衡时
恒容密闭容器中,不同温度下平衡时 和
和 的物质的量如图所示。
的物质的量如图所示。

①m_______ (填“>”或“<”)0。
②下列说法正确的是_______ (填标号)。
A.使用催化剂,可降低反应的活化能,加快反应速率
B.其他条件不变时,若扩大容器容积,则v正减小,v逆增大
C.测得容器内混合气体的密度不再随时间改变时,说明反应已达到平衡
③ 时,达到平衡,
时,达到平衡, 的平衡转化率为
的平衡转化率为_______ %(保留一位小数)。
④在恒容密闭容器中,反应温度、投料比 对
对 平衡转化率的影响如图所示,a
平衡转化率的影响如图所示,a_______ (填“>”、“<”或“=”)3;M、N两点的反应平衡常数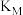
_______ (填“>”、“<”或“=”) ,判断的理由是
,判断的理由是_______ 。

(1)中科院天津工生所宣布实现二氧化碳到淀粉合成只有11步反应的人工合成途径,其中最关键的第一步反应如图所示,该反应的化学方程式为
 转化效率的方案有
转化效率的方案有
A.使用ZnO—ZrO2催化剂
B.冷凝混合气体分离出CH3OH
C.循环利用CO2和氢气
(2)
 催化加氢可以合成乙烯,反应方程式为
催化加氢可以合成乙烯,反应方程式为
 ,起始时将
,起始时将 、
、 按
按 充入
充入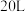 恒容密闭容器中,不同温度下平衡时
恒容密闭容器中,不同温度下平衡时 和
和 的物质的量如图所示。
的物质的量如图所示。
①m
②下列说法正确的是
A.使用催化剂,可降低反应的活化能,加快反应速率
B.其他条件不变时,若扩大容器容积,则v正减小,v逆增大
C.测得容器内混合气体的密度不再随时间改变时,说明反应已达到平衡
③
 时,达到平衡,
时,达到平衡, 的平衡转化率为
的平衡转化率为④在恒容密闭容器中,反应温度、投料比
 对
对 平衡转化率的影响如图所示,a
平衡转化率的影响如图所示,a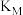
 ,判断的理由是
,判断的理由是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】氮化硅(Si3N4)是一种新型陶瓷材料,它由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)。
Si3N4(s)+6CO(g)。
(1)该反应的平衡常数表达式为K=_________ ;
(2)若知上述反应为放热反应,则其反应热△H___ 0(填“>”、“<”或“=”);升高温度,其平衡常数值___ (填“增大”、“减小”或“不变”);若已知CO生成速率为v(CO)=18mol•L﹣1•min﹣1,则N2消耗速率为v(N2)=_____ ;
(3)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.图中t4时引起平衡移动的条件可能是___ ;图中表示平衡混合物中CO的含量最高的一段时间是_____ 。
 Si3N4(s)+6CO(g)。
Si3N4(s)+6CO(g)。(1)该反应的平衡常数表达式为K=
(2)若知上述反应为放热反应,则其反应热△H
(3)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与时间t的关系如图.图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个反应,分别生成CH3OH和CO。反应的热化学方程式如下:
I.CO2(g)+3H2(g) CH3OH(g)+H2O(g)∆H1=-53.7kJ/mol
CH3OH(g)+H2O(g)∆H1=-53.7kJ/mol
II.CO2(g)+H2(g) CO(g)+H2O(g)∆H2
CO(g)+H2O(g)∆H2
某实验控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
[备注]Cat.1:Cu/ZnO纳米棒,Cat.2:Cu/ZnO纳米片;
甲醇选择性:转化的CO2中生成甲醇的百分比。
已知:①CO和H2的标准燃烧热分别为-283.0kJ/mol和285.8kJ/mol
②H2O(1) H2O(g)∆H3=+440kJ/mol
H2O(g)∆H3=+440kJ/mol
请回答(不考虑温度对∆H的影响):
(1)a.反应II的∆H2=____ kJ/mol。
b.800℃时,反应I和II对应的平衡常数分别为1.0和2.5,则该温度下反应:CO(g)+2H2(g) CH3OH(g)的平衡常数K的数值为
CH3OH(g)的平衡常数K的数值为_____ 。
(2)在图中分别画出I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程-能量”示意图(在图中标注出相应的催化剂)____ 。

(3)工业生产甲醇还有如下方法:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
副反应:2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
若生产过理中在恒压条件下通入水蒸气,从化学平衡的角度分析该操作对生产甲醇带来的利和弊____ 。
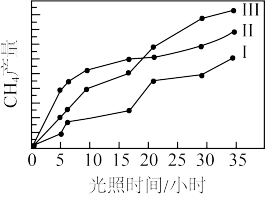
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外线照射时,在不同催化剂(1、I、III)作用下,CH4产量随光照时间的变化如下图所示。下列说法正确的是____
A.催化剂能加快化学反应速率,在反应开始时对正反应的催化效果更好
B.从图中可知催化剂I的催化效果更好
C.若光照时间足够长,三条由线将相交于一点
D.光照15h前,无论用所给的哪种催化剂,该反应均未达到平衡
(5)人们正在研究某种锂一空气电池,它是一种环境友好的蓄电池。放电时的总反应为:4Li+O2=2Li2O。在充电时,阳极区发生的过程比较复杂,目前普遍认可是按两步反应进行,请补充完整。
电极反应式:______ 和Li2O2-2e-=2Li++O2
I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)∆H1=-53.7kJ/mol
CH3OH(g)+H2O(g)∆H1=-53.7kJ/molII.CO2(g)+H2(g)
 CO(g)+H2O(g)∆H2
CO(g)+H2O(g)∆H2某实验控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒,Cat.2:Cu/ZnO纳米片;
甲醇选择性:转化的CO2中生成甲醇的百分比。
已知:①CO和H2的标准燃烧热分别为-283.0kJ/mol和285.8kJ/mol
②H2O(1)
 H2O(g)∆H3=+440kJ/mol
H2O(g)∆H3=+440kJ/mol请回答(不考虑温度对∆H的影响):
(1)a.反应II的∆H2=
b.800℃时,反应I和II对应的平衡常数分别为1.0和2.5,则该温度下反应:CO(g)+2H2(g)
 CH3OH(g)的平衡常数K的数值为
CH3OH(g)的平衡常数K的数值为(2)在图中分别画出I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程-能量”示意图(在图中标注出相应的催化剂)

(3)工业生产甲醇还有如下方法:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)副反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)若生产过理中在恒压条件下通入水蒸气,从化学平衡的角度分析该操作对生产甲醇带来的利和弊
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外线照射时,在不同催化剂(1、I、III)作用下,CH4产量随光照时间的变化如下图所示。下列说法正确的是
A.催化剂能加快化学反应速率,在反应开始时对正反应的催化效果更好
B.从图中可知催化剂I的催化效果更好
C.若光照时间足够长,三条由线将相交于一点
D.光照15h前,无论用所给的哪种催化剂,该反应均未达到平衡

(5)人们正在研究某种锂一空气电池,它是一种环境友好的蓄电池。放电时的总反应为:4Li+O2=2Li2O。在充电时,阳极区发生的过程比较复杂,目前普遍认可是按两步反应进行,请补充完整。
电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】资料显示,可用次氯酸钠处理废水中的氨氮(NH3),使其转化为氮气除去,其主要反应如下:
① NH3(aq)+ HClO(aq)═ NH2Cl(aq)+ H2O(l)
② 2NH2Cl(aq)+ HClO(aq)═ N2(g)+ H2O(l)+ 3HCl(aq)
(1)在其他条件不变的情况下,向一定量废水中逐滴滴加次氯酸钠溶液,氨氮去除率随n(NaClO)/n(NH3)的变化曲线如下:

Ⅰ.物质NH2Cl中氮元素的化合价是____________ 。
Ⅱ.a-b点间,溶液中氨氮去除率迅速提高的原因是__________ 。
(2)Ⅰ.反应①②中HClO 的来源用化学用语解释是__________ 。
Ⅱ.实验测得,废水中pH与氨氮去除率如图所示:

pH较高时,氨氮去除率下降的原因是__________ 。
pH较低时,氨氮去除率也下降,可能的原因是__________ 。
(3)运用上述原理去除废水中的氨氮,可结合下图所示的电解法。

Ⅰ. a极为__________ 。
Ⅱ. d极反应式为__________ 。
① NH3(aq)+ HClO(aq)═ NH2Cl(aq)+ H2O(l)
② 2NH2Cl(aq)+ HClO(aq)═ N2(g)+ H2O(l)+ 3HCl(aq)
(1)在其他条件不变的情况下,向一定量废水中逐滴滴加次氯酸钠溶液,氨氮去除率随n(NaClO)/n(NH3)的变化曲线如下:

Ⅰ.物质NH2Cl中氮元素的化合价是
Ⅱ.a-b点间,溶液中氨氮去除率迅速提高的原因是
(2)Ⅰ.反应①②中HClO 的来源用化学用语解释是
Ⅱ.实验测得,废水中pH与氨氮去除率如图所示:

pH较高时,氨氮去除率下降的原因是
pH较低时,氨氮去除率也下降,可能的原因是
(3)运用上述原理去除废水中的氨氮,可结合下图所示的电解法。

Ⅰ. a极为
Ⅱ. d极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】CO2的资源化利用有利于碳中和目标的实现。回答下列问题:
(1)将CO2催化加氢转化为CH3OCH3是资源化利用的途径之一,适当温度下,在催化剂存在的CO2加氢反应器中,主要反应有:
ⅰ.

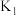
ⅱ.

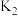
ⅲ.


①
_____________ ,
_____________ (用含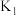 、
、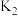 的式子表示)。
的式子表示)。
②将1mol CO2、3mol H2充入2L的刚性容器中仅发生反应ⅲ,测得反应进行到10min时,CO2的转化率与催化剂(X、Y、Z)、温度(T)间关系如图所示:

则三种催化剂条件下的反应中, 温度下活化能最大的是
温度下活化能最大的是_______ (填“Ⅰ”、“Ⅱ”、“Ⅲ”),这段时间a点对应氢气的反应速率为_____  ;转化率
;转化率 的原因可能是
的原因可能是__________________ 。
(2)CO2与H2也可用于制备甲醇:
 。TK时,向压强为9MPa的恒压容器中充入3molCO2和7molH2,达到平衡时,CH3OH的体积分数为
。TK时,向压强为9MPa的恒压容器中充入3molCO2和7molH2,达到平衡时,CH3OH的体积分数为 。
。
①写出能提高H2转化率的两种方法:_______ 。
②H2和CO2的平衡转化率之比为____ ;TK时,该反应的平衡常数
____  (以分压表示,分压=总压×气体物质的量分数)
(以分压表示,分压=总压×气体物质的量分数)
(1)将CO2催化加氢转化为CH3OCH3是资源化利用的途径之一,适当温度下,在催化剂存在的CO2加氢反应器中,主要反应有:
ⅰ.


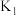
ⅱ.


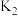
ⅲ.



①


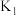 、
、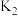 的式子表示)。
的式子表示)。②将1mol CO2、3mol H2充入2L的刚性容器中仅发生反应ⅲ,测得反应进行到10min时,CO2的转化率与催化剂(X、Y、Z)、温度(T)间关系如图所示:

则三种催化剂条件下的反应中,
 温度下活化能最大的是
温度下活化能最大的是 ;转化率
;转化率 的原因可能是
的原因可能是(2)CO2与H2也可用于制备甲醇:

 。TK时,向压强为9MPa的恒压容器中充入3molCO2和7molH2,达到平衡时,CH3OH的体积分数为
。TK时,向压强为9MPa的恒压容器中充入3molCO2和7molH2,达到平衡时,CH3OH的体积分数为 。
。①写出能提高H2转化率的两种方法:
②H2和CO2的平衡转化率之比为

 (以分压表示,分压=总压×气体物质的量分数)
(以分压表示,分压=总压×气体物质的量分数)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_________________________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:
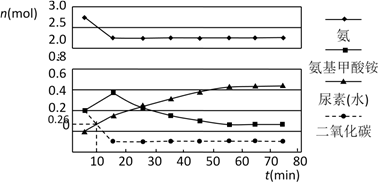
已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________ 步反应决定,总反应进行到_________ min时到达平衡。
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为________________________________ 。
Ⅱ.用焦炭还原NO2的反应为:2NO2(g)+2C(s ) N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
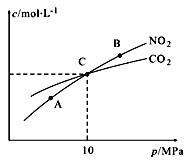
①A、B两点的浓度平衡常数关系:Kc(A)_______ Kc(B) (填 “﹥”、“<”或“﹦”)。
②计算C点时该反应的压强平衡常数Kp(C)=______ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:

已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为
Ⅱ.用焦炭还原NO2的反应为:2NO2(g)+2C(s )
 N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:Kc(A)
②计算C点时该反应的压强平衡常数Kp(C)=
您最近一年使用:0次



