(1)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Al2O3(s)+3C(s)= Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s)= Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)= Al4C3(s)+6CO(g) ΔH3
则ΔH3=____ (用ΔH1、ΔH2表示)。
(2)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值(lnK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。
Ⅰ.Mn3C(s)+4CO2(g) 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g) MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g) 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
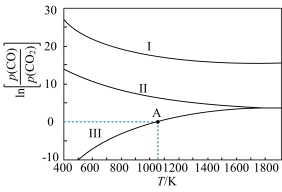
①ΔH>0的反应是____ (填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1 200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=____ 。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____ (填字母)。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.1molCO2,若只发生反应Ⅲ,则在A点反应达到平衡,当容器的总压为a kPa时,CO2的转化率为_______ ;A点对应温度下Kp(Ⅲ)=_______ 。
Al2O3(s)+3C(s)= Al2OC(s)+2CO(g) ΔH1
2Al2OC(s)+3C(s)= Al4C3(s)+2CO(g) ΔH2
2Al2O3(s)+9C(s)= Al4C3(s)+6CO(g) ΔH3
则ΔH3=
(2)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值(lnK=2.303lgK)与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。
Ⅰ.Mn3C(s)+4CO2(g)
 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)Ⅱ.Mn(s)+CO2(g)
 MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)Ⅲ.Mn3C(s)+CO2(g)
 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是
②1 200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.1molCO2,若只发生反应Ⅲ,则在A点反应达到平衡,当容器的总压为a kPa时,CO2的转化率为
更新时间:2020-11-18 20:58:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】“一带路”为中国化工企业开辟了新的国际市场,能源环保是基础。在能源领域科学家提出构想——富集空气中的CO2,并使之与H2反应生成可再生能源甲醇.流程如下:
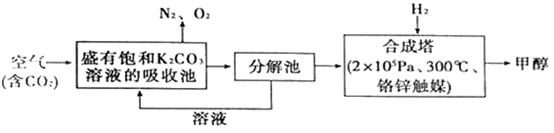
(1)在合成塔中,若有4400gCO2与足量H2完全反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式________________ 。
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2在不同催化剂作用下发生反应I、反应II、反应III,相同时间内CO2的转化率随温度变化如图1所示:
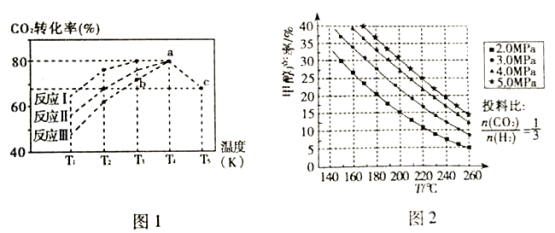
①催化效果最佳的反应是_________ (填“反应I”、“反应II”、“反应III”)。
②b点反应速率v(正)______ v(逆) (填“>”、“=”或“<”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是_________ 。
(3)选取合适的催化剂发生上述反应,测得甲醇的产率与反应温度、压强的关系如图2。
④分析图中数据可知,在220℃、5.0MPa时,CO2的转化率为________ ;将温度降低至140℃、压强减小至2.0MPa,CO2的转化率将_______ (填“增大”、“减小”或“不变”)。
⑤200℃、2.0MPa时,将amol/LCO2和3amol/LH2充入VL密闭容器中,在催化剂作用下反应达到平衡。根据图中数据计算所得甲醇的质量______ g(用含a、V的代数式表示)。
(4)用NaOH溶液吸收CO2所得饱和碳酸钠溶液可以对废旧电池中的铅膏(主要成分PbSO4)进行脱硫反应。已知Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,PbSO4(s)+CO32-(aq)==PbCO3(s)+SO42-(aq),则该反应的平衡常数K=___ (保留三位有效数字);若在其溶液中加入少量Pb(NO3)2晶体,则c(SO42-):c(CO32-)的比值将_____ (填“增大”、“减小”或“不变”)。

(1)在合成塔中,若有4400gCO2与足量H2完全反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2在不同催化剂作用下发生反应I、反应II、反应III,相同时间内CO2的转化率随温度变化如图1所示:

①催化效果最佳的反应是
②b点反应速率v(正)
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是
(3)选取合适的催化剂发生上述反应,测得甲醇的产率与反应温度、压强的关系如图2。
④分析图中数据可知,在220℃、5.0MPa时,CO2的转化率为
⑤200℃、2.0MPa时,将amol/LCO2和3amol/LH2充入VL密闭容器中,在催化剂作用下反应达到平衡。根据图中数据计算所得甲醇的质量
(4)用NaOH溶液吸收CO2所得饱和碳酸钠溶液可以对废旧电池中的铅膏(主要成分PbSO4)进行脱硫反应。已知Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,PbSO4(s)+CO32-(aq)==PbCO3(s)+SO42-(aq),则该反应的平衡常数K=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】目前工业上有一种方法是用CO2生产燃料甲醇(CH3OH)。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
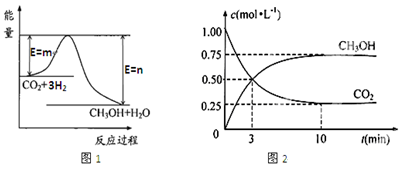
(1)该反应为_________ 热反应,原因是_____________________ 。
(2)下列能说明该反应已经达到平衡状态的是_________ (填序号)
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=________ 。 达平衡时容器内平衡时与起始时的压强比____________ 。
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为________________ ,
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的___________ 倍(保留小数点后1位)。
 CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
(1)该反应为
(2)下列能说明该反应已经达到平衡状态的是
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知反应CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2 kJ·mol-1,该反应是当前大规模获取清洁能源H2
CO2(g)+H2(g) △H=-41.2 kJ·mol-1,该反应是当前大规模获取清洁能源H2 的方法之一,也是为合成氨工业提供生产原料的反应。
的方法之一,也是为合成氨工业提供生产原料的反应。
(1)实际生产中,考虑生产成本,应提高___________ 的转化率。
若同时提高氢气的产率,可采取的下列措施有___________ 。
a.增大CO浓度 b.增大H2O(g)浓度 c.增大压强 d.适当降低温度 e.分离出CO2
(2)若在800℃的恒容密闭容器中,充入1 mol CO和3 mol H2O,达平衡时CO转化率为75%。该反应的平衡常数为___________ 。
(3)一定温度下,向该反应体系投入生石灰可增大H2的体积分数。根据CO2(g)+CaO(s)=CaCO3(s) △H=-178 kJ·mol-1;△S=-169.3 J·mol-1·K-1,用此方法增大H2的体积分数需___________ (填“较高”或“较低”)温度条件。
(4)上述体系制成的H2含有一定量的CO,若用于合成氨,其中的CO会造成催化剂“中毒”。有人从工业提纯粗镍的反应Ni(s)+4CO(g) Ni(CO)4(g) △H<0得到启发,应用金属镍除去H2中的CO,且金属镍可循环使用。查阅资料可知,实际生产中分别在不同条件应用该反应:温度为200℃、50℃;压强为1 MPa、12 MPa。则适宜吸收CO的温度和压强是
Ni(CO)4(g) △H<0得到启发,应用金属镍除去H2中的CO,且金属镍可循环使用。查阅资料可知,实际生产中分别在不同条件应用该反应:温度为200℃、50℃;压强为1 MPa、12 MPa。则适宜吸收CO的温度和压强是___________ ;适宜吸收剂再生的温度和压强是___________ 。
 CO2(g)+H2(g) △H=-41.2 kJ·mol-1,该反应是当前大规模获取清洁能源H2
CO2(g)+H2(g) △H=-41.2 kJ·mol-1,该反应是当前大规模获取清洁能源H2 的方法之一,也是为合成氨工业提供生产原料的反应。
的方法之一,也是为合成氨工业提供生产原料的反应。(1)实际生产中,考虑生产成本,应提高
若同时提高氢气的产率,可采取的下列措施有
a.增大CO浓度 b.增大H2O(g)浓度 c.增大压强 d.适当降低温度 e.分离出CO2
(2)若在800℃的恒容密闭容器中,充入1 mol CO和3 mol H2O,达平衡时CO转化率为75%。该反应的平衡常数为
(3)一定温度下,向该反应体系投入生石灰可增大H2的体积分数。根据CO2(g)+CaO(s)=CaCO3(s) △H=-178 kJ·mol-1;△S=-169.3 J·mol-1·K-1,用此方法增大H2的体积分数需
(4)上述体系制成的H2含有一定量的CO,若用于合成氨,其中的CO会造成催化剂“中毒”。有人从工业提纯粗镍的反应Ni(s)+4CO(g)
 Ni(CO)4(g) △H<0得到启发,应用金属镍除去H2中的CO,且金属镍可循环使用。查阅资料可知,实际生产中分别在不同条件应用该反应:温度为200℃、50℃;压强为1 MPa、12 MPa。则适宜吸收CO的温度和压强是
Ni(CO)4(g) △H<0得到启发,应用金属镍除去H2中的CO,且金属镍可循环使用。查阅资料可知,实际生产中分别在不同条件应用该反应:温度为200℃、50℃;压强为1 MPa、12 MPa。则适宜吸收CO的温度和压强是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮元素的化合物种类繁多,研究氮氧化物的反应机理对于消除污染有重要指导作用。
(1)NO2有较强的氧化性,能将SO2氧化成SO3,自身被还原为NO。
已知:2SO2(g)+O2(g) 2SO3(g) △H1=-196.6 kJ/mol
2SO3(g) △H1=-196.6 kJ/mol
2NO(g)+O2(g) 2NO2(g) △H2=-113.0kJ/mol
2NO2(g) △H2=-113.0kJ/mol
则NO2氧化SO2的热化学方程式为_______ 。
(2)探究压强对2NO2(g) N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图1所示。
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图1所示。
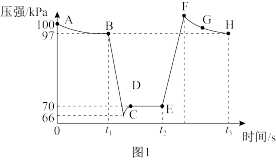
①B、E两点对应的正反应速率大小为vB_______ vE(填“<”或“>”)。
②B、F、H三点对应气体的平均相对分子质量最大的点为_______ (填字母序号)。
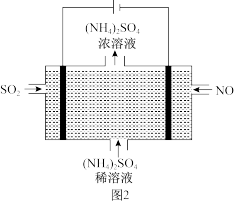
(3)可用图2装置将雾霾中的NO、SO2转化为(NH4)2SO4,则阴极的电极反应式为_______ 。
(4)将CO和NO技不同比例投入一密闭容器中,控制一定温度(T1或T2),发生反应2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0,达到平衡时,混合气体中N2的体积分数随
N2(g)+2CO2(g) △H<0,达到平衡时,混合气体中N2的体积分数随 的变化曲线如图3所示。
的变化曲线如图3所示。
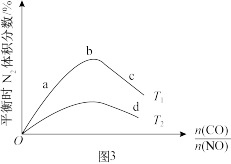
①T1_______ T2(填“>”、“<”或“=”)。
②图3中a、b、c、d中对应NO转化率最大的是_______ 。
③若 =1,T1温度下,平衡时,体系的总压强为a Pa、N2的体积分数为20%,该温度下平衡常数Kp为
=1,T1温度下,平衡时,体系的总压强为a Pa、N2的体积分数为20%,该温度下平衡常数Kp为_______ (用平衡分压代替平衡浓度计算。分压=总压×物质的量分数)。
(1)NO2有较强的氧化性,能将SO2氧化成SO3,自身被还原为NO。
已知:2SO2(g)+O2(g)
 2SO3(g) △H1=-196.6 kJ/mol
2SO3(g) △H1=-196.6 kJ/mol2NO(g)+O2(g)
 2NO2(g) △H2=-113.0kJ/mol
2NO2(g) △H2=-113.0kJ/mol则NO2氧化SO2的热化学方程式为
(2)探究压强对2NO2(g)
 N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图1所示。
N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图1所示。
①B、E两点对应的正反应速率大小为vB
②B、F、H三点对应气体的平均相对分子质量最大的点为
(3)可用图2装置将雾霾中的NO、SO2转化为(NH4)2SO4,则阴极的电极反应式为

(4)将CO和NO技不同比例投入一密闭容器中,控制一定温度(T1或T2),发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0,达到平衡时,混合气体中N2的体积分数随
N2(g)+2CO2(g) △H<0,达到平衡时,混合气体中N2的体积分数随 的变化曲线如图3所示。
的变化曲线如图3所示。
①T1
②图3中a、b、c、d中对应NO转化率最大的是
③若
 =1,T1温度下,平衡时,体系的总压强为a Pa、N2的体积分数为20%,该温度下平衡常数Kp为
=1,T1温度下,平衡时,体系的总压强为a Pa、N2的体积分数为20%,该温度下平衡常数Kp为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氨和甲烷等原料在工业生产中发挥着重要的作用。
Ⅰ.我国科学家以MoS2 为催化剂,通过调节催化剂/电解质的表界面相互作用,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图所示。
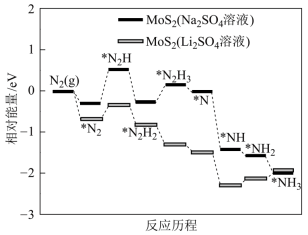
(1)将Na2SO4溶液换成Li2SO4溶液后,反应速率明显加快的主要原因是加快了下列____________ 转化的反应速率(填标号)。
A.N2→*N2 B.*N2→*N2H C.*N2H3→*N D.*NH→*NH2
Ⅱ. 甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(2)已知:CH4(g)+2O2(g)= CO2(g)+ 2H2O(l) ΔH1=akJ·mol—1,
2CO(g)+O2(g)= 2CO2(g) ΔH2=b kJ·mol—1,
2H2(g) +O2(g)=2 H2O (l) ΔH3=c kJ·mol—1
CO(g)+ H2O(g)= CO2(g)+ H2 (g) ΔH4=d kJ·mol—1
则甲烷水蒸气重整反应的ΔH=____________ kJ·mol—1(用字母a、b、c、d表示)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2物质的量分数与水碳比、平衡温度的关系如图所示:
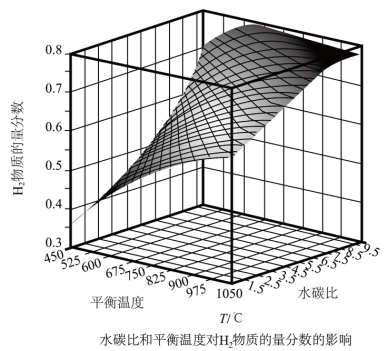
①结合如图回答:当平衡温度一定时,H2的物质的量分数与水碳比(1~10)的关系是________ ,其原因是_____________ 。
②若密闭容器中仅发生CH4(g)+H2O(g) CO(g)+3H2(g),平衡温度为750℃,水碳比为1.0时,H2的物质的量分数0.5,甲烷的转化率为
CO(g)+3H2(g),平衡温度为750℃,水碳比为1.0时,H2的物质的量分数0.5,甲烷的转化率为___________ ,其压强平衡常数Kp为________ ;用气体分压表示反应速率方程为v=k p(CH4)·p—1(H2),则此时反应速率v=_________ 。(已知:气体分压=气体的物质的量分数×总压,速率方程中k 为速率常数)。
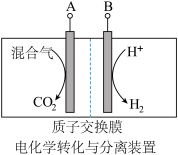
Ⅲ.利用天然气合成氨,并生产尿素的流程如下:

(3)“电化学转化与分离”装置如图,混合气中CO转化成CO2的电极反应式为______ 。
Ⅰ.我国科学家以MoS2 为催化剂,通过调节催化剂/电解质的表界面相互作用,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图所示。

(1)将Na2SO4溶液换成Li2SO4溶液后,反应速率明显加快的主要原因是加快了下列
A.N2→*N2 B.*N2→*N2H C.*N2H3→*N D.*NH→*NH2
Ⅱ. 甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g)
 CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:(2)已知:CH4(g)+2O2(g)= CO2(g)+ 2H2O(l) ΔH1=akJ·mol—1,
2CO(g)+O2(g)= 2CO2(g) ΔH2=b kJ·mol—1,
2H2(g) +O2(g)=2 H2O (l) ΔH3=c kJ·mol—1
CO(g)+ H2O(g)= CO2(g)+ H2 (g) ΔH4=d kJ·mol—1
则甲烷水蒸气重整反应的ΔH=


①结合如图回答:当平衡温度一定时,H2的物质的量分数与水碳比(1~10)的关系是
②若密闭容器中仅发生CH4(g)+H2O(g)
 CO(g)+3H2(g),平衡温度为750℃,水碳比为1.0时,H2的物质的量分数0.5,甲烷的转化率为
CO(g)+3H2(g),平衡温度为750℃,水碳比为1.0时,H2的物质的量分数0.5,甲烷的转化率为Ⅲ.利用天然气合成氨,并生产尿素的流程如下:

(3)“电化学转化与分离”装置如图,混合气中CO转化成CO2的电极反应式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】CO2催化加氢制烯烃(CnH2n)是缓解化石能源消耗、实现减排的重要途径之—。FT转化路径(CO2→CO→CnH2n)涉及的主要反应如下:
i. CO2(g) + H2(g) = CO(g)+H2O(g) ΔH1= 41.1kJ·mol-1
ii. nCO(g)+2nH2(g) = CnH2n (g) + nH2O(g) n=2时,ΔH2= -210.2 kJ·mol-1
iii. CO(g)+3H2(g) = CH4(g)+ H2O(g) ΔH3= -205.9 kJ·mol-1
(1)2CO2(g) + 6H2(g) = C2H4(g) + 4H2O(g) ΔH =_______ kJ·mol-1。_______ (填“高温”或“低温”)有利于该反应自发进行。
(2)有利于提高CO2平衡转化率的措施有_______(填标号)。
(3)n(CO2):n(H2)投料比为1:3、压强为1MPa时,无烷烃产物的平衡体系中CO2转化率和产物选择性随反应温度变化曲线如下图。
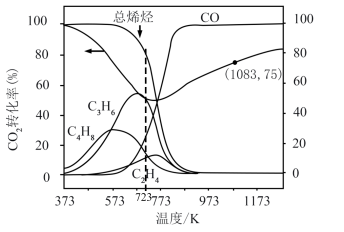
①有利于短链烯烃(n≤4)生成的温度范围为_______ (填标号)。
A.373~573K B.573~773K C.773~973K D.973~1173K
②计算1083K时,反应i的Kp=_______ 。
③373~1273K范围内,723K以前CO2的转化率降低的原因是_______ 。
(4)FT转化路径存在CH4含量过高问题,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如下。

①吸附态用*表示,CO2→甲氧基(H3CO*)过程中,_______ 的生成是决速步骤(填化学式)。
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测,短链烯烃选择性提高的原因_______ 。
i. CO2(g) + H2(g) = CO(g)+H2O(g) ΔH1= 41.1kJ·mol-1
ii. nCO(g)+2nH2(g) = CnH2n (g) + nH2O(g) n=2时,ΔH2= -210.2 kJ·mol-1
iii. CO(g)+3H2(g) = CH4(g)+ H2O(g) ΔH3= -205.9 kJ·mol-1
(1)2CO2(g) + 6H2(g) = C2H4(g) + 4H2O(g) ΔH =
(2)有利于提高CO2平衡转化率的措施有_______(填标号)。
| A.增大n(CO2):n(H2)投料比 | B.增大体系压强 |
| C.使用高效催化剂 | D.及时分离H2O |

①有利于短链烯烃(n≤4)生成的温度范围为
A.373~573K B.573~773K C.773~973K D.973~1173K
②计算1083K时,反应i的Kp=
③373~1273K范围内,723K以前CO2的转化率降低的原因是
(4)FT转化路径存在CH4含量过高问题,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如下。

①吸附态用*表示,CO2→甲氧基(H3CO*)过程中,
②H-SAPO-34具有氧八元环构成的笼状结构(直径0.94nm),笼口为小的八环孔(直径0.38nm)。从结构角度推测,短链烯烃选择性提高的原因
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气在化学工业中应用广泛。回答下列问题:
(1)已知下列热化学方程式:
i.CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)  H1=-164.9 kJ·mol-1
H1=-164.9 kJ·mol-1
ii.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  H2=+41.2 kJ·mol-1
H2=+41.2 kJ·mol-1
(1)已知在某种催化剂的作用下,CH4(g)+H2O(g) CO(g)+3H2(g)的正反应的活化能Ea(正)为312kJ·mol-1,则该反应逆反应的活化能Ea(逆)为
CO(g)+3H2(g)的正反应的活化能Ea(正)为312kJ·mol-1,则该反应逆反应的活化能Ea(逆)为_______ kJ·mol-1。该反应达平衡后采取下列措施,能提高CH4平衡转化率的措施有_______ (填标号)。
A.升高温度 B.增大压强 C.加入CH4 D.移出H2 E.使用催化剂
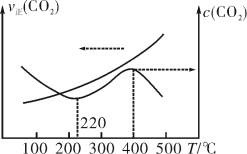
(2)将n(H2)∶n(CO2)=4∶1的混合气体充入反应器中,气体总压强为0.1 MPa,平衡时c(CO2)、v正(CO2)与温度的关系如图所示。220~400 ℃时,CO2的物质的量浓度随温度升高而增大的原因是_______ 。
(3)在一定温度下的恒容密闭容器中通入H2与CO2,使其物质的量浓度均为0.8 mol·L-1,反应足够时间后,容器中CO2和H2O的浓度分别为0.5 mol·L-1和0.4 mol·L-1,则反应ii的平衡常数K=_______ 。
(4)一定条件下,在某恒容密闭容器中,按投料比n(H2)∶n(NO)=1发生如下反应:2H2(g)+2NO(g) N2(g)+2H2O(g),下列能够说明该反应已达到化学平衡状态的是_______(填标号)。
N2(g)+2H2O(g),下列能够说明该反应已达到化学平衡状态的是_______(填标号)。
(1)已知下列热化学方程式:
i.CO2(g)+4H2(g)
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)  H1=-164.9 kJ·mol-1
H1=-164.9 kJ·mol-1ii.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  H2=+41.2 kJ·mol-1
H2=+41.2 kJ·mol-1(1)已知在某种催化剂的作用下,CH4(g)+H2O(g)
 CO(g)+3H2(g)的正反应的活化能Ea(正)为312kJ·mol-1,则该反应逆反应的活化能Ea(逆)为
CO(g)+3H2(g)的正反应的活化能Ea(正)为312kJ·mol-1,则该反应逆反应的活化能Ea(逆)为A.升高温度 B.增大压强 C.加入CH4 D.移出H2 E.使用催化剂
(2)将n(H2)∶n(CO2)=4∶1的混合气体充入反应器中,气体总压强为0.1 MPa,平衡时c(CO2)、v正(CO2)与温度的关系如图所示。220~400 ℃时,CO2的物质的量浓度随温度升高而增大的原因是

(3)在一定温度下的恒容密闭容器中通入H2与CO2,使其物质的量浓度均为0.8 mol·L-1,反应足够时间后,容器中CO2和H2O的浓度分别为0.5 mol·L-1和0.4 mol·L-1,则反应ii的平衡常数K=
(4)一定条件下,在某恒容密闭容器中,按投料比n(H2)∶n(NO)=1发生如下反应:2H2(g)+2NO(g)
 N2(g)+2H2O(g),下列能够说明该反应已达到化学平衡状态的是_______(填标号)。
N2(g)+2H2O(g),下列能够说明该反应已达到化学平衡状态的是_______(填标号)。| A.2v逆(NO)=v正(N2) | B.混合气体的密度不再变化 |
| C.容器内总压强不再变化 | D.混合气体的平均相对分子质量不再变化 |
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】碳中和是指 的排放总量和减少总量相当。我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。
的排放总量和减少总量相当。我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。
I.
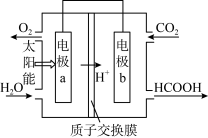
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以 和
和 为原料制备HCOOH和
为原料制备HCOOH和 的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:_______ 。
(2)下列将 转化成有机物的反应中,原子利用率最高的是_______(填序号)
转化成有机物的反应中,原子利用率最高的是_______(填序号)
(3)恒压下将 和
和 按体积比1∶3混合,在不同催化剂作用下发生下列两个反应:
按体积比1∶3混合,在不同催化剂作用下发生下列两个反应:

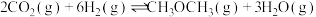
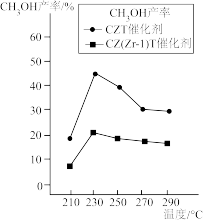
在相同的时间段内 的产率随温度的变化如下图所示。在上述条件下合成甲醇的工业条件是_______(填序号)。
的产率随温度的变化如下图所示。在上述条件下合成甲醇的工业条件是_______(填序号)。
II.在容积为2L的恒温密闭容器中,充入1mol 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 (g)的物质的量随时间的变化情况如下表。
(g)的物质的量随时间的变化情况如下表。
(4)a=_______ ;3~6min内,
_______ 。
(5)达平衡时, 的转化率为
的转化率为_______ ,混合气体中 的物质的量分数为
的物质的量分数为_______ 。
(6)能说明上述反应达到平衡状态的是_______ (填字母)。
a.
b.混合气体的密度不随时间的变化而变化
c.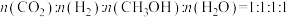
d.混合气体的平均摩尔质量不随时间的变化而变化
(7)第3min时v正( )
)_______ (填“>”、“<”或“=”)第9min时v逆( )
)
 的排放总量和减少总量相当。我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。
的排放总量和减少总量相当。我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。I.
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以
 和
和 为原料制备HCOOH和
为原料制备HCOOH和 的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
(2)下列将
 转化成有机物的反应中,原子利用率最高的是_______(填序号)
转化成有机物的反应中,原子利用率最高的是_______(填序号)A. |
B.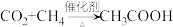 |
C.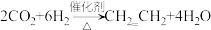 |
D. |
 和
和 按体积比1∶3混合,在不同催化剂作用下发生下列两个反应:
按体积比1∶3混合,在不同催化剂作用下发生下列两个反应:
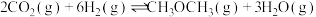
在相同的时间段内
 的产率随温度的变化如下图所示。在上述条件下合成甲醇的工业条件是_______(填序号)。
的产率随温度的变化如下图所示。在上述条件下合成甲醇的工业条件是_______(填序号)。
| A.210℃ | B.230℃ |
| C.CZT催化剂 | D.CZ(Zr-1)T催化剂 |
II.在容积为2L的恒温密闭容器中,充入1mol
 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 (g)的物质的量随时间的变化情况如下表。
(g)的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
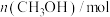 | 0 | 0.50 | 0.65 | 0.75 | 0.75 |
 | 1 | 0.50 | 0.35 | a | 0.25 |

(5)达平衡时,
 的转化率为
的转化率为 的物质的量分数为
的物质的量分数为(6)能说明上述反应达到平衡状态的是
a.

b.混合气体的密度不随时间的变化而变化
c.
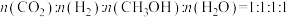
d.混合气体的平均摩尔质量不随时间的变化而变化
(7)第3min时v正(
 )
) )
)
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。则
(1)A为_____ ,B为_____ ,C为_____ ,D的最高价氧化物的水化物是_____ 。 (用化学式填空)
Ⅱ.一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
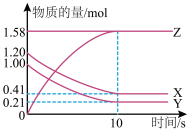
(2)反应开始到10 s,用Z表示的反应速率为_______________ mol/(L∙s)。
(3)反应开始到10 s,X的物质的量浓度减少了____________ mol/L。
(4)反应的化学方程式为:______________________________ 。
(1)A为
Ⅱ.一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

(2)反应开始到10 s,用Z表示的反应速率为
(3)反应开始到10 s,X的物质的量浓度减少了
(4)反应的化学方程式为:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
① 2NO(g)+Cl2(g)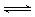 2ClNO(g) ΔH1<0 平衡常数为K1;
2ClNO(g) ΔH1<0 平衡常数为K1;
② 2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;
NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:
2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:_________________ 。ΔH3=__________ (用ΔH1、ΔH2表示)。
(2)①为研究不同条件对反应①的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应①达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=______ mol,NO的转化率α1=______ 。
②其他条件保持不变,反应②升高温度,平衡时NO2的转化率_____ ((填“增大”“减小”或“不变”),平衡常数K2______ (填“增大”“减小”或“不变”)。
① 2NO(g)+Cl2(g)
 2ClNO(g) ΔH1<0 平衡常数为K1;
2ClNO(g) ΔH1<0 平衡常数为K1;② 2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;
NaNO3(s)+ClNO(g) ΔH2<0 平衡常数为K2;(1)4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:
2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常数K的表达式为:(2)①为研究不同条件对反应①的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应①达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=
②其他条件保持不变,反应②升高温度,平衡时NO2的转化率
您最近半年使用:0次
【推荐2】I、从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)已知:Fe3O4(s) + CO(g) = 3FeO(s) + CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) + H2O(g) = Fe3O4(s) + H2(g) ΔH2 = -57.2 kJ·mol-1
C(s) + CO2(g) = 2 CO(g) ΔH3 = +172.4 kJ·mol-1
写出以铁氧化物为催化剂裂解水制氢气总反应的热化学方程式___________ 。
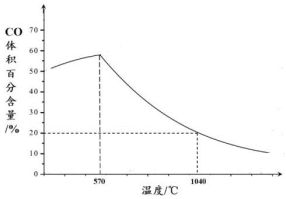
(2)下图表示其它条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度的变化关系。
①当温度低于570℃时,温度降低,CO的转化率__________ (填“增大”、“减小”或“不变”),理由是_______________ 。
②当温度高于570℃时,随温度升高,反应Fe3O4(s) + CO(g) 3FeO(s) + CO2(g)平衡常数的变化趋势是
3FeO(s) + CO2(g)平衡常数的变化趋势是_________ ;(填“增大”、“减小”或“不变”);1040℃时,该反应的化学平衡常数的数值是____________ 。
II、汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。
(1)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图所示(Ce为铈元素)。
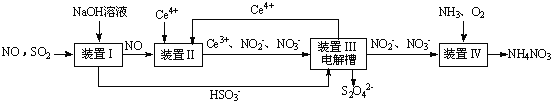
装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成NO3-和NO2-物质的量之比为2:1时的离子方程式:________________________ 。
(2)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的____ (填“阳极”或“阴极”),同时在另一极生成S2O42-的电极反应式为_________ 。
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为a g·L-1,要使1.5 m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气___ L(用含a代数式表示,结果保留整数,否则不给分 )。
(1)已知:Fe3O4(s) + CO(g) = 3FeO(s) + CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) + H2O(g) = Fe3O4(s) + H2(g) ΔH2 = -57.2 kJ·mol-1
C(s) + CO2(g) = 2 CO(g) ΔH3 = +172.4 kJ·mol-1
写出以铁氧化物为催化剂裂解水制氢气总反应的热化学方程式

(2)下图表示其它条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度的变化关系。
①当温度低于570℃时,温度降低,CO的转化率
②当温度高于570℃时,随温度升高,反应Fe3O4(s) + CO(g)
 3FeO(s) + CO2(g)平衡常数的变化趋势是
3FeO(s) + CO2(g)平衡常数的变化趋势是II、汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。
(1)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图所示(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成NO3-和NO2-物质的量之比为2:1时的离子方程式:
(2)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为a g·L-1,要使1.5 m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气
您最近半年使用:0次
【推荐3】工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
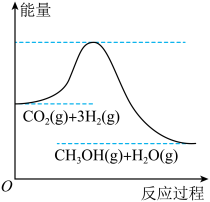
(1)上述反应平衡常数K的表达式为___ ,温度升高,平衡常数K___ (填“增大”“不变”或“减小”)。
(2)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2的物质的量随时间变化如下表所示。则达到平衡时CO2的转化率=________ 。
(3)在相同温度.容积不变的条件下,能说明该反应已达平衡状态的是_____ (填写序号字母)。
a.容器内压强保持不变
b.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
c.容器内的密度保持不变
d.H2的消耗速率与CH3OH的消耗速率之比为3∶1
(4)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________ (填写序号字母)。
a.适当升高温度
b.及时分离出CH3OH气体
c.保选择高效的催化剂
d.持容器的容积不变,再充入1molCO2和3molH2
(5)画出压强为2MPa时甲醇的转化率随温度的变化曲线图__________ 。

 CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
(1)上述反应平衡常数K的表达式为
(2)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2的物质的量随时间变化如下表所示。则达到平衡时CO2的转化率=
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
a.容器内压强保持不变
b.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1
c.容器内的密度保持不变
d.H2的消耗速率与CH3OH的消耗速率之比为3∶1
(4)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是
a.适当升高温度
b.及时分离出CH3OH气体
c.保选择高效的催化剂
d.持容器的容积不变,再充入1molCO2和3molH2
(5)画出压强为2MPa时甲醇的转化率随温度的变化曲线图

您最近半年使用:0次



