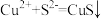室温下,向20mL含有0.10mol/LCr2+和0.10mol/LFe2+的混合溶液中滴加0.10mol/LNaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。若溶液中金属阳离子浓度小于10-5mol/L可视为完全沉淀,则下列说法错误的是( )

已知:Ksp[Cr(OH)2]=2.0×10-16mol3/L3,Ksp[Fe(OH)2]=8.0×10-16mol3/L3

已知:Ksp[Cr(OH)2]=2.0×10-16mol3/L3,Ksp[Fe(OH)2]=8.0×10-16mol3/L3
| A.曲线A表示c(Fe2+)与NaOH溶液体积的关系 |
| B.当V(NaOH溶液)=30mL时,Cr2+开始沉淀 |
| C.当pH=7时,溶液中Fe2+、Cr2+均完全沉淀 |
| D.当V(NaOH溶液)>30mL时,溶液中c(Fe2+):c(Cr2+)=4 |
更新时间:2020-11-21 21:05:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】Al、Fe、Cu都是重要而常见的金属,下列有关说法正确的是
| A.生活中常用的是它们的合金材料 |
| B.三者的单质放置在空气中均只生成氧化物 |
| C.三者所对应的氢氧化物在水中都存在溶解平衡 |
| D.工业上制备这三种金属的方法依次为电解法、热分解法和热还原法 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,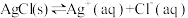 体系中,c(Ag+)和c(Cl-)的关系如图所示,下列说法正确的是
体系中,c(Ag+)和c(Cl-)的关系如图所示,下列说法正确的是
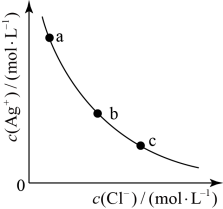
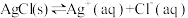 体系中,c(Ag+)和c(Cl-)的关系如图所示,下列说法正确的是
体系中,c(Ag+)和c(Cl-)的关系如图所示,下列说法正确的是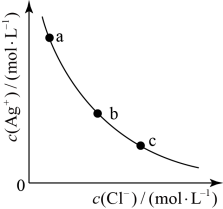
| A.a、b、c三点对应的Ksp:a点>b点>c点 |
| B.AgCl在c点的溶解度比b点的大 |
C.AgCl溶于水形成的饱和溶液中,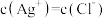 |
D.b点的溶液中加入 固体, 固体,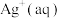 沿曲线向c点方向变化 沿曲线向c点方向变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作、现象和结论均正确的是
| 实验操作 | 实验现象 | 结论 | |
| A | 将Cu与浓硫酸反应后的混合物冷却,再向其中加入蒸馏水 | 溶液变蓝 | 有Cu2+生成 |
| B | 向0.1mol/LH2O2溶液中滴加0.1mol/LKMnO4溶液 | 溶液褪色 | H2O2具有氧化性 |
| C | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加几滴AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向淀粉溶液中加入适量20%的H2SO4溶液,加热,冷却后加入足量NaOH溶液,再滴加少量碘水 | 溶液未变蓝色 | 淀粉已完全水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
| A.升高HCl稀溶液温度,溶液中c(H+)不变 |
| B.常温,向醋酸钠溶液中滴加少量醋酸使其pH=7,则混合液中:c(Na+)=c(CH3COO-) |
| C.向AgCl、AgBr的饱和溶液中加入少量AgNO3固体,溶液中氯离子浓度和溴离子浓度比不变 |
| D.25℃时,将0.1mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述中正确的是
| A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用酸溶解去除 |
| B.常温下,BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物可能是BeCl2 |
| C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动 |
| D.反应2A(g)+B(g)==3C(s)+D(g)能自发进行,说明该反的ΔH>0 |
您最近一年使用:0次
【推荐3】化工生产上有广泛用途的轻质碱式碳酸镁[MgCO3·Mg(OH)2·3H2O]是以卤块(主要成分为MgCl2,含Fe2+、Fe3+等杂质离子)为原料制备的。工艺流程如下:

已知:Fe(OH)2沉淀絮状,不易从溶液中除去。
下列说法正确的是

已知:Fe(OH)2沉淀絮状,不易从溶液中除去。
下列说法正确的是
| A.沉淀的成分是Fe(OH)2和Fe(OH)3的混合物 |
| B.“…”的操作步骤为氧化和调节pH等分离和提纯过程 |
| C.“热解”产生的CO2对生成轻质碱式碳酸镁[MgCO3·Mg(OH)2·3H2O]有重要的作用 |
| D.“料液Ⅱ”呈中性或弱酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:25℃下,H2S溶液的电离平衡常数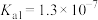 ,
,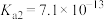 ,MnS、CuS的
,MnS、CuS的 分别为
分别为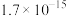 、
、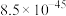 ,
,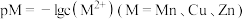 ,
,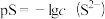 ,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线b表示ZnS。下列说法正确的是
,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线b表示ZnS。下列说法正确的是
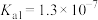 ,
,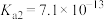 ,MnS、CuS的
,MnS、CuS的 分别为
分别为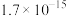 、
、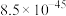 ,
,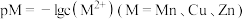 ,
,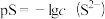 ,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线b表示ZnS。下列说法正确的是
,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线b表示ZnS。下列说法正确的是
| A.曲线c表示 MnS |
B.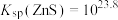 |
C.MnS和CuS的悬浊液中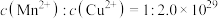 |
D.将浓度均为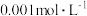 的 的 溶液和H2S溶液等体积混合,无沉淀产生 溶液和H2S溶液等体积混合,无沉淀产生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子在指定的分散系中能够大量共存的是
A.澄清透明的溶液中: 、 、 、 、 、 、 |
B.加入铝片能生成 的溶液: 的溶液: 、 、 、 、 、 、 |
C.0.1mol/L草酸溶液中: 、 、 、 、 、 、 |
D.0.1mol/L NaHS溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
【推荐1】一定温度下,AgCl和 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。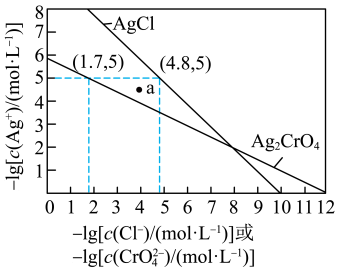
A.a点为 的不饱和溶液 的不饱和溶液 |
B.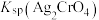 的数量级等于 的数量级等于 |
C.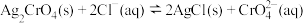 的平衡常数 的平衡常数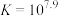 |
D.向NaCl、 均为 均为 的混合溶液中滴加 的混合溶液中滴加 溶液,先产生 溶液,先产生 沉淀 沉淀 |
您最近一年使用:0次
【推荐2】25℃时,向20mL0.01mol/L的RCl2溶液中通入氨气,测得溶液的pH与p(R2+)之间的变化曲线如图所示[已知: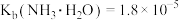 ,
,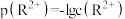 ,忽略反应过程中溶液体积的变化]。下列说法正确的是
,忽略反应过程中溶液体积的变化]。下列说法正确的是

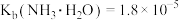 ,
,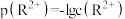 ,忽略反应过程中溶液体积的变化]。下列说法正确的是
,忽略反应过程中溶液体积的变化]。下列说法正确的是 
A.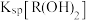 的数量级是 的数量级是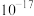 |
B.a点溶液中会产生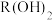 沉淀 沉淀 |
C.b点溶液存在: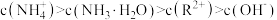 |
D.c点溶液存在: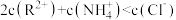 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知t ℃时,AgCl的Ksp=4×10−10,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
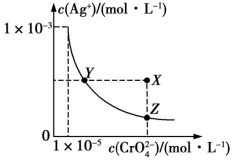

| A.在t ℃时,Ag2CrO4的Ksp为1×10−8 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4,不能使溶液由Y点移动到X点 |
C.t ℃时,反应Ag2CrO4(s)+2Cl−(aq) 2AgCl(s)+ 2AgCl(s)+ 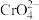 (aq)的平衡常数K=6.25×107 (aq)的平衡常数K=6.25×107 |
| D.t ℃时,以0.001 mol·L−1AgNO3溶液滴定20 mL 0.001 mol·L−1KCl和0.001 mol·L−1 K2CrO4的混合溶液,Cl−先沉淀 |
您最近一年使用:0次

 溶液与
溶液与 溶液混合:
溶液混合: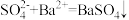
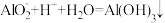
 溶于浓
溶于浓 溶液:
溶液: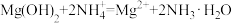
 溶液中加入
溶液中加入 粉末:
粉末: