将2molPCl3和1molCl2充入一容积不变的密闭容器中,在一定条件下反应:PCl3(g)+Cl2(g) PCl5(g)达平衡时,PCl5为0.4mol.那么,在同体积容器中充入1molPCl3和0.5molCl2,在相同温度下,达平衡时PCl5的物质的量是
PCl5(g)达平衡时,PCl5为0.4mol.那么,在同体积容器中充入1molPCl3和0.5molCl2,在相同温度下,达平衡时PCl5的物质的量是
 PCl5(g)达平衡时,PCl5为0.4mol.那么,在同体积容器中充入1molPCl3和0.5molCl2,在相同温度下,达平衡时PCl5的物质的量是
PCl5(g)达平衡时,PCl5为0.4mol.那么,在同体积容器中充入1molPCl3和0.5molCl2,在相同温度下,达平衡时PCl5的物质的量是| A.0.2mol | B.小于0.2mol | C.大于0.2mol而小于0.4mol | D.0.4mol |
更新时间:2020-11-25 09:30:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是( )
A.H2(g)+I2(g) 2HI(g)反应达平衡后,压缩体积气体颜色变深 2HI(g)反应达平衡后,压缩体积气体颜色变深 |
| B.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
C.N2(g)+3H2(g) 2NH3(g)△H<0,工业上采用高压条件更有利于合成氨 2NH3(g)△H<0,工业上采用高压条件更有利于合成氨 |
| D.浸泡在冰水中的NO2球的红棕色明显变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向三个体积分别为 、
、 、
、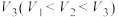 的密闭容器中分别加入足量活性炭和
的密闭容器中分别加入足量活性炭和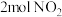 ,发生反应:
,发生反应: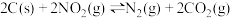 ,在相同时间内测得各容器中
,在相同时间内测得各容器中 的转化率与容器体积的关系如图所示。下列说法正确的是
的转化率与容器体积的关系如图所示。下列说法正确的是

 、
、 、
、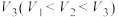 的密闭容器中分别加入足量活性炭和
的密闭容器中分别加入足量活性炭和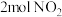 ,发生反应:
,发生反应: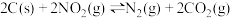 ,在相同时间内测得各容器中
,在相同时间内测得各容器中 的转化率与容器体积的关系如图所示。下列说法正确的是
的转化率与容器体积的关系如图所示。下列说法正确的是
| A.bc曲线上反应均达到平衡状态 |
B.容器内的压强: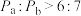 |
| C.a、c两点时气体的颜色相同 |
D.该温度下,a、b、c三点时反应的平衡常数: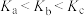 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列化学方程式中,不能正确表达反应颜色变化的是
| A.铜久置空气中表面出现绿色固体:2Cu+O2+CO2+H2O=Cu2(OH)2CO3 |
B.某种火箭发射阶段有少量N2O4逸出,产生红棕色气体:N2O4 2NO2 2NO2 |
| C.向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热:2FeCl3+3H2O=Fe2O3+6HCl |
| D.SO2通入KMnO4溶液中,溶液紫色逐渐褪去:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向一体积不变的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。
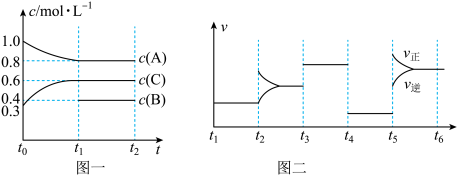
下列说法不正确的是

下列说法不正确的是
A.此温度下该反应的化学方程式为2A(g)+B(s) 3C(g) 3C(g) |
| B.t4-t5阶段改变的条件为减小压强 |
| C.B的起始物质的量为1.0 mol |
| D.在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+2c/3=2.4和b+c/3=1.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,某密闭容器中充入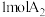 和
和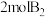 ,发生反应
,发生反应 。在达到平衡后,生成
。在达到平衡后,生成 。当温度不变时,若起始加入的
。当温度不变时,若起始加入的 、
、 、AB的物质的量分别为:x,y,z,则下列说法正确的是
、AB的物质的量分别为:x,y,z,则下列说法正确的是
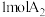 和
和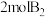 ,发生反应
,发生反应 。在达到平衡后,生成
。在达到平衡后,生成 。当温度不变时,若起始加入的
。当温度不变时,若起始加入的 、
、 、AB的物质的量分别为:x,y,z,则下列说法正确的是
、AB的物质的量分别为:x,y,z,则下列说法正确的是A.若保持恒容,当 , ,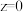 ,则达新平衡状态时 ,则达新平衡状态时 和 和 的转化率一定升高 的转化率一定升高 |
B.若保持恒压,当 ,z为任意值,则达新平衡状态时AB的物质的量为 ,z为任意值,则达新平衡状态时AB的物质的量为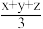 |
C.若保持恒容,当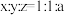 ,则达新平衡状态时 ,则达新平衡状态时 的体积分数与原平衡时相同 的体积分数与原平衡时相同 |
D.若保持恒压,当 , ,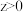 ,则达新平衡状态时 ,则达新平衡状态时 的体积分数与原平衡时可能相同 的体积分数与原平衡时可能相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,向2L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g) C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是( )
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是( )
 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是( )
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是( )| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A.反应在前5s的平均速率v(A)=0.15 mol/(L·s) |
| B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0 |
| C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的分解率大于80% |
| D.相同温度下,起始时向容器中充入0.2 mol A、0.2 mol B和1.0 mol C反应达到平衡前反应速率v(正)<v(逆) |
您最近一年使用:0次
【推荐2】某温度下密闭容器中发生反应2M(g)+N(g) 2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
 2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )| A.20% | B.60% | C.80% | D.90% |
您最近一年使用:0次

 2SO3(g),在相同温度下达到平衡。若甲容器始终保持体积不变,乙容器始终保持压强不变,则达到平衡所需时间 (
2SO3(g),在相同温度下达到平衡。若甲容器始终保持体积不变,乙容器始终保持压强不变,则达到平衡所需时间 (

