在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___ 。
(2)该反应为___ 反应(填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是___ 。
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2)=c(CO)
(4)1200℃时,在某时刻体系中CO2、H2、CO、H2O的浓度分别为2mol·L-1、2mol·L-1、4mol·L-1、4mol·L-1,则此时上述反应的平衡向___ 移动(填“正向”、“逆向”或“不”)。
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变
b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)
d.c(CO2)=c(CO)
(4)1200℃时,在某时刻体系中CO2、H2、CO、H2O的浓度分别为2mol·L-1、2mol·L-1、4mol·L-1、4mol·L-1,则此时上述反应的平衡向
更新时间:2020-12-16 10:19:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】工业上用焦炭与石英在高温下氮气流中发生如下反应,3SiO2(s)+6C(s)+2N2(g)⇌Si3N4(s)+6CO(g) +Q(Q>0),可制得一种新型陶瓷材料氮化硅(Si3N4),该材料熔点高,硬度大 ,广泛应用于光伏、轴承、冶金、化工、能源、环保等行业。回答下列问题:
(1)N2的电子式为____________ ,Si在元素周期表中的位置是_______________ ,氮化硅晶体属于__________ 晶体。
(2)该反应中,还原产物是______________ 。若测得反应生成22.4 L CO气体(标准状况下),则转移的电子的物质的量为_____________ 。
(3)该反应的平衡常数表达式K=__________________ ;若其他条件不变,降低温度,达到新的平衡时,K值____________ (填“增大”、“减小”或“不变”,以下同)。CO的浓度_________ ,SiO2的质量______________ 。
(4)已知在一定条件下的2L密闭容器中制备氮化硅,SiO2(纯度98.5%,所含杂质不与参与反应)剩余质量和反应时间的关系如右图所示。CO在0~10min的平均反应速率为_______ 。

(5)现用四氯化硅、氮气和氢气在高温下发生反应,可得较高纯度的氮化硅。反应的化学方程式为______________ 。
(1)N2的电子式为
(2)该反应中,还原产物是
(3)该反应的平衡常数表达式K=
(4)已知在一定条件下的2L密闭容器中制备氮化硅,SiO2(纯度98.5%,所含杂质不与参与反应)剩余质量和反应时间的关系如右图所示。CO在0~10min的平均反应速率为

(5)现用四氯化硅、氮气和氢气在高温下发生反应,可得较高纯度的氮化硅。反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如图所示,已知达到平衡后,降低温度,A的转化率增大。
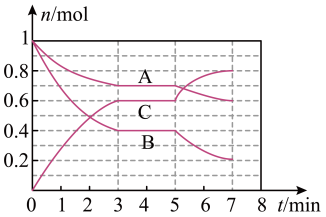
(1)根据图中数据,写出该反应的化学方程式:______ 。此反应的平衡常数的表达式K=_______ ,0~3 min内,A的速率为_______ 。在5~7min内,若K值不变,则此处曲线变化可能的原因是________ 。
(2)图中表示此反应的反应速率v和时间t的关系图:
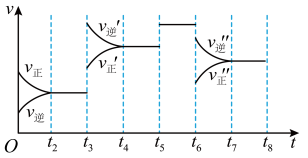
上图中t3时刻改变的条件是______ 。A的转化率最大的一段时间是_______ 。

(1)根据图中数据,写出该反应的化学方程式:
(2)图中表示此反应的反应速率v和时间t的关系图:

上图中t3时刻改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
①反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=________ (用ΔH1和ΔH2表示),K=________ (用K1和K2表示)。
②能判断CO2(g)+H2(g) CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是____ (填字母)。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。

①该条件下反应的平衡常数为________ ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为________ mol·L-1。
②下列措施中能使平衡时 增大的是
增大的是________ (填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
 FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:| 700 ℃ | 900 ℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
 CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=
CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=②能判断CO2(g)+H2(g)
 CO(g)+H2O(g)达到化学平衡状态的依据是
CO(g)+H2O(g)达到化学平衡状态的依据是A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
①该条件下反应的平衡常数为
②下列措施中能使平衡时
 增大的是
增大的是A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:
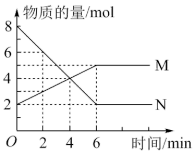
(1)反应的化学方程式为___________ 。
(2)反应达到平衡状态的时间是_______ min,该时间内的平均反应速率v(N)=_______ 。
(3)判断该反应达到平衡状态的依据是___________(填序号)。
(4)能加快反应速率的措施是___________(填序号)。

(1)反应的化学方程式为
(2)反应达到平衡状态的时间是
(3)判断该反应达到平衡状态的依据是___________(填序号)。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
| D.条件下,单位时间内消耗2molN的同时,生成1molM |
| A.升高温度 |
| B.容器容积不变,充入惰性气体Ar |
| C.容器压强不变,充入惰性气体He |
| D.使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
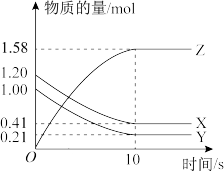
【推荐2】I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。___________ 。
(2)该反应的化学方程式为___________ 。
II.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的颜色;⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(3)一定能证明 达到平衡状态的是
达到平衡状态的是___________ (填序号,下同)。
(4)一定能证明 达到平衡状态的是
达到平衡状态的是___________ 。
(2)该反应的化学方程式为
II.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的颜色;⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(3)一定能证明
 达到平衡状态的是
达到平衡状态的是(4)一定能证明
 达到平衡状态的是
达到平衡状态的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列化学平衡相关问题:
(1)工业制硫酸的核心反应是:2SO2(g)+O2(g) 2SO3(g) ∆H<0
2SO3(g) ∆H<0
①在1L密闭容器中充入1mol SO2和2mol O2,在1min内达到平衡,测得v(SO3)=0.8mol/(L∙min)。该条件下,反应的平衡常数K=_______ 。
②下列措施中有利于提高SO2转化率的是_______  填字母
填字母 。
。
A.加入催化剂 B.通入O2 C.移出SO3 D.通入SO2
(2)将水蒸气通过红热的碳即可产生水煤气,C(s)+H2O(g) CO(g)+H2(g) ∆H=+131.3kJ∙mol-1,∆S=+133.7J∙(K∙mol)-1
CO(g)+H2(g) ∆H=+131.3kJ∙mol-1,∆S=+133.7J∙(K∙mol)-1
①该反应在_______ 能自发(填“高温”、“低温”、“任何温度”、“一定不”)。
②一定温度下,在一个恒容密闭容器中发生上述反应,下列不能判断该反应达到化学平衡状态的是_______ (填字母)。
A.1molH-H键断裂的同时生成2molH-O键
B.v正(CO)=v逆(H2O)
C.容器中的压强不再变化
D.混合气体的密度不再变化
E.c(CO)=c(H2)
(3)汽车尾气含NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g),已知该反应在2404℃时,平衡常数K=6.4×10-3,该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
2NO(g),已知该反应在2404℃时,平衡常数K=6.4×10-3,该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应_______ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”)。
(1)工业制硫酸的核心反应是:2SO2(g)+O2(g)
 2SO3(g) ∆H<0
2SO3(g) ∆H<0①在1L密闭容器中充入1mol SO2和2mol O2,在1min内达到平衡,测得v(SO3)=0.8mol/(L∙min)。该条件下,反应的平衡常数K=
②下列措施中有利于提高SO2转化率的是
 填字母
填字母 。
。A.加入催化剂 B.通入O2 C.移出SO3 D.通入SO2
(2)将水蒸气通过红热的碳即可产生水煤气,C(s)+H2O(g)
 CO(g)+H2(g) ∆H=+131.3kJ∙mol-1,∆S=+133.7J∙(K∙mol)-1
CO(g)+H2(g) ∆H=+131.3kJ∙mol-1,∆S=+133.7J∙(K∙mol)-1①该反应在
②一定温度下,在一个恒容密闭容器中发生上述反应,下列不能判断该反应达到化学平衡状态的是
A.1molH-H键断裂的同时生成2molH-O键
B.v正(CO)=v逆(H2O)
C.容器中的压强不再变化
D.混合气体的密度不再变化
E.c(CO)=c(H2)
(3)汽车尾气含NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)
 2NO(g),已知该反应在2404℃时,平衡常数K=6.4×10-3,该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
2NO(g),已知该反应在2404℃时,平衡常数K=6.4×10-3,该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据所学知识回答下列问题:
I.用纯净的锌粒与稀盐酸反应制取氢气,请回答:

(1)实验过程如图所示,化学反应速率最快的是_______
A.OE段 B.EF段 C.FG段
(2)请解释图中曲线变化的原因:_______ 。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质少许,可行的是_______。
II.在温度为373K时,将0.100mol N2O4气体通入1L的恒容密闭容器中,发生反应N2O4(g) 2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。

(4)计算在20至40秒时间内,NO2的平均生成速率为_______ 。
(5)该反应的化学平衡常数表达式为_______ 。
(6)下表是不同温度下测定得到的该反应的化学平衡常数。
据此可推测该反应(生成NO2)是_______ 反应(选填“吸热”或“放热”)。
(7)反应达平衡后再加入0.100mol的N2O4气体,推测反应重新达到平衡后N2O4的转化率_______ (选填“增大”、“不变”或“减小”)
I.用纯净的锌粒与稀盐酸反应制取氢气,请回答:

(1)实验过程如图所示,化学反应速率最快的是
A.OE段 B.EF段 C.FG段
(2)请解释图中曲线变化的原因:
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质少许,可行的是_______。
| A.NaCl溶液 | B.硫酸铜溶液 | C.浓盐酸 | D.CH3COONa固体 |
II.在温度为373K时,将0.100mol N2O4气体通入1L的恒容密闭容器中,发生反应N2O4(g)
 2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
2NO2(g)。下图是测定到的N2O4的浓度变化曲线图。
(4)计算在20至40秒时间内,NO2的平均生成速率为
(5)该反应的化学平衡常数表达式为
(6)下表是不同温度下测定得到的该反应的化学平衡常数。
| T/K | 323 | 373 |
| K值 | 0.022 | 0.36 |
(7)反应达平衡后再加入0.100mol的N2O4气体,推测反应重新达到平衡后N2O4的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=_________ ,ΔH______ 0(填“>”、“<”或“=”);
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平衡反应速率v(CO2)=_________ 、CO的平衡转化率=___________ 。
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式K=
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平衡反应速率v(CO2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮是地球上含量丰富的一种元素,合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重要影响。铵盐在工农业生产、生活中有着重大作用。
 完成下列填空
完成下列填空
(1).在固定体积的密闭容器中,进行如下放热反应:N2(g)+3H2(g) 2NH3(g),其平衡常数K与温度T的关系如下表。
则该反应的平衡常数K1________ K2 (填“>”、“<”或“=”)。
(2).能说明该反应已达到平衡状态的是________ (填序号)。
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。
请回答下列问题:
(3).相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+)________ (填“等于”“大于”或“小于”)0.1 mol·L-1NH4HSO4中的c(NH4+)。
(4).如图所示是0.1 mol·L-1电解质溶液的pH随温度变化的图象。
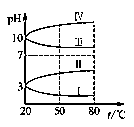
①其中符合0.1 mol·L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是________ (填写序号),导致pH随温度变化的原因是_______________________________ ;
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=__________ 。
(5).室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。

试分析图中a、b、c、d四个点,水的电离程度最大是________ 点;在b点,溶液中各离子浓度由大到小的排列顺序是______________ 。
 完成下列填空
完成下列填空(1).在固定体积的密闭容器中,进行如下放热反应:N2(g)+3H2(g) 2NH3(g),其平衡常数K与温度T的关系如下表。
| T/K | 298 | 398 | 498 | …… |
| 平衡常数K | 4.1×106 | K1 | K2 | …… |
则该反应的平衡常数K1
(2).能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。
请回答下列问题:
(3).相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+)
(4).如图所示是0.1 mol·L-1电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol·L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②20℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(5).室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示。

试分析图中a、b、c、d四个点,水的电离程度最大是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知2A2(g)+B2(g) 2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量bkJ。
2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量bkJ。
(1)a________ b(填“>”“=”或“<”)。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将________ (填“增大”“减小”或“不变”)。
(3)能说明该反应已经达到平衡状态的是________ 。
a.v(C)=2v(B2) b.容器内压强保持不变
c.v逆(A2)=2v正(B2) d.容器内的密度保持不变
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________ 。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
(5)密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g) H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为________ 。
 2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量bkJ。
2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量bkJ。(1)a
(2)若将反应温度升高到700 ℃,该反应的平衡常数将
(3)能说明该反应已经达到平衡状态的是
a.v(C)=2v(B2) b.容器内压强保持不变
c.v逆(A2)=2v正(B2) d.容器内的密度保持不变
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
(5)密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)
 H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知反应H2(g)+I2(g) 2HI(g)。在698K时各物质的初始浓度和平衡浓度的数据如表所示。
2HI(g)。在698K时各物质的初始浓度和平衡浓度的数据如表所示。
(1)请计算填写表中的空格。
(2)分析上述数据,回答下列问题。
①在一定温度下,反应H2(g)+I2(g) 2HI(g),
2HI(g),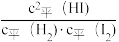 的数值与H2(g)、I2(g)、HI(g)的初始浓度大小有关吗
的数值与H2(g)、I2(g)、HI(g)的初始浓度大小有关吗____ ?
②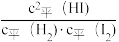 的数值与平衡从正向建立,还是从逆向建立有关吗
的数值与平衡从正向建立,还是从逆向建立有关吗____ ?
 2HI(g)。在698K时各物质的初始浓度和平衡浓度的数据如表所示。
2HI(g)。在698K时各物质的初始浓度和平衡浓度的数据如表所示。(1)请计算填写表中的空格。
| 初始浓度/(mol·L-1) | 平衡浓度/(mol·L-1) | 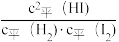 | ||||
| c始(H2) | c始(I2) | c始(HI) | c平(H2) | c平(I2) | c平(HI) | |
| 0.01067 | 0.01196 | 0 | 0.00183 | 0.00313 | 0.01767 | |
| 0.01135 | 0.00904 | 0 | 0.00356 | 0.00125 | 0.01559 | |
| 0.01134 | 0.00751 | 0 | 0.00457 | 0.00074 | 0.01354 | |
| 0 | 0 | 0.00449 | 0.00048 | 0.00048 | 0.00353 | |
| 0 | 0 | 0.01069 | 0.00114 | 0.00114 | 0.00841 | |
(2)分析上述数据,回答下列问题。
①在一定温度下,反应H2(g)+I2(g)
 2HI(g),
2HI(g),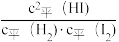 的数值与H2(g)、I2(g)、HI(g)的初始浓度大小有关吗
的数值与H2(g)、I2(g)、HI(g)的初始浓度大小有关吗②
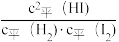 的数值与平衡从正向建立,还是从逆向建立有关吗
的数值与平衡从正向建立,还是从逆向建立有关吗
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知反应A(g)+B(g) C(g)+D(g)的平衡常数与温度的关系如表所示:
C(g)+D(g)的平衡常数与温度的关系如表所示:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=
(2)800℃时,某时刻测得c(A)=2.5mol•L-1,c(B)=2mol•L-1,c(C)=4mol•L-1,c(D)=1mol•L-1,此时反应向
(3)830℃时,向一个密闭容器中充入浓度为0.04mol•L-1的A和0.04mol•L-1的B,若反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1,则6s时c(A)=
(4)一定温度下,在一密闭容器中进行该反应,判断该反应达到平衡的依据为
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.相同时间内生成C、D的物质的量相等
(5)1200℃时,反应C(g)+D(g)
 A(g)+B(g)的平衡常数为
A(g)+B(g)的平衡常数为
您最近一年使用:0次



