运用化学反应原理知识研究SO2与O2的反应对工业生产硫酸有重要意义。
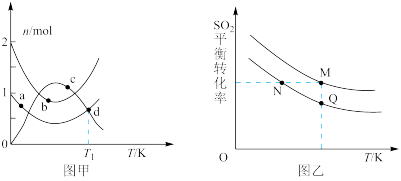
(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应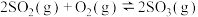 一定条件下能自发进行的原因是
一定条件下能自发进行的原因是___________ 。
②图中a、b、c三点中处于平衡状态的是___________ 点。
③T1温度时反应的平衡常数为___________ 。
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)___________ 2p(Q)
②M、N两点的平衡常数K (M)___________ K(N)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是___________ 。

(1)向体积均为2L的恒容密闭容器中,分别加入2 mol SO2与1 mol O2,反应相同时间,不同温度下各容器中SO2、O2、SO3的物质的量如图甲所示。
①反应
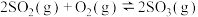 一定条件下能自发进行的原因是
一定条件下能自发进行的原因是②图中a、b、c三点中处于平衡状态的是
③T1温度时反应的平衡常数为
(2)若在两个体积相等的容器内起始分别加入2 mol SO2和1 mol O2、1 mol SO2和0.5 mol O2,SO2的平衡转化率随温度的变化如图乙所示。
①M、Q两点容器内压强p(M)
②M、N两点的平衡常数K (M)
③M、N、Q三点的正反应速率v(M)正、v(N)正、v(Q)正由大到小的顺序是
更新时间:2020-12-10 10:35:22
|
相似题推荐
填空题
|
适中
(0.65)
真题
解题方法
【推荐1】接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:2SO2(g)+O2(g) 2SO3(g) 放出+190KJ的热量,
2SO3(g) 放出+190KJ的热量,
(1)该反应所用的催化剂是___ (填写化合物名称),该反应450℃时的平衡常数_____ 500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是____________ .
(3)下列描述中能说明上述反应已达到平衡状态的是__________
a.v(O2)正=2v(SO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20 mol 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2) =
,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2) =______ mol⋅L−1⋅min−1若继续通入0.20mol 和0.10mol
和0.10mol ,则平衡
,则平衡______ 移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,______ mol<n(SO3)<______ mol。
 2SO3(g) 放出+190KJ的热量,
2SO3(g) 放出+190KJ的热量,(1)该反应所用的催化剂是
(2)该热化学反应方程式的意义是
(3)下列描述中能说明上述反应已达到平衡状态的是
a.v(O2)正=2v(SO3)逆 b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20 mol
 和0.10mol
和0.10mol ,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2) =
,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2) = 和0.10mol
和0.10mol ,则平衡
,则平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】 和
和 是工业排放的对环境产生影响的废气,充分利用(例如合成尿素)既可以降低成本,也可以减少对环境的污染。
是工业排放的对环境产生影响的废气,充分利用(例如合成尿素)既可以降低成本,也可以减少对环境的污染。
(1)以 与
与 为原料合成化肥尿素的主要反应如下:
为原料合成化肥尿素的主要反应如下:
①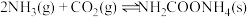 ;
;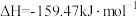
②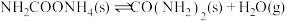 ;
;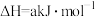
③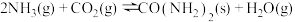 ;
;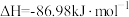 。
。
则a为_______
(2)写出反应②的平衡常数的表达式K=_______ 。
(3)下列说法正确的是_______
(4)在一个初始体积为VL的恒温恒压的容器中,起始充入14mol 和13mol
和13mol ,发生反应③,经过20min后,氨气的转化率达到50%,则用尿素来表示这个反应在20min内的平均反应速率为
,发生反应③,经过20min后,氨气的转化率达到50%,则用尿素来表示这个反应在20min内的平均反应速率为_______ mol/min。并将0-30min内体系内气体的密度随时间的变化趋势画在下图中。________

 和
和 是工业排放的对环境产生影响的废气,充分利用(例如合成尿素)既可以降低成本,也可以减少对环境的污染。
是工业排放的对环境产生影响的废气,充分利用(例如合成尿素)既可以降低成本,也可以减少对环境的污染。(1)以
 与
与 为原料合成化肥尿素的主要反应如下:
为原料合成化肥尿素的主要反应如下:①
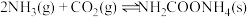 ;
;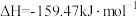
②
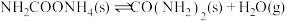 ;
;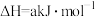
③
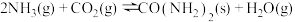 ;
;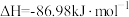 。
。则a为
(2)写出反应②的平衡常数的表达式K=
(3)下列说法正确的是_______
| A.某恒温恒容的容器中仅发生反应①,若混合气体平均相对分子质量保持不变,说明反应达到了平衡 |
B.某恒温恒压的容器中仅发生反应②,达到平衡后,充入少量He,继续反应足够时间,则 会被完全反应 会被完全反应 |
C.对于反应③,反应开始后的一段时间内,适当升温可提高单位时间内 的转化率 的转化率 |
D.对于反应③,在容器中加入CaO,(可与 反应),提高 反应),提高 产率 产率 |
 和13mol
和13mol ,发生反应③,经过20min后,氨气的转化率达到50%,则用尿素来表示这个反应在20min内的平均反应速率为
,发生反应③,经过20min后,氨气的转化率达到50%,则用尿素来表示这个反应在20min内的平均反应速率为
您最近一年使用:0次
【推荐1】SO2具有抗氧化、保鲜、防腐、脱色等功用,合理利用二氧化硫可服务于人们更好的生活。但空气中过量的二氧化硫会形成酸雨、易引起呼吸道疾病等问题,因此,二氧化硫的污染治理是化学研究的重要课题。
(1)硝化法既能生产硫酸,也能处理二氧化硫,主要反应为:NO2(g)+SO2(g) SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
①t℃时,该反应的化学平衡常数为___ 。
②t℃时,向某容器中同时充入NO2、SO2、SO3、NO各1mol,v正___ v逆(填“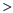 ”、“
”、“ ”或“
”或“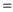 ”)
”)
(2)某实验室尝试变废为宝,模仿工业制硫酸工艺利用SO2,方程式为2SO2(g)+O2(g) 2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
①通过分析第1组和第2组实验数据,比较两组实验中SO2的化学反应速率,可得到影响该反应速率因素的相关结论为___ 。
②在第3组的实验中一开始加入了0.5mol的SO3,反应达平衡时c仍为0.4mol,则a=___ ,b=__ 。
(1)硝化法既能生产硫酸,也能处理二氧化硫,主要反应为:NO2(g)+SO2(g)
 SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。
SO3(g)+NO(g)△H<0。t℃时,向恒容密闭容器中加入等物质的量的NO2和SO2,达到平衡时NO和NO2的浓度之比为3:1。①t℃时,该反应的化学平衡常数为
②t℃时,向某容器中同时充入NO2、SO2、SO3、NO各1mol,v正
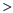 ”、“
”、“ ”或“
”或“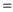 ”)
”)(2)某实验室尝试变废为宝,模仿工业制硫酸工艺利用SO2,方程式为2SO2(g)+O2(g)
 2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:
2SO3(g),在一容积固定为10L的密闭容器中进行该反应,测得如下数据:| 实验组 | 温度(℃) | 起始量/mol | 平衡量/mol | 达到平衡所需时间/h | |
| SO2 | O2 | SO2 | |||
| 1 | 250 | 4 | 2 | 0.4 | 48 |
| 2 | 260 | 2 | 1 | 0.4 | 16 |
| 3 | 260 | a | b | c | t |
①通过分析第1组和第2组实验数据,比较两组实验中SO2的化学反应速率,可得到影响该反应速率因素的相关结论为
②在第3组的实验中一开始加入了0.5mol的SO3,反应达平衡时c仍为0.4mol,则a=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,有1
 气体和3
气体和3
 气体发生下列反应:
气体发生下列反应:
 。
。
(1)若在相同温度下,分别在1L定压密闭容器A中和1L定容密闭容器B中反应:哪个容器中的反应先达到平衡?答:_______ 。哪个容器中的N2的转化率高?答:_______ 。
(2)若在上述定压密闭容器A中,反应已达到平衡时,再加入0.5摩氩气,则 的转化率会起什么变化?答:
的转化率会起什么变化?答:_______ 。正反应速度与原平衡相比,有无变化_______ ,简答理由。_______ 。
(3)若在1L定容容器中,上述反应达到平衡时,平衡混和物中 、
、 、
、 的物质的量分别为A、B、C摩尔。仍维持原温度,用x、y、z分别表示开始时
的物质的量分别为A、B、C摩尔。仍维持原温度,用x、y、z分别表示开始时 、
、 、
、 的加入的物质的量(
的加入的物质的量( ),使达到平衡后
),使达到平衡后 、
、 、
、 的物质的量也为A、B、C摩尔。则应满足的条件是:
的物质的量也为A、B、C摩尔。则应满足的条件是:
①若 ,
, ,则
,则
_______ 。
②若 ,则y应为
,则y应为_______  、z应为
、z应为_______  。
。

 气体和3
气体和3
 气体发生下列反应:
气体发生下列反应:
 。
。(1)若在相同温度下,分别在1L定压密闭容器A中和1L定容密闭容器B中反应:哪个容器中的反应先达到平衡?答:
(2)若在上述定压密闭容器A中,反应已达到平衡时,再加入0.5摩氩气,则
 的转化率会起什么变化?答:
的转化率会起什么变化?答:(3)若在1L定容容器中,上述反应达到平衡时,平衡混和物中
 、
、 、
、 的物质的量分别为A、B、C摩尔。仍维持原温度,用x、y、z分别表示开始时
的物质的量分别为A、B、C摩尔。仍维持原温度,用x、y、z分别表示开始时 、
、 、
、 的加入的物质的量(
的加入的物质的量( ),使达到平衡后
),使达到平衡后 、
、 、
、 的物质的量也为A、B、C摩尔。则应满足的条件是:
的物质的量也为A、B、C摩尔。则应满足的条件是:①若
 ,
, ,则
,则
②若
 ,则y应为
,则y应为 、z应为
、z应为 。
。
您最近一年使用:0次
【推荐3】一定条件下,CO2和CO可以互相转化
(1)某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
甲容器15min后达到平衡,此时CO2的转化率为75%,则0-15min内平均反应速率 (H2)=
(H2)=______ ,此条件下该反应的平衡常数K=______ 。欲使平衡后乙与甲中相同组分气体的体积分数相等,则w、x、y、z需满足的关系是________________ ,且________________ (用含y的等式表示)。
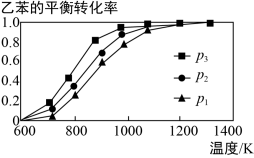
(2)研究表明,温度、压强对反应C6H5CH2CH3(g)+CO2(g) C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH
C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH ______ 0(填“>”“< ” 或“=”),压强p1、p2、p3从大到小的顺序是________________ 。
(3)CO可被NO2氧化CO+NO2 CO2+NO。当温度高于225℃时,反应速率
CO2+NO。当温度高于225℃时,反应速率 正=k正·c(CO) ·c(NO2)、
正=k正·c(CO) ·c(NO2)、 逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为______ 。
(1)某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g)
 CO(g)+H2O(g)。
CO(g)+H2O(g)。| 容器 | 反应物 |
| 甲 | 8molCO2(g)、16molH2(g) |
| 乙 | wmolCO2(g)、xmolH2(g)、ymolCO(g)、zmolH2O(g) |
甲容器15min后达到平衡,此时CO2的转化率为75%,则0-15min内平均反应速率
 (H2)=
(H2)=
(2)研究表明,温度、压强对反应C6H5CH2CH3(g)+CO2(g)
 C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH
C6H5CH=CH2(g)+CO(g)+H2O(g) ΔH中乙苯的平衡转化率影响如下图所示:则ΔH (3)CO可被NO2氧化CO+NO2
 CO2+NO。当温度高于225℃时,反应速率
CO2+NO。当温度高于225℃时,反应速率 正=k正·c(CO) ·c(NO2)、
正=k正·c(CO) ·c(NO2)、 逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
逆= k逆·c(CO2) ·c(NO),k正、k逆分别为正、逆反应速率常数。在上述温度范围内,k正、k逆与该反应的平衡常数K之间的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知合成氨 ,在298K即25℃下,K值为
,在298K即25℃下,K值为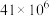 ,
, ,该生产设备可承受压强为20MPa,铁触媒催化剂的活性温度为400~500℃。请按要求回答下列问题。
,该生产设备可承受压强为20MPa,铁触媒催化剂的活性温度为400~500℃。请按要求回答下列问题。
(1)请结合数据分析在298K下可利用合成氨反应进行工业固氮的理由。
①从反应限度视角分析:_______ 。
②从反应自发视角分析:_______ 。
(2)依据合成氨反应速率方程即 (k为常数,随温度的升高而增大),可得知提高该化学反应速率的措施有增大原料气的浓度、
(k为常数,随温度的升高而增大),可得知提高该化学反应速率的措施有增大原料气的浓度、_______ 、_______ 。
(3)合成氨反应的历程和能量变化如下图所示,符号“。”可视为催化剂。
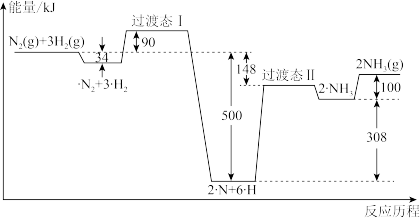
对合成氨总反应速率影响最大的基元反应的活化能为_______  ,该步反应的化学方程式为
,该步反应的化学方程式为_______ 。
(4)下图表示在恒压密闭容器中,不同温度下,达到平衡时 的体积百分数与投料比[
的体积百分数与投料比[ ]的关系。
]的关系。
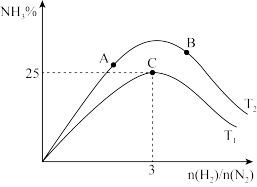
①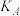 、
、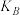 、
、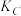 的大小关系为:
的大小关系为:_______ 。
②C点 的平衡转化率为
的平衡转化率为_______ 。
 ,在298K即25℃下,K值为
,在298K即25℃下,K值为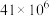 ,
, ,该生产设备可承受压强为20MPa,铁触媒催化剂的活性温度为400~500℃。请按要求回答下列问题。
,该生产设备可承受压强为20MPa,铁触媒催化剂的活性温度为400~500℃。请按要求回答下列问题。(1)请结合数据分析在298K下可利用合成氨反应进行工业固氮的理由。
①从反应限度视角分析:
②从反应自发视角分析:
(2)依据合成氨反应速率方程即
 (k为常数,随温度的升高而增大),可得知提高该化学反应速率的措施有增大原料气的浓度、
(k为常数,随温度的升高而增大),可得知提高该化学反应速率的措施有增大原料气的浓度、(3)合成氨反应的历程和能量变化如下图所示,符号“。”可视为催化剂。

对合成氨总反应速率影响最大的基元反应的活化能为
 ,该步反应的化学方程式为
,该步反应的化学方程式为(4)下图表示在恒压密闭容器中,不同温度下,达到平衡时
 的体积百分数与投料比[
的体积百分数与投料比[ ]的关系。
]的关系。
①
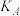 、
、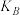 、
、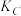 的大小关系为:
的大小关系为:②C点
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1mol NH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=_______ mol·L-1·min-1(用含t1的代数式表示);
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________
(3)在该温度下,反应的标准平衡常数Kθ=____ 。[已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)⇌gG(g)+hH(g) Kθ= ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
(2)t2时将容器容积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
(3)在该温度下,反应的标准平衡常数Kθ=
 ,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
,其中pθ=100kPa,pG、pH、pD、pE为各组分的平衡分压]。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】尿素(H2NCONH2)是一种非常重要的高氮化肥,氨基甲酸铵(NH2COONH4)是尿素合成过程的中间体,某研究小组在实验室进行氨基甲酸铵分解反应平衡常数和分解反应速率的测定。
(1)工业上合成尿素的反应:2NH3(g)+CO2(g) H2O(1)+H2NCONH4(1) ΔH=-103.7kJ·mol-1
H2O(1)+H2NCONH4(1) ΔH=-103.7kJ·mol-1
①上述可逆反应的逆反应为_______ (填“放热”或“吸热”)反应
②下列措施中有利于提高尿素产率的是_______ (填字母)。
A.采用高压 B.采用高温 C.寻找更高效的催化剂
(2)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g) ΔH。
2NH3(g)+CO2(g) ΔH。
实验测得不同温度下的平衡数据列于下表:
①ΔH_______ (填“>”或“<”)
②根据表中数据,计算25.0℃时氨基甲酸铵分解反应的平衡常数K=_______ (mol·L-1)3。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下分解应达到平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量_______ (填“增加“减少”或“不变”)。
(1)工业上合成尿素的反应:2NH3(g)+CO2(g)
 H2O(1)+H2NCONH4(1) ΔH=-103.7kJ·mol-1
H2O(1)+H2NCONH4(1) ΔH=-103.7kJ·mol-1①上述可逆反应的逆反应为
②下列措施中有利于提高尿素产率的是
A.采用高压 B.采用高温 C.寻找更高效的催化剂
(2)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)
 2NH3(g)+CO2(g) ΔH。
2NH3(g)+CO2(g) ΔH。实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/(mol/L) | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
②根据表中数据,计算25.0℃时氨基甲酸铵分解反应的平衡常数K=
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下分解应达到平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量
您最近一年使用:0次



