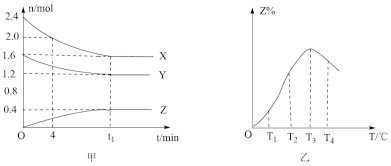
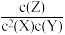下列图示与对应的叙述相符的是


A.图一表示反应:mA(s)+nB(g)  pC(g) △H>O,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢 pC(g) △H>O,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢 |
B.图二是可逆反应:A(g)+B(s)  C(s)+D(g) △H>O的速率时间图象,在t1时刻改变条件一定是加入催化剂 C(s)+D(g) △H>O的速率时间图象,在t1时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应mA(g)+nB(g)  pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0 pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0 |
| D.图四所示图中的阴影部分面积的含义是(v正-v逆) |
更新时间:2021-01-09 11:17:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列操作能实现相应目的的是
| A.将FeCl3溶液加热蒸干制备无水FeCl3 |
| B.用干燥的pH试纸测定NaClO溶液的pH |
| C.用饱和氯化铵溶液作焊接金属时的除锈剂 |
| D.SO2的催化氧化反应,升高温度能提高SO2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】甲醇通过催化氧化制取甲醛时,在无催化剂(图中实线)和加入特定催化剂(图中虚线)时均会产生甲醛,其反应中相关物质的相对能量如图所示。下列说法错误的是
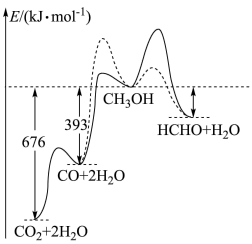

| A.无催化剂时,温度升高,生成甲醛的正反应速率增大的程度比逆反应速率增大程度大 |
B.无催化剂时,生成 比生成甲醛的活化能小 比生成甲醛的活化能小 |
C.该条件下 比 比 的稳定性强 的稳定性强 |
| D.加入该催化剂不能改变反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡: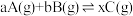 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
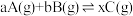 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指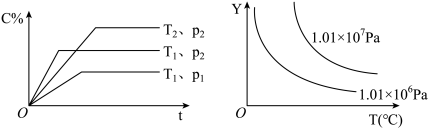
| A.反应物A的百分含量 | B.平衡混合气的总物质的量 | C.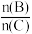 比值 比值 | D.反应物B的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】液氨是一种很好的溶剂,液氨可以微弱的电离产生 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是
 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是A.该反应的 H>0 H>0  S<0 S<0 |
B.该反应的平衡常数表达式为  |
C.升高温度, 该反应的  (正)增大, (正)增大,  (逆)减小 (逆)减小 |
| D.将容器体积压缩为原来一半,气体颜色比压缩前深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、现象、结论均正确的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向平衡体系FeCl3+3KSCN Fe(SCN)3+3KCl中加入适量KCl固体 Fe(SCN)3+3KCl中加入适量KCl固体 | 溶液的颜色变浅 | 平衡逆向移动 |
| B | 对平衡体系2NO2(g) N2O4(g)压缩体积,增大压强 N2O4(g)压缩体积,增大压强 | 混合气体的颜色变深 | 平衡逆向移动 |
| C | 2mL0.1mol•L-1K2Cr2O7溶液中存在:Cr2O +H2O +H2O 2CrO 2CrO +2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 +2H+,向其中滴加5~10滴6mol•L-1NaOH溶液 | 溶液由橙色变为黄色 | 平衡正向移动 |
| D | CuCl2溶液中存在:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O △H>0,对CuCl2溶液加热 [CuCl4]2-(黄色)+4H2O △H>0,对CuCl2溶液加热 | 溶液由蓝色变为黄色 | 平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知反应A2(?)+2B2(g)  2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
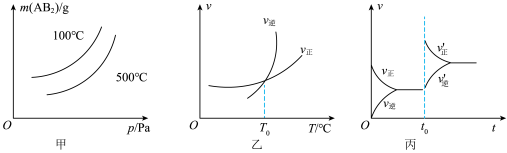
 2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
| A.由图甲可知,A2为气体 |
| B.由图甲可知,ΔH<0 |
| C.由图乙可知,T=T0℃时,该可逆反应达到平衡状态 |
| D.由图丙可知,t=t0时,改变的条件可能是增加了B2的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在某密闭容器中,可逆反应:A(g)+B(g) xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )
xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )

 xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )
xC(g)符合图像(Ⅰ)所示关系。由此推断,对图像(Ⅱ)的不正确的说法是( )
| A.p3>p4,y轴表示A的转化率 |
| B.p3>p4,y轴表示B的质量分数 |
| C.p3>p4,y轴表示C的质量分数 |
| D.p3>p4,y轴表示混合气体的平均相对分子质量 |
您最近一年使用:0次