将2.00 mol X和1.00 mol Y充入体积不变的密闭容器中,在一定条件下发生反应:X(g)+Y(g)⇌Z(g),达到平衡时X为1.50 mol,如果此时移走1.00 mol X和0.50 mol Y,保持温度和体积不变,再次达到平衡时,X的物质的量可能为
| A.0.75 mol | B.0.55 mol | C.0.80 mol | D.1.00 mol |
更新时间:2021-02-04 09:02:16
|
相似题推荐
单选题
|
困难
(0.15)
名校
解题方法
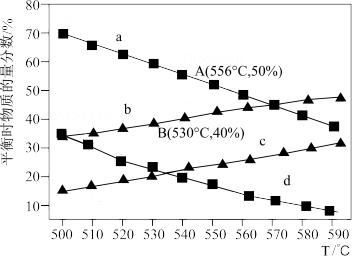
【推荐1】利用丙烷(C3H8)在无氧条件下制备丙烯(C3H6)的反应方程式为:C3H8(g) C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
 C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
| A.c曲线表示的是0.01MPa压强下丙烯随温度变化的物质的量分数 |
| B.A点对应的该反应平衡常数Kp=1.25MPa(Kp为以分压表示的平衡常数) |
| C.B点丙烷的平衡转化率为33.3% |
| D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,增大丙烯的平衡产率 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
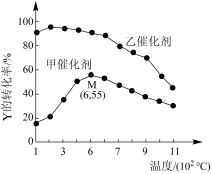
【推荐2】为研究反应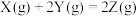 ,向一固定体积的容器中加入足量1molX和2molY发生反应。一定条件下,在甲、乙两种催化剂作用下,反应相同时间,测得Y的转化率与温度的关系如下图所示。下列说法错误的是
,向一固定体积的容器中加入足量1molX和2molY发生反应。一定条件下,在甲、乙两种催化剂作用下,反应相同时间,测得Y的转化率与温度的关系如下图所示。下列说法错误的是
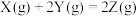 ,向一固定体积的容器中加入足量1molX和2molY发生反应。一定条件下,在甲、乙两种催化剂作用下,反应相同时间,测得Y的转化率与温度的关系如下图所示。下列说法错误的是
,向一固定体积的容器中加入足量1molX和2molY发生反应。一定条件下,在甲、乙两种催化剂作用下,反应相同时间,测得Y的转化率与温度的关系如下图所示。下列说法错误的是
| A.反应达到平衡后,恒温时,再加入少量Z,达到新平衡时Y的体积分数减小 |
| B.在相同温度下,与催化剂甲相比,乙使反应活化能更低 |
| C.M点可能是该反应的平衡点 |
| D.反应达到平衡后,恒温时,再加入少量Y,Z的体积分数减小 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】在容积可变的密闭容器中充入2mol A和1mol B发生反应:mA(g) + nB(g)  pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是

 pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
pC(g)。在一定温度下达到平衡时,分别得到A的物质的量浓度如下表,以下说法正确的是
| A.维持压强2×105Pa,若反应开始后5min时达到平衡,则v(A)=0.016mol/(L·min) |
| B.P从2×105Pa增加到5×105Pa时,平衡逆向移动 |
C.P为1×106Pa时,平衡常数表达式K=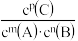 |
D.其它条件相同时,在上述三个压强下分别发生该反应。A的转化率随时间变化曲线如图所示 |
您最近半年使用:0次
【推荐1】一定温度下,在3个体积均为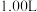 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应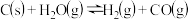
 ,相关数据如下表(已知:炭粉足量)。
,相关数据如下表(已知:炭粉足量)。
下列说法错误的是
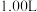 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应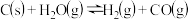
 ,相关数据如下表(已知:炭粉足量)。
,相关数据如下表(已知:炭粉足量)。| 容器 | T/℃ | 物质的起始浓度/( ) ) | 物质的平衡浓度
| ||
 |  | 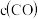 | |||
| Ⅰ |  | 1.00 | 0 | 0 | 0.85 |
| Ⅱ |  | 0 | 1.00 | 1.00 | x |
| Ⅲ |  | 2.00 | 0 | 0 | 1.60 |
A. | B.达到平衡所需时间: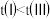 |
C.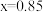 | D. ℃,该反应的化学平衡常数 ℃,该反应的化学平衡常数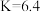 |
您最近半年使用:0次
单选题
|
困难
(0.15)
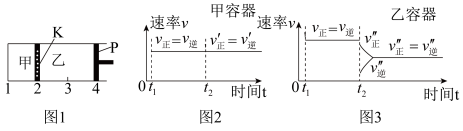
【推荐2】一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】在温度、容积相同的3个密闭容器中,按不同方式投入反应,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g)
2NH3(g) 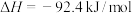 )
)
下列说法正确的是
 2NH3(g)
2NH3(g) 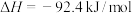 )
)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| 的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | p1 | p2 | p3 |
| 反应物转化率 |  |  |  |
A. | B.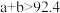 | C.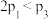 | D.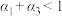 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) 2SO3(g)△H = -196.0 kJ.mol-1,测得反应的相关数据如下,下列说法正确的是( )
2SO3(g)△H = -196.0 kJ.mol-1,测得反应的相关数据如下,下列说法正确的是( )
 2SO3(g)△H = -196.0 kJ.mol-1,测得反应的相关数据如下,下列说法正确的是( )
2SO3(g)△H = -196.0 kJ.mol-1,测得反应的相关数据如下,下列说法正确的是( )容器1 | 容器2 | 容器3 | |
| 应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、1mol O2 | 4mol SO3 | 2 mol SO3 |
| 平衡v正(SO2)/mol•L-1•S-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol•L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 反应能量变化 | 放出a KJ | 吸收b KJ | 吸收c KJ |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A. v1< v2,c2<2c1 | B. K1> K3,p2>2p3 |
| C.v1< v3,α1(SO2 ) <α2(SO2 ) | D. c2>2c3,α2(SO3 )+α3(SO2 )<1 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐2】在相同温度下,在三个大小完全一样的容器中发生反应(保持容器体积不变):3H2(g)+N2(g) 2NH3(g)△H=-92kJ/mol。开始时投料情况是:A中3molH2(g)和1molN2(g);B中2molNH3(g);C中4molNH3(g),都达到平衡后,下列说法正确的是
2NH3(g)△H=-92kJ/mol。开始时投料情况是:A中3molH2(g)和1molN2(g);B中2molNH3(g);C中4molNH3(g),都达到平衡后,下列说法正确的是
 2NH3(g)△H=-92kJ/mol。开始时投料情况是:A中3molH2(g)和1molN2(g);B中2molNH3(g);C中4molNH3(g),都达到平衡后,下列说法正确的是
2NH3(g)△H=-92kJ/mol。开始时投料情况是:A中3molH2(g)和1molN2(g);B中2molNH3(g);C中4molNH3(g),都达到平衡后,下列说法正确的是| A.三个容器中的转化率的关系是:α(A)+α(B)>α(A)+α(C) |
| B.A容器放出的热量为92kJ,B容器中吸收热量为92kJ |
| C.达到平衡后三容器中氨气的体积分数相等 |
| D.A容器中氨气的平衡浓度是C容器中氨气的平衡浓度的一半 |
您最近半年使用:0次
【推荐3】在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如表,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是

 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是| 容器 | n(CO2)/mol | n(C)/mol | n(CO)/mol |
| 甲 | 0.1 | 0.3 | 0 |
| 乙 | 0 | 0 | 0.4 |

| A.曲线Ⅰ对应的是甲容器 |
| B.a、b两点所处状态的压强大小关系:9pa>14pb |
C.c点:CO的体积分数>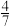 |
| D.900K时,若起始向容器乙中加入CO、CO2、C各1mol,则v(正)>v(逆) |
您最近半年使用:0次



