21. (1)煤的气化的主要反应为C(s)+H
2O(g)
⇌CO(g)+H
2(g)
△H>0。若在一个密闭容器中投入过量的碳和一定比例的H
2O(g)、H
2,一定条件下发生上述反应,测得反应过程中气体的平均相对分子质量不变,则气体的平均相对分子质量是
______,H
2O(g)和H
2的体积之比是
______。
(2)煤的气化还发生反应C(s)+2H
2O(g)
⇌CO
2(g)+2H
2(g)
△H>0,当该反应处于化学平衡状态时,若既要提高反应速率又要提高H
2O的平衡转化率,下列措施中可行的是
______(填字母)。
a.增大体系压强
b.使用合适的催化剂
c.升高温度
d.增大H
2O(g)的浓度
e.加入适量的C(s)
f.分离出CO
2(3)一定温度下,煤的气化还可以发生反应C(s)+CO
2(g)
⇌2CO(g)
△H>0。在某密闭容器中加入适量碳和CO
2气体发生该反应,测得在气体压强缓慢增大的过程中,CO的消耗速率与总压的关系如图所示。
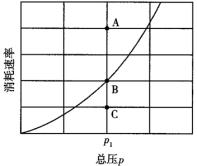
已知在此条件下,CO
2、CO的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(CO
2)=k
1·p(CO
2)、v(CO)=k
2·p
2(CO)。图中在总压为p
1时可逆反应达到平衡状态,则表示CO
2的消耗速率的点是
______(填“A”“B”或“C”);k
1、k
2与该反应的平衡常数K
p(用平衡分压代替平衡浓度计算的平衡常数)间的关系是K
p=
______。