氢氟酸是芯片加工的重要试剂,常见制备反应为: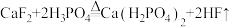 。已知
。已知 溶液显酸性,下列有关说法不正确的是
溶液显酸性,下列有关说法不正确的是
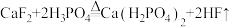 。已知
。已知 溶液显酸性,下列有关说法不正确的是
溶液显酸性,下列有关说法不正确的是A. 溶液中微粒浓度大小顺序: 溶液中微粒浓度大小顺序: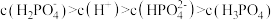 |
B. 的空间构型为正四面体形 的空间构型为正四面体形 |
| C.已知CaF2晶胞中每个Ca2+被8个F-包围,则F-的配位数是4 |
| D.芯片加工时用氢氟酸除去硅表面的氧化物,是利用了氢氟酸的强酸性 |
2021·湖北·模拟预测 查看更多[2]
更新时间:2021-03-26 08:53:59
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关物质的用途与化学原理具有对应关系的是
| 选项 | 用途 | 化学原理 |
| A | 用氢氟酸雕刻玻璃 | 氢氟酸显弱酸性 |
| B | 用FeCl3溶液蚀刻印刷电路板 | FeCl3溶液显酸性 |
| C | 用SiO2制造坩埚 | SiO2熔点高 |
| D | 用HNO3制备硝酸铵 | HNO3具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列“类比”合理的是
| 已知事实 | 类比得出 | |
| A | 浓盐酸与过量 反应会有盐酸剩余 反应会有盐酸剩余 | 浓硫酸与过量铜反应也会有硫酸剩余 |
| B |  与 与 溶液不反应 溶液不反应 |  与 与 溶液也不反应 溶液也不反应 |
| C | 氢氟酸是弱酸,可以溶解 | 高氯酸是强酸,也可以溶解 |
| D |  可以用浓硫酸干燥 可以用浓硫酸干燥 |  也可用浓硫酸干燥 也可用浓硫酸干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某温度时,将n mol•L﹣1氨水滴入20 mL1.0 mol•L﹣1盐酸中,忽略溶液混合时的体积变化,溶液pH和温度随加入氨水体积变化的曲线如图所示。下列有关说法正确的是( )


| A.a点:Kw=1.0×10﹣14 |
B.b点:c(NH )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
| C.25℃NH4Cl水解常数为(n﹣1)×10-6 |
| D.b点水的电离程度最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】电解质溶液有许多奇妙之处,下列关于电解质溶液的叙述中正确的是
| A.常温下c(OH-)=1×10-2的 氢氧化钠溶液和c(H+)=1×10-2 醋酸溶液等体积混合后,所得混合液中:c(CH3COO-)=c (Na+) |
| B.c(NH4+)浓度相等的下列溶液①NH4Cl②NH4HSO4③(NH4)2SO4④(NH4)2CO3⑤(NH4)2Fe(SO4)2它们的物质的量浓度由大到小的顺序为①>②>④>③>⑤ |
| C.常温下,某溶液中由水电离出的c(H+)=10-5mol/L,则此溶液可能是盐酸 |
| D.等物质的量浓度的Na2CO3、NaHCO3的混合溶液中c(CO32-)>c(HCO3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】电解质溶液有许多奇妙之处,只有深入思考,才能体会到它的乐趣。常温时,关于下列溶液的叙述正确的是
A.0.1mol·L-1NaHSO3溶液pH<7,则溶液中c(H2SO3)>c(SO ) ) |
B.浓度相同的①NH4Cl、②CH3COONH4、③NH4HSO4三种溶液中的c(NH ):①>③>② ):①>③>② |
C.将相同物质的量浓度的氨水与盐酸等体积混合,所得溶液中的离子浓度关系:c(Cl-)>c(NH )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| D.将amol·L-1CH3COOH溶液与bmol·L-1NaOH溶液等体积混合,测得溶液pH为7,则a与b的关系:a<b |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体 形成的
形成的 分子是非极性分子,与其他卤素形成的卤素互化物(如
分子是非极性分子,与其他卤素形成的卤素互化物(如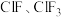 )具有与
)具有与 相似的化学性质,与氮形成的
相似的化学性质,与氮形成的 可与
可与 反应生成
反应生成 (结构式:
(结构式: )。自然界中,含氯矿石有萤石
)。自然界中,含氯矿石有萤石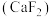 、冰晶石
、冰晶石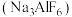 等,萤石可与浓硫酸共热制取
等,萤石可与浓硫酸共热制取 气体。工业上,可通过电解
气体。工业上,可通过电解 的无水
的无水 溶液(含
溶液(含 和
和 离子)制取
离子)制取 。下列有关说法正确的
。下列有关说法正确的
 形成的
形成的 分子是非极性分子,与其他卤素形成的卤素互化物(如
分子是非极性分子,与其他卤素形成的卤素互化物(如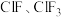 )具有与
)具有与 相似的化学性质,与氮形成的
相似的化学性质,与氮形成的 可与
可与 反应生成
反应生成 (结构式:
(结构式: )。自然界中,含氯矿石有萤石
)。自然界中,含氯矿石有萤石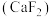 、冰晶石
、冰晶石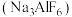 等,萤石可与浓硫酸共热制取
等,萤石可与浓硫酸共热制取 气体。工业上,可通过电解
气体。工业上,可通过电解 的无水
的无水 溶液(含
溶液(含 和
和 离子)制取
离子)制取 。下列有关说法正确的
。下列有关说法正确的A. 的空间结构为Ⅴ形 的空间结构为Ⅴ形 | B. 与 与 互为同素异形体 互为同素异形体 |
C.键角: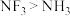 | D. 存在顺反异构现象 存在顺反异构现象 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将少量硫酸铜溶液滴入氨基乙酸钠溶液(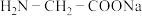 )中即可得到结构如图所示的产物。下列叙述错误的是
)中即可得到结构如图所示的产物。下列叙述错误的是
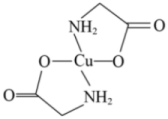
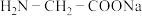 )中即可得到结构如图所示的产物。下列叙述错误的是
)中即可得到结构如图所示的产物。下列叙述错误的是
A.氨基乙酸钠中的氮原子采取 杂化 杂化 |
B.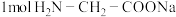 中含有 中含有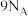 个 个 键 键 |
C.产物中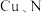 原子VSEPR模型均为四面体形结构 原子VSEPR模型均为四面体形结构 |
| D.该反应产物为配合物,只有内界而无外界 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.金刚石中碳原子杂化类型为sp2 |
| B.12g石墨中含有2NA个六元环 |
| C.SiO2晶体中最小环为6元环 |
| D.CaF2晶体是离子晶体,阴阳离子配位数之比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A.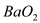 (过氧化钡)固体中的阴离子和阳离子之比为2∶1 (过氧化钡)固体中的阴离子和阳离子之比为2∶1 |
| B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C.HCl的相对分子质量大于HF,所以HCl的沸点高于HF |
| D.由ⅠA族和ⅥA族元素可形成原子个数比为1∶1、电子总数为38的化合物 |
您最近一年使用:0次

 是
是 、
、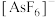 与
与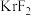 分子形成的加合物,其晶胞如图所示。下列说法正确的是
分子形成的加合物,其晶胞如图所示。下列说法正确的是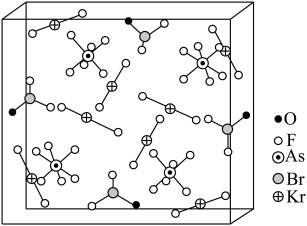
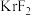 和
和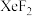 属于同构型的分子晶体,且
属于同构型的分子晶体,且

 周围紧邻的
周围紧邻的 数目是8个
数目是8个 晶体中一个
晶体中一个

