25℃时,下列说法不正确 的是
A.稀释醋酸溶液,溶液中的 和 和 数目都增大 数目都增大 |
B.在醋酸溶液中加入 至溶液为中性,此时 至溶液为中性,此时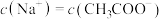 |
C.pH相等的 和 和 溶液,水的电离程度相同 溶液,水的电离程度相同 |
D.已知 溶液显中性。常温下等浓度的 溶液显中性。常温下等浓度的 和 和 ,若前者的 ,若前者的 ,后者的 ,后者的 ,则 ,则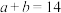 |
更新时间:2021-05-02 14:58:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列操作中,能使电离平衡H2O H++OH-,向右移动且溶液呈酸性的是
H++OH-,向右移动且溶液呈酸性的是
 H++OH-,向右移动且溶液呈酸性的是
H++OH-,向右移动且溶液呈酸性的是 | A.向水中加入NaHSO4溶液 |
| B.向水中加入Al2(SO4)3固体 |
| C.向水中加入Na2CO3溶液 |
| D.将水加热到100℃,使pH=6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.SO2溶于水,其水溶液能导电,说明SO2是电解质 |
| B.向纯水中加入盐酸或氢氧化钠都能使水的电离平衡逆向移动,水的离子积减小 |
| C.铅蓄电池在放电过程中,负极质量增加,正极质量减少 |
| D.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)==4Fe(OH)3(s)的△H<0、△S<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,向 氨水中逐滴加入
氨水中逐滴加入 的
的 溶液,溶液的导电能力和
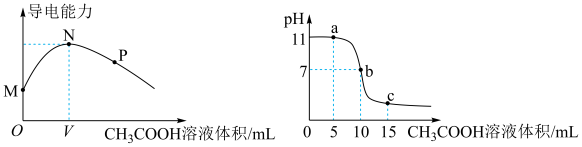
溶液,溶液的导电能力和 变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
 氨水中逐滴加入
氨水中逐滴加入 的
的 溶液,溶液的导电能力和
溶液,溶液的导电能力和 变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
A.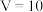 |
B.常温下,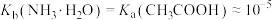 |
C. 点溶液中存在关系: 点溶液中存在关系: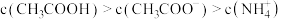 |
D. 点溶液中存在关系: 点溶液中存在关系: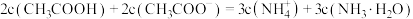 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向100 mL 0.01 mol·L-1Ba(OH)2溶液中滴加0.1 mol·L-1NaHCO3溶液,测得溶液的电导率变化如图。下列说法正确的是
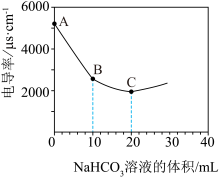

A.NaHCO3在水中的电离方程式为 |
B.A→B的过程中,溶液中 的浓度在逐渐增大 的浓度在逐渐增大 |
C.B→C的过程中,发生反应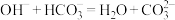 |
| D.B、C两点的阴离子浓度相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,向100 mL0.2 mol· L-1 Na2CO3溶液中逐滴滴入0. 1 mol· L-1的盐酸(已知:H2CO3的电离常数Ka1=5×10-7、Ka2=5 × 10-11,不考虑溶液混合时温度和体积的变化,lg5=0.7)。下列说法错误的是
A.当滴入盐酸的体积为50 mL时,溶液中一定存在c(Na+ )+c(H+ )=2c( )+c( )+c( )+c(OH- )+c(Cl- ) )+c(OH- )+c(Cl- ) |
B.当滴入盐酸的体积为150 mL时,溶液中一定存在7c(Na+ )>8c( )+8c( )+8c( )+8c(H2CO3) )+8c(H2CO3) |
C.当c( )=c(H2CO3)时,溶液的pH=8.3 )=c(H2CO3)时,溶液的pH=8.3 |
D.当滴入的盐酸体积为200 mL时,溶液中一定存在c(Na+ )<c(Cl-)+c( )+c( )+c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温常压下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1NaOH溶液,整个过程溶液中pH的变化如图所示,下列有关叙述正确的是


A.②处溶液中存在平衡常数K= [c(Cl2)为Cl2在水溶液中的平衡浓度] [c(Cl2)为Cl2在水溶液中的平衡浓度] |
| B.曲线②至③段,n(HClO)+n(ClO-)始终逐渐增大 |
| C.曲线②至④段,③处表示溶液中水的电离程度最大 |
| D.④处表示Cl2与NaOH溶液恰好完全反应,共转移了0.1mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法正确的是
A.室温下,向NH4HSO4溶液中加入NaOH溶液至中性,则c( )>c(Na+)>c( )>c(Na+)>c( ) ) |
| B.体积相等pH=12的氨水和NaOH溶液中和盐酸的能力相同 |
| C.向10ml 0.01mol/L AgNO3溶液中依次滴入2~3滴0.01mol/L NaCl溶液、0.01mol/L NaI溶液,所得沉淀由白色变成黄色,则可推知Ksp(AgI)<Ksp(AgCl) |
| D.物质的量浓度之比为1:2的CH3COOH和CH3COONa的混合溶液中: 2[c(CH3COOH)+c(CH3COO-)]=3c(Na+) |
您最近一年使用:0次



