在 密闭容器中,800℃时,反应
密闭容器中,800℃时,反应 体系中,
体系中,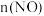 随时间的变化如表所示.
随时间的变化如表所示.
(1)图中,A点处
_______  (填“大于”小于”或“等于”)。
(填“大于”小于”或“等于”)。
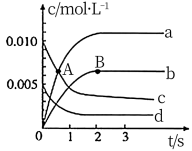
(2)图中表示 变化的曲线是
变化的曲线是_______ 。用 表示从
表示从 内该反应的平均速率
内该反应的平均速率
_______ 。
(3)下列能使该反应的反应速率增大的是_______ 。
a.及时分离出 气体 b.适当升高温度
气体 b.适当升高温度
c.适当扩大容器的容积 d.选择高效的催化剂
 密闭容器中,800℃时,反应
密闭容器中,800℃时,反应 体系中,
体系中,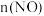 随时间的变化如表所示.
随时间的变化如表所示.| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)图中,A点处

 (填“大于”小于”或“等于”)。
(填“大于”小于”或“等于”)。
(2)图中表示
 变化的曲线是
变化的曲线是 表示从
表示从 内该反应的平均速率
内该反应的平均速率
(3)下列能使该反应的反应速率增大的是
a.及时分离出
 气体 b.适当升高温度
气体 b.适当升高温度c.适当扩大容器的容积 d.选择高效的催化剂
更新时间:2021-05-06 14:57:47
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某可逆反应从0—2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示。

(1)则该反应的的反应物_____ ,生成物是_______ ,化学方程式为_______ ;
(2)能否计算反应开始至2分钟时,用C表示的反应速率?若能,其反应速率为多少,若不能,则其原因为_______ ;
(3)2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了_______ 状态。

(1)则该反应的的反应物
(2)能否计算反应开始至2分钟时,用C表示的反应速率?若能,其反应速率为多少,若不能,则其原因为
(3)2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2019年国际非政府组织“全球碳计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋缓。CO2的综合利用是解决温室问题的有效途径。
(1)一种途径是将CO2转化成有机物实现碳循环。如:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH1=-44.2kJ·mol-1
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH2=+1411.0kJ·mol-1
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) ΔH3=___ 。
(2)CO2甲烷化反应是由法国化学家Sabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如图:
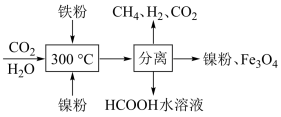
上述过程中,产生H2反应的化学方程式为__ 。
②HCOOH是CO2转化为CH4的中间体:CO2 HCOOH
HCOOH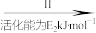 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是__ (填“I”或“Ⅱ”)。
(3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g) CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
反应Ⅱ:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
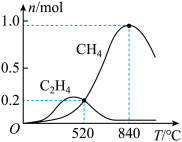
在1L恒容密闭容器中充入1molCO2和4molH2,测得平衡时有关物质的物质的量随温度变化如图所示。520℃时,CO2的转化率为__ ,520℃时,反应I的平衡常数K=__ 。
(4)已知CO2催化加氢合成乙醇的反应原理为2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ΔH。m代表起始时的投料比,即m=
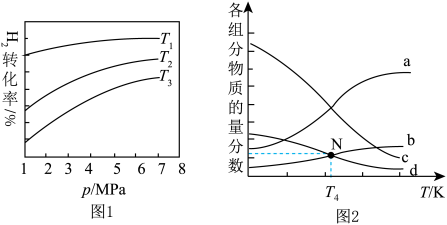
C2H5OH(g)+3H2O(g) ΔH。m代表起始时的投料比,即m=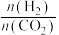 。图1中投料比相同,温度T3>T2>T1,则ΔH
。图1中投料比相同,温度T3>T2>T1,则ΔH___ (填“>”或“<”)0。
②m=3时,该反应达到平衡状态后p(总)=20Mpa,恒压条件下各物质的物质的量分数与温度的关系如图2。则曲线b代表的物质为___ (填化学式),T4温度时,反应达到平衡时物质d的分压p(d)=___ 。
(1)一种途径是将CO2转化成有机物实现碳循环。如:
C2H4(g)+H2O(l)=C2H5OH(l) ΔH1=-44.2kJ·mol-1
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) ΔH2=+1411.0kJ·mol-1
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) ΔH3=
(2)CO2甲烷化反应是由法国化学家Sabatier提出的,因此,该反应又叫Sabatier反应。CO2催化氢化制甲烷的研究过程如图:

上述过程中,产生H2反应的化学方程式为
②HCOOH是CO2转化为CH4的中间体:CO2
 HCOOH
HCOOH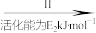 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,当增加镍粉用量时,CO2镍催化氢化制甲烷的两步反应中反应速率增加较大的一步是(3)CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)反应Ⅱ:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g) 
在1L恒容密闭容器中充入1molCO2和4molH2,测得平衡时有关物质的物质的量随温度变化如图所示。520℃时,CO2的转化率为
(4)已知CO2催化加氢合成乙醇的反应原理为2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) ΔH。m代表起始时的投料比,即m=
C2H5OH(g)+3H2O(g) ΔH。m代表起始时的投料比,即m=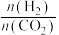 。图1中投料比相同,温度T3>T2>T1,则ΔH
。图1中投料比相同,温度T3>T2>T1,则ΔH②m=3时,该反应达到平衡状态后p(总)=20Mpa,恒压条件下各物质的物质的量分数与温度的关系如图2。则曲线b代表的物质为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH________ 0(填“大于”或“小于”);
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。
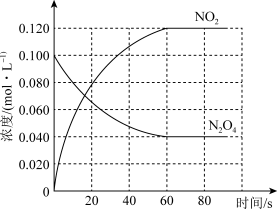
在0~60 s时段,反应速率v(N2O4)为___________________ mol·L-1·s-1;反应的平衡常数K的数值为_________________________ (保留两位小数)。
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向________ (填“正反应”或“逆反应”)方向移动。
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T________ 100 ℃(填“大于”或“小于”)。
(1)反应的ΔH
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。

在0~60 s时段,反应速率v(N2O4)为
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在某一容积为2 L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
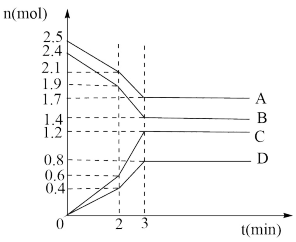
回答下列问题:
①该反应的化学方程式为______ ;
②前2 min用A的浓度变化表示的化学反应速率为____ ,在2 min时,图象发生改变的原因是_______ (填字母)。
A 增大压强 B 降低温度 C 加入催化剂 D 增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:
①该反应的化学方程式_______ ,达到平衡时四氧化二氮的转化率为____ ;
②反应速率最大的时间段为____ (指0~20s、20~40s、40~60s、60~80s、80~100 s),其原因是_____________

回答下列问题:
①该反应的化学方程式为
②前2 min用A的浓度变化表示的化学反应速率为
A 增大压强 B 降低温度 C 加入催化剂 D 增加A的物质的量
(2)在100 ℃时,将0.01 mol的四氧化二氮气体充入0.1 L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L-1 | 0.100 | 0.070 | 0.050 | c3 | a | b |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
①该反应的化学方程式
②反应速率最大的时间段为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)向2L密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
①0~2min内,v(NH3)=___ 。
②H2在平衡混合气体中的体积分数为__ 。
③平衡时容器的压强与起始时的压强之比为___ 。
(2)某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应的化学方程式为___ 。
②从开始至2min,B的平均反应速率为___ ;平衡时,C的浓度为___ ,A的转化率为_ 。
③下列叙述能说明该反应已达到化学平衡状态的是__ (填序号)。
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗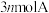 ,同时消耗
,同时消耗
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
④在某一时刻采取下列措施能使该反应速率减小的是___ (填序号)。
A.加正催化剂 B.降低温度 C.容积不变,充入A D.容积不变,从容器中分离出A
(1)向2L密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2
 2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:
2NH3,2min时达到平衡。测得平衡混合气体中NH3的体积分数为25%,则:①0~2min内,v(NH3)=
②H2在平衡混合气体中的体积分数为
③平衡时容器的压强与起始时的压强之比为
(2)某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

①该反应的化学方程式为
②从开始至2min,B的平均反应速率为
③下列叙述能说明该反应已达到化学平衡状态的是
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗
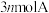 ,同时消耗
,同时消耗
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
④在某一时刻采取下列措施能使该反应速率减小的是
A.加正催化剂 B.降低温度 C.容积不变,充入A D.容积不变,从容器中分离出A
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在某一容积为2L的恒容密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化曲线如图所示。回答下列问题:
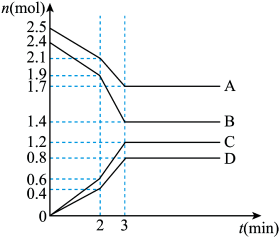
(1)该反应的化学方程式为______ 。
(2)前2min内用A的浓度变化表示的化学反应速率为_______ ,4min时,v正(A)______ v逆(D)(填“>”“<”或“=”)。
(3)在2min时,图象发生改变的原因可能是_____ (填字母)
A增大B的物质的量 B降低温度
C加入催化剂 D减小A的物质的量
(4)能说明该反应已达到平衡状态的标志是_______ (填字母)。
A消耗5mol B的同时生成4molD
B反应速率4v(B)= 5v(D)
C容器内D的浓度不再随时间而发生变化
D容器内压强不再随时间而发生变化
E容器内混合气体的密度不再随时间而发生变化
(5)由图示求得平衡时A的转化率为________ 。

(1)该反应的化学方程式为
(2)前2min内用A的浓度变化表示的化学反应速率为
(3)在2min时,图象发生改变的原因可能是
A增大B的物质的量 B降低温度
C加入催化剂 D减小A的物质的量
(4)能说明该反应已达到平衡状态的标志是
A消耗5mol B的同时生成4molD
B反应速率4v(B)= 5v(D)
C容器内D的浓度不再随时间而发生变化
D容器内压强不再随时间而发生变化
E容器内混合气体的密度不再随时间而发生变化
(5)由图示求得平衡时A的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】反应:aA(g)+bB(g) 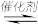 cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
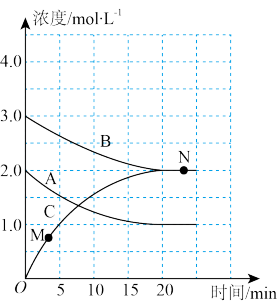
(1)该反应的化学方程式中,a:b:c为________ 。
(2)反应从起始至20min内,A的平均反应速率v (A)=_________ 。平衡时B的体积分数为_______ 。
(3)判断该反应是否达到平衡的依据为______ (填字母)。
A 压强不随时间改变
B A的物质的量分数不随时间改变
C 气体的密度不随时间改变
D 单位时间内消耗A和B的物质的量相等
(4)下列措施能增大反应速率的是______ (填字母)。
A 升高温度 B 降低压强 C 减小C的浓度 D 加入合适的催化剂
(5)N点的正反应速率v正(C)________ (填“大于”“小于”或“等于”)M点的逆反应速率v逆(C)。
 cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
cC(g)在恒温恒容条件下进行,各物质的浓度随时间变化的曲线如图所示。
(1)该反应的化学方程式中,a:b:c为
(2)反应从起始至20min内,A的平均反应速率v (A)=
(3)判断该反应是否达到平衡的依据为
A 压强不随时间改变
B A的物质的量分数不随时间改变
C 气体的密度不随时间改变
D 单位时间内消耗A和B的物质的量相等
(4)下列措施能增大反应速率的是
A 升高温度 B 降低压强 C 减小C的浓度 D 加入合适的催化剂
(5)N点的正反应速率v正(C)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学反应速率和限度是化工生产工艺中,需要特别关注的两个方面。某化工生产要合成C物质,需要在密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g) 2C(g),若达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。请回答下列问题:
2C(g),若达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。请回答下列问题:

(1)30 min和40 min时改变的外界条件依次是______
(2)化学方程式中的 x =______
(3)正反应为______ 热反应
(4)反应开始到8 min内A的平均反应速率为______
(5)35min时该反应的平衡常数为______
 2C(g),若达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。请回答下列问题:
2C(g),若达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如下图所示。请回答下列问题:
(1)30 min和40 min时改变的外界条件依次是
(2)化学方程式中的 x =
(3)正反应为
(4)反应开始到8 min内A的平均反应速率为
(5)35min时该反应的平衡常数为
您最近一年使用:0次

 气体,发生分解反应
气体,发生分解反应 ,控制不同的温度和压强,实验结果如图。
,控制不同的温度和压强,实验结果如图。


