利用活性炭可以处理NO的污染,其原理为: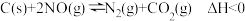 。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
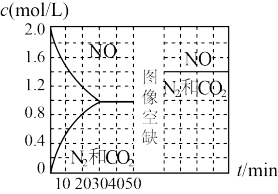
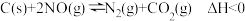 。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
。现向某容积固定的密闭容器加入一定量的活性炭和一定量的NO,在T1℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
| A.0~10min的平均速率v(CO2)=0.1mol·L-1·min-1 |
| B.50min时改变的条件是升温 |
C.若原平衡态压强为100kPa,维持体积不变,再通入一定量的CO2(g),达到平衡后压强变为150kPa,则平衡时NO转化了 |
| D.50min时改变的条件是加入高效的催化剂 |
2021·重庆·三模 查看更多[3]
更新时间:2021-05-20 21:17:49
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】汽车尾气中的氮氧化物主要来自发动机工作时氮气和氧气的化合,反应为N2(g)+O2(g) 2NO(g) ΔH=+180 kJ·mol−1。在2 000 K条件下,向10 L密闭容器中充入N2、O2各1 mol发生上述反应,相关物质的体积分数随时间的变化情况如表所示。
2NO(g) ΔH=+180 kJ·mol−1。在2 000 K条件下,向10 L密闭容器中充入N2、O2各1 mol发生上述反应,相关物质的体积分数随时间的变化情况如表所示。
下列有关说法不正确的是
 2NO(g) ΔH=+180 kJ·mol−1。在2 000 K条件下,向10 L密闭容器中充入N2、O2各1 mol发生上述反应,相关物质的体积分数随时间的变化情况如表所示。
2NO(g) ΔH=+180 kJ·mol−1。在2 000 K条件下,向10 L密闭容器中充入N2、O2各1 mol发生上述反应,相关物质的体积分数随时间的变化情况如表所示。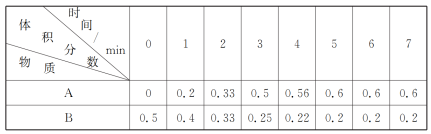
下列有关说法不正确的是
| A.0~5 min内v(NO)=0.024 mol·L−1·min−1 |
| B.当反应进行至各物质含量保持不变时,N2的转化率为60% |
| C.当反应进行至各物质含量保持不变时,放出的热量为180 kJ |
| D.若将容器的容积压缩到原来的1/2,则正、逆反应速率均加快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】T℃时在2L密闭容器中使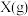 与
与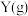 发生反应生成
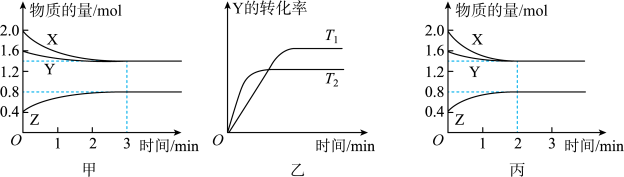
发生反应生成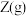 ,反应过程中X、Y、Z的物质的量变化如图甲所示;若保持其他条件不变,温度分别为T1和T2时,Y的转化率与时间的关系如图乙所示。则下列结论正确的是
,反应过程中X、Y、Z的物质的量变化如图甲所示;若保持其他条件不变,温度分别为T1和T2时,Y的转化率与时间的关系如图乙所示。则下列结论正确的是
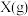 与
与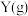 发生反应生成
发生反应生成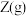 ,反应过程中X、Y、Z的物质的量变化如图甲所示;若保持其他条件不变,温度分别为T1和T2时,Y的转化率与时间的关系如图乙所示。则下列结论正确的是
,反应过程中X、Y、Z的物质的量变化如图甲所示;若保持其他条件不变,温度分别为T1和T2时,Y的转化率与时间的关系如图乙所示。则下列结论正确的是
A.反应进行的前 内,用X表示的反应速率 内,用X表示的反应速率 |
| B.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| C.若改变反应条件,使反应进程如图丙所示,则改变的条件是增大压强 |
D.容器中发生的反应可表示为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】利用催化技术可将汽车尾气中的 NO和 CO转变成CO2和N2,化学方程式:2NO(g)+2CO(g)  2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
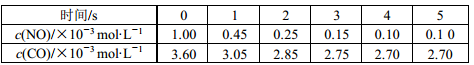
下列说法中不正确的是
 2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
下列说法中不正确的是
| A.2 s内的平均反应速率 v(N2)=1.875×10-4 mol·L-1·s-1 |
| B.在该温度下,反应的平衡常数 K=5 |
| C.若将容积缩小为原来的一半, NO 转化率大于 90% |
| D.使用催化剂可以提高整个过程中 CO 和 NO 的处理量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】反应: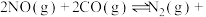 2CO2(g)
2CO2(g)  ,可用于消除汽车尾气中的有害气体。在密闭容器中充4mol NO和5mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是
,可用于消除汽车尾气中的有害气体。在密闭容器中充4mol NO和5mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是

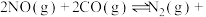 2CO2(g)
2CO2(g)  ,可用于消除汽车尾气中的有害气体。在密闭容器中充4mol NO和5mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是
,可用于消除汽车尾气中的有害气体。在密闭容器中充4mol NO和5mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法不正确的是
A.温度: |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】卤族元素单质及其化合物应用广泛。 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

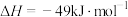 。下列关于反应
。下列关于反应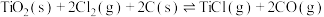 的说法
的说法不正确 的是
 具有与卤素单质相似的化学性质。
具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37.
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37. 通入
通入 酸性溶液中可制得黄绿色气体
酸性溶液中可制得黄绿色气体 ,该气体常用作自来水消毒剂。工业用
,该气体常用作自来水消毒剂。工业用 制备
制备 的热化学方程式为
的热化学方程式为

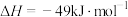 。下列关于反应
。下列关于反应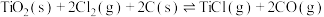 的说法
的说法A.保持其他条件不变,平衡时升高温度, |
B.保持其他条件不变,平衡时通入 ,达到新平衡时 ,达到新平衡时 变小 变小 |
C.反应生成1mol ,转移电子数目为 ,转移电子数目为 |
D.及时分离出CO,有利于 生成 生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】CO2催化重整CH4的反应:
(Ⅰ)CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1,
2CO(g)+2H2(g) ΔH1,
主要副反应:(Ⅱ)H2(g)+CO2(g) CO(g)+H2O(g) ΔH2>0,
CO(g)+H2O(g) ΔH2>0,
(Ⅲ)4H2(g)+CO2(g) CH4(g)+2H2O(g) ΔH3<0。
CH4(g)+2H2O(g) ΔH3<0。
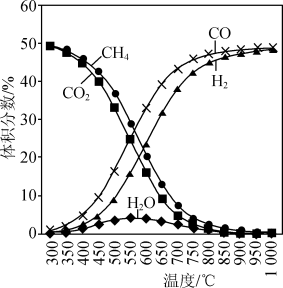
在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法不正确 的是
(Ⅰ)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1,
2CO(g)+2H2(g) ΔH1,主要副反应:(Ⅱ)H2(g)+CO2(g)
 CO(g)+H2O(g) ΔH2>0,
CO(g)+H2O(g) ΔH2>0,(Ⅲ)4H2(g)+CO2(g)
 CH4(g)+2H2O(g) ΔH3<0。
CH4(g)+2H2O(g) ΔH3<0。在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法

| A.ΔH1=2ΔH2-ΔH3>0 |
| B.其他条件不变,适当增大起始时V(CH4)∶V(CO2),可抑制副反应(Ⅱ)、(Ⅲ)的进行 |
| C.300~580℃时,H2O的体积分数不断增大,是由于反应(Ⅲ)生成H2O的量大于反应(Ⅱ)消耗的量 |
| D.T℃时,在2.0L容器中加入2molCH4、2molCO2以及催化剂进行重整反应,测得CO2的平衡转化率为75%,则反应(Ⅰ)的平衡常数小于81 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】温度为 时,在三个容积均为1L的恒容密闭容器中均发生反应:
时,在三个容积均为1L的恒容密闭容器中均发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: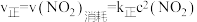 ,
,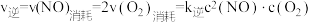 ,
, 、
、 为速率常数,受温度影响。
为速率常数,受温度影响。
下列说法正确的是
 时,在三个容积均为1L的恒容密闭容器中均发生反应:
时,在三个容积均为1L的恒容密闭容器中均发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: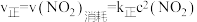 ,
,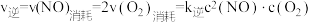 ,
, 、
、 为速率常数,受温度影响。
为速率常数,受温度影响。| 容器编号 | 物质的起始浓度( ) ) | 物质的平衡浓度( ) ) | ||
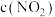 | 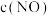 | 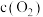 |
| |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
A.容器Ⅱ达到平衡前 |
B.达到平衡时,容器Ⅲ中 的体积分数大于50% 的体积分数大于50% |
C.设K为该反应的化学平衡常数,则有 |
D.当温度改变为 时,若 时,若 ,则 ,则 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是

| A.反应达到平衡时,X的转化率为80% |
B.该反应的平衡常数表达式为K=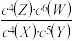 |
| C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
 2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是
2SO3(g)△H = -197kJ/mol。实验测得起始、平衡时的有关数据如右表所示。下列叙述正确的是| 容器 | 起始各物质的物质的量/mol | 达到平衡时体 系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A.Q1=Q2=Q3 |
| B.达到平衡时,丙容器中SO2的体积分数最大 |
| C.甲、乙、丙3个容器中反应的平衡常数不相等 |
| D.若在上述条件下反应生成2molSO3(s)的放热大于197kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】一定条件下 混合气体通过反应器,发生的反应有:
混合气体通过反应器,发生的反应有:
a.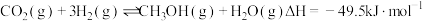
b.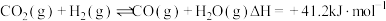
实验中检测反应器出口气体的成分及其含量,其他条件相同时,反应温度对 的转化率和
的转化率和 的选择性的影响如图1、如图2所示:
的选择性的影响如图1、如图2所示: 选择性
选择性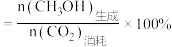
下列说法不正确 的是
 混合气体通过反应器,发生的反应有:
混合气体通过反应器,发生的反应有:a.
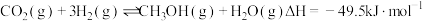
b.
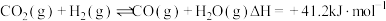
实验中检测反应器出口气体的成分及其含量,其他条件相同时,反应温度对
 的转化率和
的转化率和 的选择性的影响如图1、如图2所示:
的选择性的影响如图1、如图2所示:
 选择性
选择性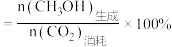
下列说法
| A.由如图1可知,实验中反应均未达到化学平衡状态 |
B.由如图1可知,温度高于 时, 时, 平衡转化率变化的原因是升高温度对反应b的影响程度大于对反应a的 平衡转化率变化的原因是升高温度对反应b的影响程度大于对反应a的 |
C.由如图2可知,温度相同时 选择性的实验值略高于其平衡值,可能原因是该温度下反应a的平衡常数大于反应b的 选择性的实验值略高于其平衡值,可能原因是该温度下反应a的平衡常数大于反应b的 |
D. 时,反应器出口气体中 时,反应器出口气体中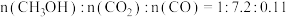 ,则该温度下 ,则该温度下 转化率 转化率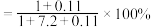 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】用活性炭还原法可以处理氮氧化物。某研究小组向2L密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) 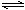 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
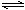 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是| 时间/t(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| A.10~20 min内,NO的平均反应速率为0.018mol/(L∙min) |
| B.T1℃时,该反应的平衡常数K=0.25 |
| C.保持与前30min的反应条件相同,再向容器中加入2molN2和2molNO,则平衡向左移动 |
| D.30min后,只改变了一个条件,根据上述表格判断,该条件可能为缩小容器体积 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】苯乙烯是生产各种塑料的重要单体,其制备原理C6H5—C2H5(g) C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是

 C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
| A.b点和c点温度和压强相同,则反应速率相同 |
| B.恒容时加入稀释剂,C6H5—C2H5平衡转化率不变 |
| C.a点转化率为75%,则混合气体中苯乙烯的体积分数为1/3 |
| D.b点转化率为50%,若起始向2L恒容容器中充入1mol乙苯,则平衡常数为0.5mol·L-1 |
您最近一年使用:0次



