近年来,有科学家提出,使用氯气消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。二氧化氯( ,是易溶于水的黄绿色气体)是高效、低毒的消毒剂。回答下列问题:
,是易溶于水的黄绿色气体)是高效、低毒的消毒剂。回答下列问题:
(1)工业上可用 与
与 在
在 存在下制得
存在下制得 。
。
①该反应的离子方程式为___________ 。
②每生成 ,消耗还原剂的物质的量为
,消耗还原剂的物质的量为___________  ,转移的电子数为
,转移的电子数为___________  。
。
(2)实验室以 、盐酸、
、盐酸、 为原料,通过图中流程制备
为原料,通过图中流程制备 。
。

① 属于
属于___________ (填“离子化合物”或“共价化合物”), 分子内存在
分子内存在___________ (填“极性键”、“非极性键”或“极性键和非极性键”)。
②除去 中的
中的 可选用的试剂是
可选用的试剂是___________ (填标号)。
a. 固体氯化钙
b. 澄清石灰水
c. 浓硫酸
d. 饱和食盐水
③ 溶液和
溶液和 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
 ,是易溶于水的黄绿色气体)是高效、低毒的消毒剂。回答下列问题:
,是易溶于水的黄绿色气体)是高效、低毒的消毒剂。回答下列问题:(1)工业上可用
 与
与 在
在 存在下制得
存在下制得 。
。①该反应的离子方程式为
②每生成
 ,消耗还原剂的物质的量为
,消耗还原剂的物质的量为 ,转移的电子数为
,转移的电子数为 。
。(2)实验室以
 、盐酸、
、盐酸、 为原料,通过图中流程制备
为原料,通过图中流程制备 。
。
①
 属于
属于 分子内存在
分子内存在②除去
 中的
中的 可选用的试剂是
可选用的试剂是a. 固体氯化钙
b. 澄清石灰水
c. 浓硫酸
d. 饱和食盐水
③
 溶液和
溶液和 发生反应的化学方程式为
发生反应的化学方程式为
更新时间:2021-07-20 17:08:32
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】已知氮化硅陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得: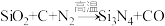 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
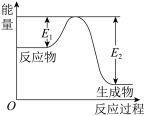
试回答下列问题。
(1)该反应中的氧化剂是________ ,还原产物是________ 。
(2)该反应是________ (填“吸热反应”或“放热反应”),
________ (填“>” “<”或“=”)0。
(3)该反应过程中,断裂旧化学键吸收的总能量________ (填“>”“<”或“=”)形成新化学键释放的总能量。
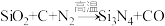 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
试回答下列问题。
(1)该反应中的氧化剂是
(2)该反应是

(3)该反应过程中,断裂旧化学键吸收的总能量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应: 2NaNO2+4HI=2NO↑+2NaI+I2+2H2O
(1)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为______ 。
(2)自来水中的 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。
____ Al+___  +
+_____ =____  +
+____ N2↑+____
(1)用双线桥法标出该反应中电子转移的方向及数目:
(2)自来水中的
 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。 +
+ +
+
您最近一年使用:0次
【推荐3】回答下列问题
(1)已知 ,在上述过程中
,在上述过程中 被
被___________ (填“氧化”或“还原”), 中M的化合价是
中M的化合价是___________ 价。
(2)已知常温下在溶液中可发生如下两个反应:


由此可以确定 、
、 、
、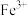 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是___________ 。
(3)由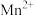 、
、 、
、 、
、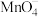 、
、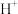 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,氧化剂是___________ ,氧化产物是___________ 。
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式并配平:___________ 。
___________+___________+___________→___________+___________
(4)实验室用 和浓盐酸制氯气的反应为
和浓盐酸制氯气的反应为
①用双线桥在方程式中标出电子转移的情况___________ ;
②反应中,如果有17.4g纯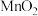 被还原,那么被氧化的氯化氢的质量为
被还原,那么被氧化的氯化氢的质量为___________ 。
(1)已知
 ,在上述过程中
,在上述过程中 被
被 中M的化合价是
中M的化合价是(2)已知常温下在溶液中可发生如下两个反应:


由此可以确定
 、
、 、
、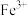 三种离子的氧化性由强到弱的顺序是
三种离子的氧化性由强到弱的顺序是(3)由
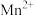 、
、 、
、 、
、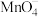 、
、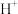 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,氧化剂是
②将以上物质分别填入下面对应的横线上,组成一个配平的离子方程式并配平:
___________+___________+___________→___________+___________

(4)实验室用
 和浓盐酸制氯气的反应为
和浓盐酸制氯气的反应为
①用双线桥在方程式中标出电子转移的情况
②反应中,如果有17.4g纯
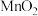 被还原,那么被氧化的氯化氢的质量为
被还原,那么被氧化的氯化氢的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在抗击新冠肺炎疫情的战役中,病毒在不断发生变异,因此民众的防疫意识不能松懈。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。研究表明新冠病毒可能通过气溶胶传播。气溶胶属于_______ (填“胶体”或“溶液”);常利用_______ 区分溶液和胶体。
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) =MnCl2+2H2O+Cl2↑
=MnCl2+2H2O+Cl2↑
b.□KMnO4+□HCl(浓)=□KCl+□MnCl2+□Cl2↑+□H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
①常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是_______ ,电解质是_______ 。
②写出反应c对应的离子方程式:_______ 。
③反应b配平后的系数依次为_______ 。
④a反应中,如果有17.4g纯MnO2被还原,被氧化的氯化氢的质量为_______ 。
(3)纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4,氯变为-1价。若把④中产生的Cl2完全转化,需要Na2SO3的质量为_______ 。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。研究表明新冠病毒可能通过气溶胶传播。气溶胶属于
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓)
 =MnCl2+2H2O+Cl2↑
=MnCl2+2H2O+Cl2↑b.□KMnO4+□HCl(浓)=□KCl+□MnCl2+□Cl2↑+□H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
①常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是
②写出反应c对应的离子方程式:
③反应b配平后的系数依次为
④a反应中,如果有17.4g纯MnO2被还原,被氧化的氯化氢的质量为
(3)纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4,氯变为-1价。若把④中产生的Cl2完全转化,需要Na2SO3的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】离子方程式RO +F2+mOH-=RO
+F2+mOH-=RO +aF-+H2O,试推算未知数n=
+aF-+H2O,试推算未知数n=___________ ,a=___________ ,m=___________ ,RO 中元素R的化合价为
中元素R的化合价为___________ 。
 +F2+mOH-=RO
+F2+mOH-=RO +aF-+H2O,试推算未知数n=
+aF-+H2O,试推算未知数n= 中元素R的化合价为
中元素R的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(Ⅰ)近年来我国对碳纳米管的研究也有了较大突破,即用电弧合成法来制碳纳米管,但往往有大量的碳纳米颗粒,需用氧化法来提纯这些颗粒,化学方程式为:

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为_______ ,被氧化的元素为________ 。
(3)H2SO4在上述反应中表现出来的性质是___ (填字母)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为__________ 。
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
_______________________________________________________
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是____ 。
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是____ 。

试回答下列问题:
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂为
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应若生成11 g CO2,则转移电子的数目为
(Ⅱ)2009年3月底至4月中旬,墨西哥、美国等多国接连暴发甲型H1N1型流感(或称H1N1型猪流感)疫情,随后也不断蔓延我国各地.防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感.
(5)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在H2SO4存在下与Na2SO3溶液反应制得。请写出该反应的离子方程式:
(6)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只被还原的是
A. MnO2 B.KMnO4溶液
C.稀盐酸 D.Na2SO3溶液
(7)漂白剂亚氯酸钠(NaClO2)在常温于黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子个数是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。几种主族元素在周期表中的位置如图:

根据上表回答下列问题:
(1)⑥元素的氢化物是______ (填化学式)。
(2)③④⑦三种元素简单离子半径由大到小的顺序是______ (用离子符号表示)。
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是______ ,用电子式表示该化合物的形成过程______ 。
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是______ ,最高价氧化物对应水化物酸性最强的化合物的化学式是______ 。
(5)写出②与水反应的离子方程式为______ 。
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是______ (填字母,下同)。
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是______ 。


根据上表回答下列问题:
(1)⑥元素的氢化物是
(2)③④⑦三种元素简单离子半径由大到小的顺序是
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是
(5)写出②与水反应的离子方程式为
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有下列物质:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
(1)上述物质中既含共价键又含离子键的是___________ (选填数字编号,下同);属于共价化合物的是___________ ;属于非极性分子的化合物是___________ 。
(2)④溶于水时破坏___________ ,固体⑦熔化时破坏___________ 。
A.离子键 B.共价键
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。(1)上述物质中既含共价键又含离子键的是
(2)④溶于水时破坏
A.离子键 B.共价键
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下面是同学们熟悉的物质:①O2 ②H2O ③MgCl2 ④HCl ⑤NaF ⑥CO2 ⑦CH4 ⑧CaO ⑨NaOH;这些物质中,属于盐的是____ (填序号,下同);属于共价化合物的是____ ;只含有离子键的是_____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将其与浓盐酸混合加热,产生黄绿色气体。
(1)反应中氧化剂是___ (填化学式)。
(2)若消耗了1molMnO2,则生成标准状况下Cl2的体积是___ L,转移电子的物质的量是__ mol。
(3)将21.9gHCl气体溶于水得到50mL的浓盐酸:求此浓盐酸的物质的量浓度___ 。
(1)反应中氧化剂是
(2)若消耗了1molMnO2,则生成标准状况下Cl2的体积是
(3)将21.9gHCl气体溶于水得到50mL的浓盐酸:求此浓盐酸的物质的量浓度
您最近一年使用:0次
【推荐2】化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。请推测并回答:
(1)NaAlH4中H元素化合价为___________ 。甲的化学式___________ 。
(2)甲与AlCl3反应得到NaAlH4的化学方程式___________ 。
(3)甲与水反应时,1mol甲可以转移电子个数为___________ 。
(1)NaAlH4中H元素化合价为
(2)甲与AlCl3反应得到NaAlH4的化学方程式
(3)甲与水反应时,1mol甲可以转移电子个数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】碱式硫酸铁[化学式Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,可由FeSO4和KClO3在水溶液中反应得到,有关反应的化学方程式如下:6FeSO4+KClO3+________=6Fe(OH)SO4+KCl
(1)请将上述化学方程式补充完整。________
(2)用双线桥法标出上述反应中转移电子的方向和数目。________
(3)上述反应中的还原剂是________ ,被还原的元素是________ ,每1molFeSO4参加反应,转移电子_________ mol。
(1)请将上述化学方程式补充完整。
(2)用双线桥法标出上述反应中转移电子的方向和数目。
(3)上述反应中的还原剂是
您最近一年使用:0次



