可逆反应2A(s)+3B(g)  C(g)+2D(g) ΔH<0,在一定条件下达到平衡。下列叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡。下列叙述正确的是
 C(g)+2D(g) ΔH<0,在一定条件下达到平衡。下列叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡。下列叙述正确的是| A.增加A的量,υ正加快,平衡向正反应方向移动 |
| B.升高温度,υ正、υ逆加快程度不同,平衡向逆反应方向移动 |
| C.缩小容器容积,υ正、υ逆不变,平衡不移动 |
| D.加入催化剂,B的平衡转化率提高 |
20-21高一下·黑龙江哈尔滨·期末 查看更多[3]
重庆市永川景圣中学校2021-2022学年高二上学期第一次月考化学试题(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期期末考试化学(理)试题
更新时间:2021-07-15 21:39:26
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法,其流程如图所示。已知向反应Ⅰ得到的产物中加过量I2会得到两层溶液-含低浓度I2的H2SO4层和含高浓度I2的HI层,这两层分别进行反应Ⅱ和Ⅲ,循环分解制氢。下列说法错误 的是
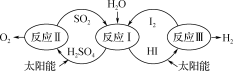

| A.反应Ⅰ的化学方程式为SO2+2H2O+I2=H2SO4+2HI |
| B.该流程将太阳能转化为化学能,且降低了水分解制氢的活化能 |
| C.反应Ⅲ是分解反应,I2是还原产物 |
| D.SO2和I2是反应2H2O=2H2+O2的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验能达到实验目的的是______ 。
| 序号 | 实验内容 | 实验目的 |
| A | 盛有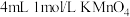 酸性溶液的两支试管,一只加入 酸性溶液的两支试管,一只加入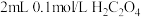 溶液,另一只加入 溶液,另一只加入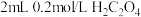 溶液 溶液 | 探究浓度对反应速率的影响 |
| B | 用石墨电极电解 、 、 的混合液 的混合液 | 比较确定铜和镁的金属活动性强弱 |
| C | 在容积可变的密闭容器中发生反应:2NO2(g) N2O4(g),把容器的体积缩小一半 N2O4(g),把容器的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | 向2支试管中各加入相同体积、相同浓度的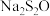 3溶液,再分别加入不同体积相同浓度的稀硫酸,分别放入冷水和热水中 3溶液,再分别加入不同体积相同浓度的稀硫酸,分别放入冷水和热水中 | 探究温度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】从下列实验事实所引出的相应结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 溴水中有平衡:Br2+H2O HBr+HBrO,当加入AgNO3固体后,溶液颜色变浅 HBr+HBrO,当加入AgNO3固体后,溶液颜色变浅 | 生成物浓度降低,平衡逆向移动 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | K2Cr2O7溶液中存在 (橙)+H2O (橙)+H2O 2 2 (黄)+2H+。加水稀释后,溶液颜色变黄 (黄)+2H+。加水稀释后,溶液颜色变黄 | 加水稀释使该反应的Q<K |
| D | H+浓度相同的盐酸和硫酸分别与等质量的形状相同的锌粒反应 | 硫酸反应速率快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】氨基甲酸铵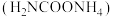 是一种氨化剂,易分解,易水解,难溶于
是一种氨化剂,易分解,易水解,难溶于 。某小组设计如图所示装置制备氨基甲酸铵。已知:
。某小组设计如图所示装置制备氨基甲酸铵。已知: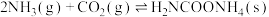
 。
。
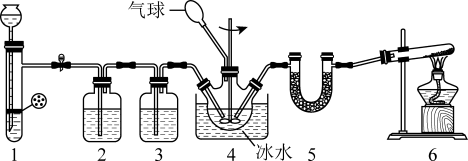
下列分析正确的是
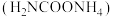 是一种氨化剂,易分解,易水解,难溶于
是一种氨化剂,易分解,易水解,难溶于 。某小组设计如图所示装置制备氨基甲酸铵。已知:
。某小组设计如图所示装置制备氨基甲酸铵。已知: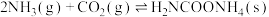
 。
。
下列分析正确的是
A.装置2中试剂为浓硫酸,装置3中试剂为饱和 溶液 溶液 |
| B.装置5中试剂可以为五氧化二磷 |
| C.装置4中冰水浴的目的是防止氨基甲酸铵分解 |
| D.装置4中发生的反应为氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,在2L的密闭容器中,充入4 mol A和2 mol B进行如下反应: ,反应一段时间达到平衡,测得生成1.6 mol C,则下列说法正确的是
,反应一段时间达到平衡,测得生成1.6 mol C,则下列说法正确的是
 ,反应一段时间达到平衡,测得生成1.6 mol C,则下列说法正确的是
,反应一段时间达到平衡,测得生成1.6 mol C,则下列说法正确的是| A.增大压强,平衡向逆反应方向移动 |
| B.达平衡后B的转化率为40% |
| C.增力A,平衡正向移动,化学平衡常数增大 |
D.若升高温度,A的转化率增大,则该反应 |
您最近一年使用:0次



