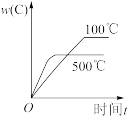
下列变化不能用勒夏特列原理解释的是
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
B.H2(g)+I2(g) 2HI(g)的平衡体系中压缩容器体积后颜色变深 2HI(g)的平衡体系中压缩容器体积后颜色变深 |
| C.Na2CrO4溶液中滴加稀硫酸,溶液颜色变深 |
| D.实验室用排饱和食盐水的方法收集氯气 |
19-20高二上·四川绵阳·阶段练习 查看更多[2]
四川省绵阳市南山中学实验学校2019-2020学年高二12月月考化学试题(已下线)2.3.3 温度对化学平衡的影响(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)
更新时间:2019-12-11 10:13:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸工业中通过 氧化氧化为
氧化氧化为 :
:
根据反应原理和上表中数据分析下列叙述错误的是
 氧化氧化为
氧化氧化为 :
:
| 温度/℃ | 平衡时 的转化率 的转化率 | ||||
 | 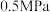 |  | 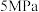 | 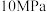 | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.实际生产中可以通过通入大量的空气来提高 的转化率 的转化率 |
B.常压下 的转化率已经比较大了,所以实际生产中没必要增大成本采用高压 的转化率已经比较大了,所以实际生产中没必要增大成本采用高压 |
C.生产中采用温度 主要是考虑催化剂的活性温度从而提高反应物的转化率 主要是考虑催化剂的活性温度从而提高反应物的转化率 |
D.尾气中的 必须回收循环利用防止污染环境并提高原料的利用率 必须回收循环利用防止污染环境并提高原料的利用率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
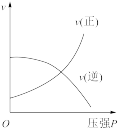
【推荐2】温度一定时,在恒压密闭容器中发生反应:2SO2(g)+O2(g)  2SO3(g)∆H=-197kJ/mol,下列有关说法正确的是
2SO3(g)∆H=-197kJ/mol,下列有关说法正确的是
 2SO3(g)∆H=-197kJ/mol,下列有关说法正确的是
2SO3(g)∆H=-197kJ/mol,下列有关说法正确的是| A.达到化学平衡状态时,v正(O2) = 2 v逆(SO2) |
| B.容器内的压强不再变化说明反应达到化学平衡状态 |
| C.加入 0.2 mol SO2和 0.1 mol O2,充分反应后放出热量 19.7 kJ |
| D.向容器中充入二氧化硫,正反应速率增大,逆反应速率减小,化学平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
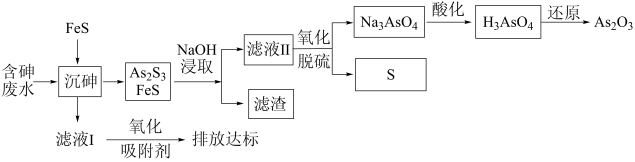
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq) 2AsS
2AsS (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq)
(aq)III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是
| A.As2S3中砷元素的化合价为+3价 |
| B.“沉砷”过程中FeS可以用过量的Na2S代替 |
C.用氧气进行“氧化脱硫”涉及离子方程式AsS +2O2=AsO +2O2=AsO +3S↓ +3S↓ |
| D.能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一密闭容器中加入等物质的量的A、B,发生如下反应: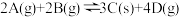 ,平衡常数随温度和压强的变化如表所示。下列判断正确的是
,平衡常数随温度和压强的变化如表所示。下列判断正确的是
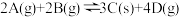 ,平衡常数随温度和压强的变化如表所示。下列判断正确的是
,平衡常数随温度和压强的变化如表所示。下列判断正确的是平衡常数 压强/MPa 温度/℃ | 1.0 | 1.5 | 2.0 |
| 300 | a | b | 16 |
| 516 | c | 64 | e |
| 800 | 160 | f | g |
| A.g>f |
B. |
| C.2.0MPa、800℃时,A的转化率最小 |
| D.1.5MPa、300℃时,B的转化率为50% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】可逆反应aA(s)+bB(g) cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是
cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是
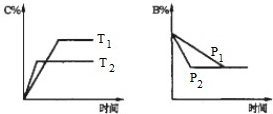
 cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是
cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是 
| A.T1 > T2 ,Q > 0 |
| B.Tl < T2 ,Q > 0 |
| C.P1 > P2 ,a+b=c+d |
| D.Pl< P2 ,b=c+d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列能用勒沙特列原理解释的是
| A.Fe(SCN)3溶液中加入固体KSCN后颜色变深,新制的氯水在光照条件下颜色变浅 |
B.2NO2 N2O4缩小体积增大压强,c(NO2)增大 N2O4缩小体积增大压强,c(NO2)增大 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D.H2、I2、HI平衡混和气加压后颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学与社会生活密切相关。下列叙述中,不能用勒夏特列原理解释的是
| A.食品包装中加抗氧化剂利于延长保质期 | B.用排饱和食盐水法收集氯气 |
| C.用浓氨水和氧化钙固体快速制取氨气 | D.用热的纯碱溶液洗去油污效果更好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
[Co(H2O)6]2++4Cl- [CoCl4]2- +6H2O ΔH
[CoCl4]2- +6H2O ΔH
用该溶液做实验,溶液的颜色变化如下:

已知:无水CoCl2呈蓝色,[Co(H2O)6]2+呈粉红色, [CoCl4]2-呈蓝色,[ZnCl4]2-为无色。
以下结论和解释不正确的是
[Co(H2O)6]2++4Cl-
 [CoCl4]2- +6H2O ΔH
[CoCl4]2- +6H2O ΔH用该溶液做实验,溶液的颜色变化如下:

已知:无水CoCl2呈蓝色,[Co(H2O)6]2+呈粉红色, [CoCl4]2-呈蓝色,[ZnCl4]2-为无色。
以下结论和解释不正确的是
| A.由实验①可推知△H>0 |
| B.实验②主要是由于c(H2O)增大,导致上述平衡逆向移动 |
| C.由实验③可知配合离子的稳定性: [ZnC14]2->[CoCl4]2- |
| D.蓝色钴玻璃片加入的物质是Co(AlO2)2,可以吸收黄光 |
您最近一年使用:0次

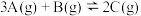
 ,下列各图正确的是
,下列各图正确的是