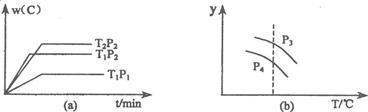
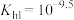在一个固定容积的密闭容器中,可发生以下反应:A(g)+B(g)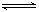 xC(g);∆H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
xC(g);∆H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
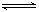 xC(g);∆H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
xC(g);∆H=?符合下图(a)所示的关系。w(c)为C的质量分数,由此推断关于图(b)的说法正确的是
| A.P3>P4,y轴表示A的转化率 |
| B.P3<P4,y轴表示B的体积分数 |
| C.P3<P4,y轴表示混合气体的平均相对分子质量 |
| D.P3>P4,y轴表示混合气体的密度 |
12-13高二上·黑龙江绥化·期中 查看更多[4]
天津市崇化中学2022-2023学年高二 上学期阶段性质量监测化学试卷夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学平衡移动及其影响因素(强化练习)河北省石家庄二中雄安校区-河北安新中学2019-2020学年高二上学期期中考试化学试题(已下线)2012-2013学年黑龙江省庆安三中高二上学期期中考试化学试卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】向两个不同容器中分别通入 和
和 ,发生反应:在压强为
,发生反应:在压强为 和
和 下分别达到平衡,平衡时
下分别达到平衡,平衡时 和
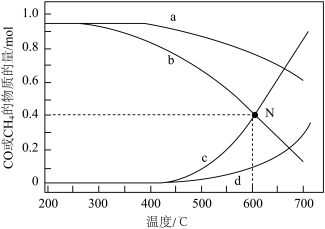
和 的物质的量在不同温度下的变化如图所示,下列说法正确的是
的物质的量在不同温度下的变化如图所示,下列说法正确的是
Ⅰ.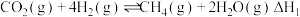
Ⅱ.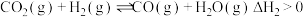
 和
和 ,发生反应:在压强为
,发生反应:在压强为 和
和 下分别达到平衡,平衡时
下分别达到平衡,平衡时 和
和 的物质的量在不同温度下的变化如图所示,下列说法正确的是
的物质的量在不同温度下的变化如图所示,下列说法正确的是
Ⅰ.
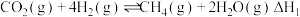
Ⅱ.
A.曲线c表示 时 时 的物质的量 的物质的量 |
B.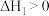 |
| C.在N点条件下,反应Ⅱ的平衡常数为2.4 |
D. ,随着温度升高 ,随着温度升高 的体积分数增大 的体积分数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一定条件下,[Zn(CN)4]2-与甲醛发生如下反应:[Zn(CN)4]2-+4HCHO+4H2O=[Zn(OH)4]2-+4HOCH2CN
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN- [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2
下列说法不正确 的是
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN-
 [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2下列说法
| A.反应前后Zn2+均提供4个空轨道容纳4对孤电子对 |
| B.HOCH2CN的氰基由CN-与甲醛发生反应而来 |
| C.依据上述[Zn(CN)4]2-与甲醛的反应可以证明:K1<K2 |
| D.上述反应必须在碱性条件下进行,既保证安全性,也能提高反应物转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
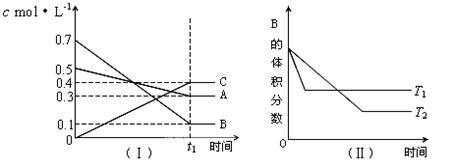

| A.在t1min时,3V正(B)=2V逆(C) |
| B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.T℃时,在相同容器中,若由0.3mol·L—1 A、0.1 mol·L—1 B和0.4 mol·L—1 C反应,达到平衡后,C的浓度仍为0.4 mol·L—1 |
| D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在1.0 L恒容密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g) Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是

 Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是
Y(g)+Z(g) ΔH<0,容器内气体总压强p随反应时间t的变化关系如图所示。以下分析正确的是 
| A.该温度下此反应的平衡常数K=3.2 |
| B.从反应开始到t1时的平均反应速率v(X)=0.2/t1 mol·L-1·min-1 |
| C.欲提高平衡体系中Y的百分含量,可加入一定量的X |
| D.其他条件不变,再充入0.1 mol气体X,平衡正向移动,X的转化率减少 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】可逆反应aA(g)+bB(g)⇌cC(g)+dD(g)△H,根据图像判断,下列叙述正确的是( )
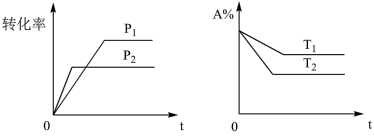

| A.p1<p2,a+b<c+d,T1<T2,△H>0 |
| B.p1<p2,a+b>c+d,T1>T2,△H>0 |
| C.p1<p2,a+b<c+d,T1>T2,△H>0 |
| D.以上答案均不对 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在容积一定的密闭容器中,可逆反应A(g)+B(g) xC(g),有如图所示的关系曲线,根据如图下列判断正确的是
xC(g),有如图所示的关系曲线,根据如图下列判断正确的是
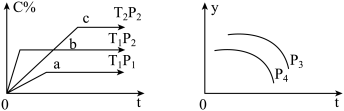
 xC(g),有如图所示的关系曲线,根据如图下列判断正确的是
xC(g),有如图所示的关系曲线,根据如图下列判断正确的是
| A.p3>p4,y轴表示A的物质的量分数 |
| B.p3>p4,y轴表示混合气体的平均摩尔质量 |
| C.p3<p4,y轴表示平衡常数K |
| D.若增大A的浓度,平衡体系颜色加深,C一定是有颜色的气体 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图I所示;若保持其他条件不变,温度分别为Tl和T2时,B的体积百分含量与时间的关系如图Ⅱ所示。则下列结论正确的是
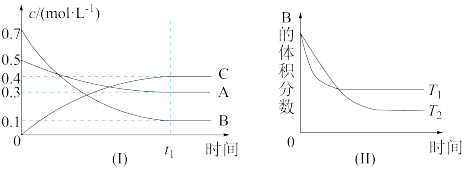

| A.在达平衡后,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.在达平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.保持其他条件不变,若反应开始时A、B、C的浓度分别为0.4mol·L-1、0.5 mol·L-1和0.2 mol·L—1,则达到平衡后,C的浓度大于0.4 mol·L-1 |
| D.保持其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次

 2HBr(g);ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g);ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是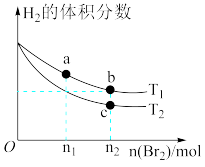
 三元酸
三元酸 溶液中滴加
溶液中滴加 的NaOH溶液,溶液中含A微粒的物质的量分数(
的NaOH溶液,溶液中含A微粒的物质的量分数( )随溶液pH的变化如图所示,下列说法正确的是
)随溶液pH的变化如图所示,下列说法正确的是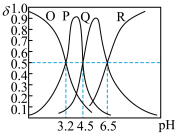
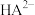 的物质的量分数与溶液pH的关系曲线
的物质的量分数与溶液pH的关系曲线 的水解常数
的水解常数