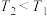在一定条件下,[Zn(CN)4]2-与甲醛发生如下反应:[Zn(CN)4]2-+4HCHO+4H2O=[Zn(OH)4]2-+4HOCH2CN
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN- [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2
下列说法不正确 的是
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN-
 [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2下列说法
| A.反应前后Zn2+均提供4个空轨道容纳4对孤电子对 |
| B.HOCH2CN的氰基由CN-与甲醛发生反应而来 |
| C.依据上述[Zn(CN)4]2-与甲醛的反应可以证明:K1<K2 |
| D.上述反应必须在碱性条件下进行,既保证安全性,也能提高反应物转化率 |
2022·北京海淀·三模 查看更多[3]
北京市海淀区北京大学附属中学2022届高三下学期三模化学试题山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题(已下线)第37讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)
更新时间:2022-05-31 14:26:25
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反应mX(g)+nY(g) pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
下列说法不正确的是
 pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g) △H=Q kJ/mol。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。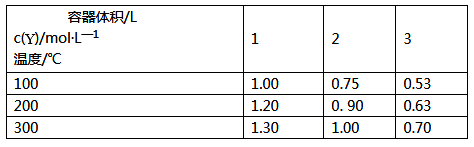
下列说法不正确的是
| A.m+n>p |
| B.Q <0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH3):CH3OH(g)+CO(g)⇌HCOOCH3 (g),在容积固定的密闭容器中,投入等物质的量CH3OH和CO,测得相同时间内CO的转化率随温度变化如图所示,下列说法正确的是
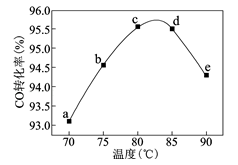

| A.a→c,CO的转化率随温度的升高而增大的原因是因为该反应是吸热反应,升高温度反应正向移动 |
| B.平衡常数Kb<Kd,由图可知生产时反应温度控制在80~85℃为宜 |
| C.向该容器中充入N2,CH3OH的转化率增大 |
| D.反应速率υb<υd |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。 乙基
乙基 甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是
甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是
 乙基
乙基 甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是
甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是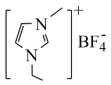
A.该离于液体中 杂化方式为 杂化方式为 、 、 |
| B.阴离子呈正四面体形,存在共价键和配位键 |
C.阳离子中 键数目是阴离子中 键数目是阴离子中 键数目的5倍 键数目的5倍 |
| D.该离子液体与水能够形成氢键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】利用氧化法制备 的化学方程式为
的化学方程式为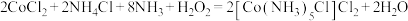 ,下列说法错误的是。
,下列说法错误的是。
 的化学方程式为
的化学方程式为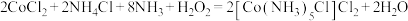 ,下列说法错误的是。
,下列说法错误的是。A.键角: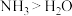 |
| B.反应物的各种晶体中存在共价晶体 |
| C.氢键作用能:O—H…O>N—H…N |
D.向 溶液中滴加 溶液中滴加 溶液有白色沉淀生成 溶液有白色沉淀生成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】硫元素的很多化合物用途广泛。 可用于制杀虫剂、发光漆等。高温下木炭和
可用于制杀虫剂、发光漆等。高温下木炭和 可以反应生成
可以反应生成 。在潮湿的空气中
。在潮湿的空气中 极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。
极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。 与
与 反应可以释放出
反应可以释放出 。
。 能与
能与 溶液发生复分解反应生成黑色
溶液发生复分解反应生成黑色 沉淀。
沉淀。 的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
 可用于制杀虫剂、发光漆等。高温下木炭和
可用于制杀虫剂、发光漆等。高温下木炭和 可以反应生成
可以反应生成 。在潮湿的空气中
。在潮湿的空气中 极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。
极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。 与
与 反应可以释放出
反应可以释放出 。
。 能与
能与 溶液发生复分解反应生成黑色
溶液发生复分解反应生成黑色 沉淀。
沉淀。 的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是A. 的空间构型为直线型 的空间构型为直线型 | B. 的价电子排布式为 的价电子排布式为 |
C. 的键角比 的键角比 的大 的大 | D. 中含有 中含有 键 键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列有关说法不正确的是
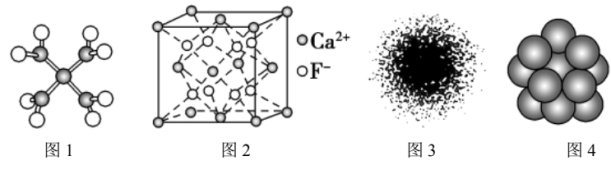

| A.四水合铜离子的模型如图1所示,1个四水合铜离子中有4个配位键 |
B. 晶体的晶胞如图2所示,设 晶体的晶胞如图2所示,设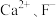 半径分别为 半径分别为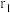 和 和 ,晶胞边长为a,则有 ,晶胞边长为a,则有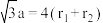 |
| C.H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动 |
| D.金属Cu中原子堆积模型如图4所示,为最密堆积,Cu原子的配位数为12 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】2020年某科研团队经多次实验发现一种新型漂白剂(结构见下图),可用于漂白蚕丝等织品,其组成元素均为短周期元素,W、X对应的简单离子核外电子排布相同,且W、Y、Z的最外层电子数之和等于X的最外层电子数,下列说法错误的是


| A.四种元素中X的电负性最大 |
| B.该物质中含有2mol配位键 |
| C.Y的最高价氧化物的水化物是一元弱酸 |
| D.离子半径:Z+˂W2+<X2- |
您最近一年使用:0次

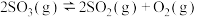 (正反应吸热),温度为
(正反应吸热),温度为 时,实验测得
时,实验测得 ,
,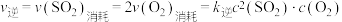 ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是 )
)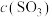
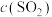

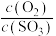 比容器I中的大
比容器I中的大 的体积分数小于50%
的体积分数小于50% 时,若
时,若 ,则
,则