恒容条件下,1molSiHCl3发生如下反应:2SiHCl3(g)⇌SiH2Cl2(g)+SiCl4(g)。已知:v正=v消耗(SiHCl3)=k正x2(SiHCl3),v逆=2v消耗(SiH2Cl2)=k逆x(SiH2Cl2)·x(SiCl4),k正、k逆分别为正、逆反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下x(SiHCl3)随时间的变化。下列说法正确的是
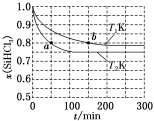

| A.该反应为放热反应,v正,a<v逆,b |
| B.化学平衡状态时,2v消耗(SiHCl3)=v消耗(SiCl4) |
C.当反应进行到a点时, = =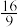 |
| D.T2K时,平衡体系中再充入1molSiHCl3,平衡正向移动,x(SiH2Cl2)增大 |
2019·河北唐山·一模 查看更多[7]
【全国百强校】河北省唐山市第一中学2019届高三下学期冲刺(一)理科综合化学试题浙江省宁波市效实中学2020届高三上学期第一次模拟考试化学试题(已下线)【新东方】2020-67(已下线)考点08 化学反应速率及其影响因素-2020年高考化学命题预测与模拟试题分类精编(已下线)专题讲座(五)反应速率、平衡图像题解题策略(练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市长郡中学2021-2022学年高二上学期第一次月考化学试题(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
更新时间:2021-09-06 08:46:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下,反应室(容积恒定为2L)中有反应:A(g)+2B(g)=C(g)。不能说明上述反应达到平衡状态的是( )
| A.反应中A与B的物质的量浓度之比为1:2 |
| B.混合气体总物质的量不再变化 |
| C.混合气体的平均摩尔质量不随时间的变化而变化 |
| D.2v正(A)=v逆(B) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒温条件下,在恒容密闭容器中充入1molCO2(g)和2molH2O(g)发生反应:CO2(g)+2H2O(g)⇌CH4(g)+2O2(g)。下列能说明该反应一定达到平衡状态的是
| A.2v正(CO2)=v逆(O2) |
| B.容器中压强保持不变 |
| C.CO2(g)与H2O(g)的物质的量之比为1:2且保持不变 |
| D.混合气体的平均相对分子质量保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在某密闭容器中发生可逆反应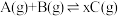 。当其他条件不变时,C 的体积分数与温度和压强的关系如图所示,下列说法不正确的是
。当其他条件不变时,C 的体积分数与温度和压强的关系如图所示,下列说法不正确的是
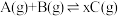 。当其他条件不变时,C 的体积分数与温度和压强的关系如图所示,下列说法不正确的是
。当其他条件不变时,C 的体积分数与温度和压强的关系如图所示,下列说法不正确的是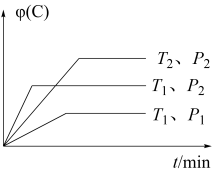
| A.p1<p2 | B.该反应为放热反应 |
| C.x≥1 | D.T1>T2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】CH4还原CO2是实现“双碳”经济的有效途径之一。相关的主要反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,密闭容器中发生反应aX(g) bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
 bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y的浓度是原来的1.8倍。则下列叙述正确的是 | A.可逆反应的系数:a>b +c |
| B.压缩容器的容积时,v(正)=v(逆) |
| C.达到新平衡时,混合物中Z的质量分数增大 |
| D.达到新平衡时,物质X的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知图1为一定温度下,压强与化学反应速率的关系曲线,图2为压强一定时,C%与温度、时间的关系曲线(图中C%表示某反应物在体系中的百分含量)。同时符合以下两个图示的反应是
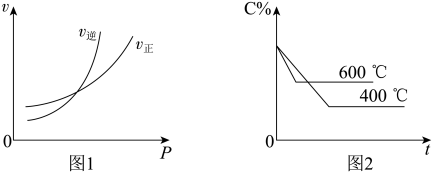

A.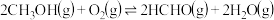  |
B.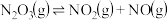  |
C.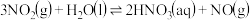  |
D.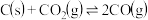  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验方法、操作均正确,且能达到实验目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 测定中和反应反应热 | 用简易量热器测量浓硫酸与NaOH溶液反应前后的温度 |
| B | 探究温度对化学平衡的影响 | 将NO2球分别浸泡在冷水和热水中,观察溶液颜色变化 |
| C | 探究压强对化学反应平衡移动的影响 | 容器中反应H2(g) + I2(g)  2HI(g)达平衡时,将容器压缩为原体积的 2HI(g)达平衡时,将容器压缩为原体积的 ,观察颜色变化 ,观察颜色变化 |
| D | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的盐酸,分别加入等体积、等浓度的NaOH溶液,对比现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是

