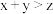CH4还原CO2是实现“双碳”经济的有效途径之一。相关的主要反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
更新时间:2023-12-14 11:33:39
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和 ,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是

 ,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
,在无、有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
A.可以通过 和 和 计算HCOOH的总键能 计算HCOOH的总键能 |
B. |
C.途径Ⅱ中 参与反应,通过改变反应途径加快反应速率 参与反应,通过改变反应途径加快反应速率 |
| D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| B.铁表面镀铜时,铜与电源的负极相连,而铁与电源的正极相连 |
| C.某反应的平衡常数K300℃>K350℃,则该反应 △H<0 |
| D.合成氨生产中将NH3液化分离,目的是加快正反应速率,提高H2的转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下在密闭烧瓶内发生反应:2NO2(g) N2O4(g) △H<0。下列说法正确的是
N2O4(g) △H<0。下列说法正确的是
 N2O4(g) △H<0。下列说法正确的是
N2O4(g) △H<0。下列说法正确的是| A.测定NO2的相对分子质量时,选择高温、高压条件时误差较小 |
| B.将烧瓶放入热水中,正逆反应速率均加快,烧瓶内气体颜色加深 |
| C.若向烧瓶内充入NO2,平衡向右移动,烧瓶内气体颜色比原来的浅 |
| D.若向烧瓶内充入N2,烧瓶内压强增大,反应速率加快 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式不能正确表示体系颜色变化的是
| A.向AgCl悬浊液中加Na2S溶液,有黑色难溶物生成:2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-(aq) |
B.向酸性KMnO4溶液中加入NaHSO3固体,溶液紫色褪去:2MnO +5SO +5SO +6H+=2Mn2++5SO +6H+=2Mn2++5SO +3H2O +3H2O |
C.向橙色K2Cr2O7溶液中加入NaOH溶液,溶液变黄色:Cr2O +2OH-=2CrO +2OH-=2CrO +H2O +H2O |
D.向稀硝酸中加入铜粉,溶液变蓝色:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】北京航空航天大学教授团队与中科院高能物理研究所合作,合成了两种单原子催化剂Y/NC和Sc/NC,实现常温常压下催化还原氮气合成氨气,反应历程与相对能量如图所示(*表示稀土单原子催化剂)。下列说法错误的是
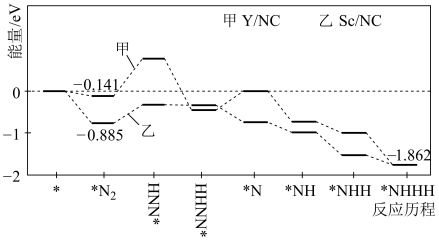

A. 的值甲>乙 的值甲>乙 |
| B.升高温度氨气的产率不一定提高 |
C.Sc/NC比Y/NC更有利于吸附 |
D.使用Y/NC单原子催化剂时,历程中决速步的反应为: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在容积可变的密闭容器中存在如下反应:2A(g)+2B(g) C(g)+3D(g) ∆H<0,该可逆反应的反应速率-时间、转化率-时间关系图如下,下列分析中不正确的是
C(g)+3D(g) ∆H<0,该可逆反应的反应速率-时间、转化率-时间关系图如下,下列分析中不正确的是
 C(g)+3D(g) ∆H<0,该可逆反应的反应速率-时间、转化率-时间关系图如下,下列分析中不正确的是
C(g)+3D(g) ∆H<0,该可逆反应的反应速率-时间、转化率-时间关系图如下,下列分析中不正确的是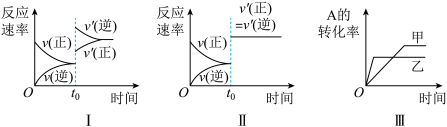
A.图Ⅰ可体现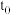 时升高温度对反应速率的影响 时升高温度对反应速率的影响 |
B.图Ⅱ可体现 时缩小体积增大压强或使用催化剂对反应速率的影响 时缩小体积增大压强或使用催化剂对反应速率的影响 |
| C.图Ⅲ可体现催化剂对化学平衡的影响,且乙使用了催化剂 |
| D.图Ⅲ可体现温度对化学平衡的影响,且乙的温度较高 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在1L密闭容器中进行如下反应:X(g)+3Y(g) 2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
 2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是| A.化学平衡常数不变,平衡不移动 | B.向正反应方向移动 |
| C.向逆反应方向移动 | D.容器内压强始终保持原来的2倍 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在373K时,把0.5molN2O4气通入体积为5L的恒容真空密闭容器中立即出现红棕色,反应进行到2s时,NO2的浓度为0.02mol/L,在60s时体系达到平衡,此时容器内压强为开始压强的1.6倍。下列说法正确的是
| A.前2svN2O4=0.01mol/L·s |
| B.2s时体系内压强为开始时的1.1倍 |
| C.平衡时体系内含N2O40.25mol |
| D.平衡时若压缩容器体积可提高N2O4的转化率 |
您最近半年使用:0次

 催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。
催化重整的反应过程中,还发生积炭反应,积炭的存在会使催化剂失活。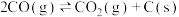

 裂解:
裂解:
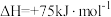
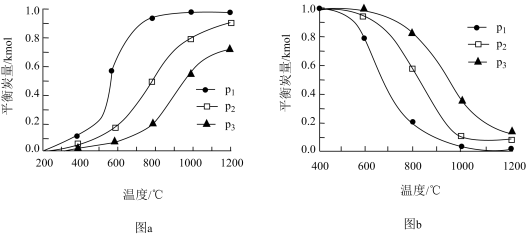

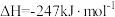
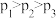
 CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是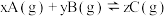 ,平衡时测得A的浓度为
,平衡时测得A的浓度为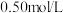 。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得A的浓度变为
。保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得A的浓度变为 。下列有关判断不正确的是
。下列有关判断不正确的是