在1L密闭容器中进行如下反应:X(g)+3Y(g) 2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
 2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是| A.化学平衡常数不变,平衡不移动 | B.向正反应方向移动 |
| C.向逆反应方向移动 | D.容器内压强始终保持原来的2倍 |
更新时间:2018-12-06 11:09:31
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
| A.再通入少量氯气,c(H+)/c(ClO-)减小 |
| B.通入少量SO2,溶液漂白性增强 |
| C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) |
| D.加入少量固体NaOH,溶液的pH会略微增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.向水中加入少量NaOH(s)后恢复至常温,溶液的pH增大 |
| B.氯水中加入CaCO3粉末以提高氯水中HClO的浓度 |
| C.将碳酸饮料瓶摇晃后,拧开瓶盖立即有大量泡沫溢出 |
| D.盛有Na2S2O3与稀H2SO4混合溶液的试管浸入热水中,溶液迅速变浑浊 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理解释的是( )
A.溴水中存在如下平衡:Br2+H2O HBr+HBrO,当加入NaOH溶液后颜色变浅 HBr+HBrO,当加入NaOH溶液后颜色变浅 |
B.合成氨反应:N2+3H2 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施 |
C.反应:CO+NO2 CO2+NO ΔH<0,升高温度,平衡向逆反应方向移动 CO2+NO ΔH<0,升高温度,平衡向逆反应方向移动 |
D.对2H2O2 2H2O+O2↑的反应,使用MnO2可加快制O2的反应速率 2H2O+O2↑的反应,使用MnO2可加快制O2的反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在密闭容器中自发进行可逆反应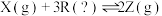
 ,反应达到平衡后,在
,反应达到平衡后,在 时仅降低温度,正、逆反应速率的变化如图①所示;达到平衡后,在不同压强下测得体系内某物质平衡时的物理量随温度变化如图②所示(物质的状态不随温度而改变)。下列有关该反应的说法中正确的是
时仅降低温度,正、逆反应速率的变化如图①所示;达到平衡后,在不同压强下测得体系内某物质平衡时的物理量随温度变化如图②所示(物质的状态不随温度而改变)。下列有关该反应的说法中正确的是

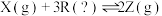
 ,反应达到平衡后,在
,反应达到平衡后,在 时仅降低温度,正、逆反应速率的变化如图①所示;达到平衡后,在不同压强下测得体系内某物质平衡时的物理量随温度变化如图②所示(物质的状态不随温度而改变)。下列有关该反应的说法中正确的是
时仅降低温度,正、逆反应速率的变化如图①所示;达到平衡后,在不同压强下测得体系内某物质平衡时的物理量随温度变化如图②所示(物质的状态不随温度而改变)。下列有关该反应的说法中正确的是
A. | B.y可能为气体X的转化率 |
C. | D.物质R为气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知N2(g)+3H2(g) 2NH3(g)ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2molN2和8molH2达到平衡时生成1molNH3。现在相同条件下的同一容器中充入xmolN2,ymolH2和2molNH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为( )
2NH3(g)ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2molN2和8molH2达到平衡时生成1molNH3。现在相同条件下的同一容器中充入xmolN2,ymolH2和2molNH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为( )
 2NH3(g)ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2molN2和8molH2达到平衡时生成1molNH3。现在相同条件下的同一容器中充入xmolN2,ymolH2和2molNH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为( )
2NH3(g)ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2molN2和8molH2达到平衡时生成1molNH3。现在相同条件下的同一容器中充入xmolN2,ymolH2和2molNH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为( )| A.5,21 | B.3,13 | C.2,9 | D.1.5,7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在1 L密闭容器中通入2 mol NH3,在一定温度下发生反应:2NH3 N2+3H2,达到平衡状态时,N2的物质的量分数为a%,维持容器的容积和温度不变,分别通入下列几组物质,达到平衡状态时,容器内N2的物质的量分数仍为a%的是
N2+3H2,达到平衡状态时,N2的物质的量分数为a%,维持容器的容积和温度不变,分别通入下列几组物质,达到平衡状态时,容器内N2的物质的量分数仍为a%的是
 N2+3H2,达到平衡状态时,N2的物质的量分数为a%,维持容器的容积和温度不变,分别通入下列几组物质,达到平衡状态时,容器内N2的物质的量分数仍为a%的是
N2+3H2,达到平衡状态时,N2的物质的量分数为a%,维持容器的容积和温度不变,分别通入下列几组物质,达到平衡状态时,容器内N2的物质的量分数仍为a%的是| A.3 mol H2和1 mol NH3 |
| B.2 mol N2和3 mol H2 |
| C.1 mol N2和3 mol NH3 |
| D.0.1 mol NH3、0.95 mol N2、2.85 mol H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,向某密闭容器中充入1.6 molH2与1.0molCO,发生如下可逆反应并达到平衡:H2(g)+CO(g)⇌C(s)+H2O(g)+Q kJ(Q>0).若压缩容器体积并同时升高温度,达到新平衡后,关于下列物理量的变化情况叙述错误的是( )
| A.反应速率一定增大 |
| B.平衡常数一定减小 |
| C.混合气体的平均摩尔质量可能减小 |
| D.H2O(g)的体积分数可能增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一氧化氮的氢化还原反应为2NO(g)+2H2(g)  N2(g)+2H2O(g) ΔH=-664kJ·mol-1,其正反应速率方程为v=kca(NO)·cb(H2),T℃时,实验得到的一组数据如下表所示:
N2(g)+2H2O(g) ΔH=-664kJ·mol-1,其正反应速率方程为v=kca(NO)·cb(H2),T℃时,实验得到的一组数据如下表所示:
下列说法正确的是
 N2(g)+2H2O(g) ΔH=-664kJ·mol-1,其正反应速率方程为v=kca(NO)·cb(H2),T℃时,实验得到的一组数据如下表所示:
N2(g)+2H2O(g) ΔH=-664kJ·mol-1,其正反应速率方程为v=kca(NO)·cb(H2),T℃时,实验得到的一组数据如下表所示:| 实验组别 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 正反应速率/(mol·L-1·s-1) |
| I | 6.00×10-3 | 2.00×10-3 | 2.16×10-3 |
| II | 1.20×10-2 | 2.00×10-3 | 8.64×10-3 |
| III | 6.00×10-3 | 4.00×10-3 | 4.32×10-3 |
| A.平衡常数:K(I)<K(II) |
| B.a=1,b=2 |
| C.升高温度,k的值减小 |
| D.增大NO浓度比增大H2浓度对正反应速率影响大 |
您最近一年使用:0次

 与
与 反应生成NO,NO进一步氧化生成
反应生成NO,NO进一步氧化生成 。
。
 。大气中过量的
。大气中过量的 和水体中过量的
和水体中过量的 、
、 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为 ,下列说法正确的是
,下列说法正确的是 ,NO的转化率下降
,NO的转化率下降
 ,
,
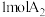 和
和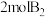 ,发生反应
,发生反应 。在达到平衡后,生成
。在达到平衡后,生成 。当温度不变时,若起始加入的
。当温度不变时,若起始加入的 、
、 、AB的物质的量分别为:x,y,z,则下列说法正确的是
、AB的物质的量分别为:x,y,z,则下列说法正确的是 ,
,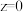 ,则达新平衡状态时
,则达新平衡状态时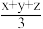
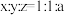 ,则达新平衡状态时
,则达新平衡状态时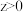 ,则达新平衡状态时
,则达新平衡状态时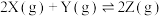 反应,平衡时X的转化率与温度变化关系如图所示曲线上任何一点都表示平衡状态,下列说法中正确的是
反应,平衡时X的转化率与温度变化关系如图所示曲线上任何一点都表示平衡状态,下列说法中正确的是

 、
、 时的平衡常数分别为
时的平衡常数分别为 、
、 ,则
,则
 时,当反应处于D点,则该反应的逆反应速率大于正反应速率
时,当反应处于D点,则该反应的逆反应速率大于正反应速率

