向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[t0~t1阶段c(B)未画出]。图乙为t2时刻后改变条件平衡体系中化学反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件并且改变的条件均不同。已知,t3~t4阶段为使用催化剂。下列说法正确的是


| A.t5~t6阶段可能是减小压强 |
| B.t4~t5阶段改变的条件为降低反应温度 |
| C.B的起始物质的量为0.02mol |
| D.若t1=15s,生成物C在t0~t1时间段的化学反应速率为0.004mol·L-1·s-1 |
更新时间:2021-10-11 10:23:54
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在一定温度下,将气体X和Y各1.6mol充入10L恒容密闭容器中,发生如下反应:
X(g)+ Y(g) 2Z(g),在反应过程中,X的物质的量与时间的关系如下表所示:
2Z(g),在反应过程中,X的物质的量与时间的关系如下表所示:
下列说法不正确的是
X(g)+ Y(g)
 2Z(g),在反应过程中,X的物质的量与时间的关系如下表所示:
2Z(g),在反应过程中,X的物质的量与时间的关系如下表所示:t/min | 0 | 2 | 4 | 6 | 8 | …… | 16 | 18 |
n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | …… | …… | 1.000 | 1.000 |
| A.4~6min时间段内Z的平均反应速率为2.5×10-3mol/(L·min) |
| B.此温度下该反应的平衡常数K=1.44 |
C.达平衡后,升高温度, 减小,则正反应 减小,则正反应 |
| D.若保持其他条件不变,再充入1.6mol Z,达新平衡后Z的体积分数不变 |
您最近一年使用:0次
【推荐2】下列有关实验内容、实验装置和对应的实验目的均正确的是

| A.图①不能用于探究氧化性: KMnO4>Cl2>I2 |
| B.图②验证CuCl2对双氧水分解的催化作用 |
| C.图③通过测定收集一定体积氢气所用的时间来测量锌粒和一定浓度的稀硫酸反应的速率 |
| D.图④比较不同温度对化学反应速率的影响 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】我国科学家团队打通了温和条件下草酸二甲酯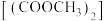 催化加氢制乙二醇的技术难关,反应为
催化加氢制乙二醇的技术难关,反应为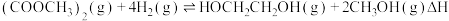 。如图所示,在恒容密闭容器中,反应温度为
。如图所示,在恒容密闭容器中,反应温度为 时,
时,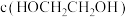 和
和 随时间
随时间 的变化分别为曲线I和II,反应温度为
的变化分别为曲线I和II,反应温度为 时,
时, 随时间
随时间 的变化为曲线Ⅲ。下列判断正确的是
的变化为曲线Ⅲ。下列判断正确的是
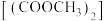 催化加氢制乙二醇的技术难关,反应为
催化加氢制乙二醇的技术难关,反应为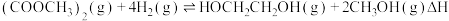 。如图所示,在恒容密闭容器中,反应温度为
。如图所示,在恒容密闭容器中,反应温度为 时,
时,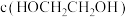 和
和 随时间
随时间 的变化分别为曲线I和II,反应温度为
的变化分别为曲线I和II,反应温度为 时,
时, 随时间
随时间 的变化为曲线Ⅲ。下列判断正确的是
的变化为曲线Ⅲ。下列判断正确的是
| A.该反应反应物的总能量小于生成物的总能量 |
B. 两时刻生成乙二醇的速率: 两时刻生成乙二醇的速率: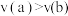 |
C.在 温度下,反应在 温度下,反应在 内的平均速率为 内的平均速率为 |
D.其他条件相同,在 温度下,起始时向该容器中充入一定量的氩气,则反应达到平衡时 温度下,起始时向该容器中充入一定量的氩气,则反应达到平衡时 |
您最近一年使用:0次
单选题
|
较难
(0.4)
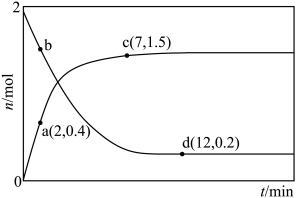
【推荐2】在160℃、250℃条件下,分别向两个固定容积为2L的容器中充入2molCO(g)和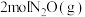 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
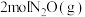 ,发生反应:
,发生反应:
 。实验测得两容器中CO或
。实验测得两容器中CO或 的物质的量随时间的变化关系如图所示。下列说法错误的是
的物质的量随时间的变化关系如图所示。下列说法错误的是
A.ac段 的平均反应速率为 的平均反应速率为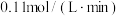 |
| B.曲线bd对应160℃条件下的反应 |
C.正反应速率: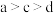 |
D.160℃时,该反应的平衡常数 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】将 4 mol A 气体和 2 mol B 气体在 2 L 的定容容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )| A.①③ | B.②⑤ | C.③⑤ | D.②③ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】通过反应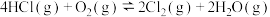 可将有机氯化工业的副产品HCl转化为
可将有机氯化工业的副产品HCl转化为 。体积不变的密闭容器中,保持
。体积不变的密闭容器中,保持 相同,进料比
相同,进料比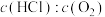 分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
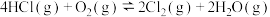 可将有机氯化工业的副产品HCl转化为
可将有机氯化工业的副产品HCl转化为 。体积不变的密闭容器中,保持
。体积不变的密闭容器中,保持 相同,进料比
相同,进料比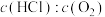 分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是
分别为1:1、4:1、7:1时HCl的平衡转化率随温度变化关系如图所示。下列说法正确的是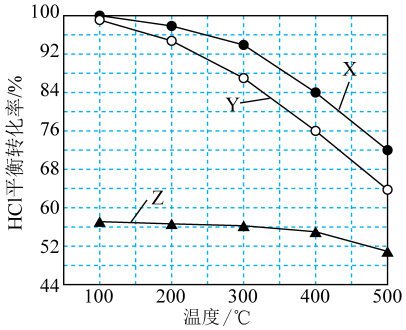
A.上述反应 |
B.曲线X表示的是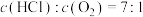 的变化 的变化 |
| C.其他条件不变,使用高效催化剂能使曲线Y与曲线X重叠 |
D.设HCl初始浓度为 ,根据进料 ,根据进料 的数据计算 的数据计算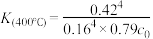 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列实验的操作、现象及结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 向盛有未知溶液的试管中滴加足量NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中不含 |
B | 向2支分别盛有5mL | 均有气泡产生且 |
|
C | 往 | 溶液先变成血红色后无明显变化 |
|
D | 用50mL注射器抽入20mL | 混合气体的颜色先变深再变浅 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】我国提出“CO2排放力争于2023年前达到峰值,努力争取2060年前实现碳中和”。研发CO2的利用技术,降低空气中CO2的含量是实现该目标的重要途径。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1
II.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
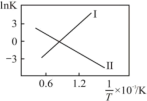
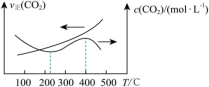
①反应I、II的lnK随1/T的变化如图所示,则ΔH2___________ 0(填“>”“<”或“=”)0;有利于反应I自发进行的温度是___________ (填“高温”或“低温”)。___________ ,而速率仍然增大的可能原因是___________ ___________ ,反应II的平衡常数Kp为___________ (保留两位有效数字)。[已知:CH4的选择性=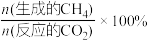 ]
]
(2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。___________ ,该化学链的总反应是___________ 。
(1)下面是用H2捕捉CO2时发生的两个反应:
I.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1
CH4(g)+2H2O(g) ∆H1II.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2①反应I、II的lnK随1/T的变化如图所示,则ΔH2
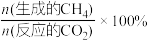 ]
](2)利用化学链将高炉废气中的CO2转化为CO的示意图如下。

您最近一年使用:0次
单选题
|
较难
(0.4)
名校
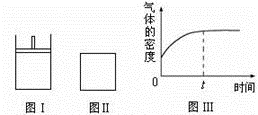
【推荐1】如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+ Y(?) a Z(g)。
a Z(g)。
此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断不正确的是
 a Z(g)。
a Z(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断不正确的是

| A.物质Z的化学计量数a =1 |
| B.若X、Y均为气态,则在平衡时X的转化率:Ⅰ>Ⅱ |
| C.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态 |
| D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知:。向体积可变的密闭容器中充入一定量的CH4(g)和O2(g)发生反应,CH4(g)的平衡转化率与温度(T)和压强(p)的关系如下图所示(已知T1>T2)。
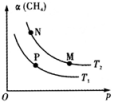
下列说法正确的是

下列说法正确的是
| A.该反应的△H>0 |
| B.M、N两点的H2的物质的量浓度:c(M)>c(N) |
| C.温度不变时,增大压强可由N点到P点 |
| D.N、P两点的平衡常数:K(N)<K(P) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:a、b、c三个容器中分别发生下列反应:
a: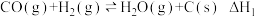
b: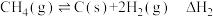
c:
反应a、b、c的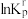 随
随 (温度的倒数)的变化如图所示,它们的起始压强相同,起始投料不同。设
(温度的倒数)的变化如图所示,它们的起始压强相同,起始投料不同。设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以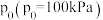 。下列说法错误的是
。下列说法错误的是
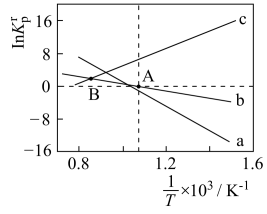
a:
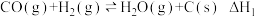
b:
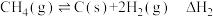
c:

反应a、b、c的
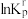 随
随 (温度的倒数)的变化如图所示,它们的起始压强相同,起始投料不同。设
(温度的倒数)的变化如图所示,它们的起始压强相同,起始投料不同。设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以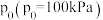 。下列说法错误的是
。下列说法错误的是
A.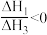 |
B.反应b的相对压力平衡常数表达式为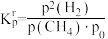 |
C.B点处有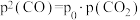 |
D.A点对应温度、原料组成为 、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时 、初始总压为100kPa的恒容密闭容器中进行反应,体系达到平衡时 的分压为40kPa,此时 的分压为40kPa,此时 的平衡转化率为68% 的平衡转化率为68% |
您最近一年使用:0次

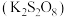 与
与 溶液混合发生反应
溶液混合发生反应 ,
,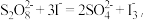 反应机理为:
反应机理为: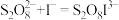 ;②……;③
;②……;③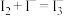 (快);反应速率方程
(快);反应速率方程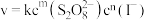 ,k为速率常数。已知该反应速率随反应物浓度的变化如下表所示:
,k为速率常数。已知该反应速率随反应物浓度的变化如下表所示: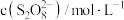

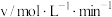

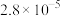
 ,
,
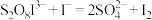
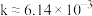

 、
、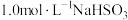 溶液的试管中同时加入2mL5%
溶液的试管中同时加入2mL5% 溶液
溶液
 溶液产生气泡快
溶液产生气泡快 溶液中滴加KSCN溶液,再加入少量
溶液中滴加KSCN溶液,再加入少量 固体
固体 与
与 的反应不可逆
的反应不可逆 和
和 混合气体,细管端用橡胶塞封闭,将针筒迅速推至10mL处
混合气体,细管端用橡胶塞封闭,将针筒迅速推至10mL处 平衡右移
平衡右移

