T℃时,向一个容积为2L的密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: ,反应过程中测得的部分数据如表。下列说法不正确的是
,反应过程中测得的部分数据如表。下列说法不正确的是
 ,发生如下反应:
,发生如下反应: ,反应过程中测得的部分数据如表。下列说法不正确的是
,反应过程中测得的部分数据如表。下列说法不正确的是 | 0 | 10 | 20 | 30 |
 | 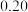 |  |  | |
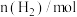 |  |  |
A.若其他条件不变,升高温度,平衡时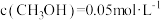 ,则该反应的 ,则该反应的 |
B.在前10min内该反应的平均反应速率 |
C.T℃时,该反应的平衡常数为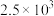 |
D.相同温度下,若起始时向该容器中只充入 ,达到平衡时 ,达到平衡时 的转化率小于20% 的转化率小于20% |
更新时间:2021-10-20 16:41:58
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列测量化学反应速率的依据不可行的是
| 选项 | 化学反应 | 测量依据(单位时间内) |
| A | 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O | 溶液颜色变化 |
| B | AgNO3+NaCl=AgC1↓+NaNO3 | 沉淀质量变化 |
| C | H2(g)+I2(g) 2HI(g) 2HI(g) | 温度、体积一定时,体系压强变化 |
| D | H2O2+2HI=2H2O+I2 | 溶液体积一定时,I-的浓度变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)在不同条件下进行,下列表示的反应速率最快的是
| A.v(NH3)=0.012mol·L-1·s-1 | B.v(O2)=0.01mol·L-1·min-1 |
| C.v(NO)=0.001mol·L-1·min-1 | D.v(H2O)=0.012mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验不能 达到实验目的的是
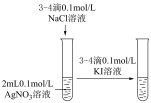 | 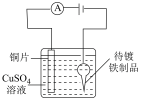 | 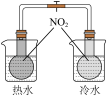 |  |
| A.验证AgCl溶解度大于AgI | B.电镀铜 | C.证明温度对平衡的影响 | D.验证Fe与水的反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在温度为T3、T4时,N2O4(g)⇌2NO2(g) ΔH>0,该平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
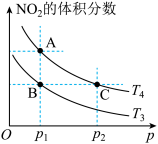

| A.A、C两点的反应速率:A>C | B.A、B两点N2O4的转化率:A<B |
| C.A、C两点气体的颜色:A浅,C深 | D.T3>T4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,以I2为催化剂,氯苯(C6H5Cl)和Cl2在CS2中发生平行反应,生成邻二氯苯和对二氯苯,其反应式为:
反应①C6H5Cl+Cl2 C6H4Cl2 (邻二氯苯)+HCl
C6H4Cl2 (邻二氯苯)+HCl 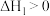
反应②C6H5Cl+Cl2 C6H4Cl2 (对二氯苯) +HCl
C6H4Cl2 (对二氯苯) +HCl 
反应①和②的速率方程分别为:① ;②
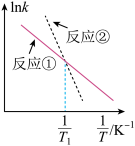
;② ;k为速率常数且只与温度有关。图为①和②的
;k为速率常数且只与温度有关。图为①和②的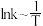 曲线。下列说法
曲线。下列说法不正确 的是
反应①C6H5Cl+Cl2
 C6H4Cl2 (邻二氯苯)+HCl
C6H4Cl2 (邻二氯苯)+HCl 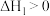
反应②C6H5Cl+Cl2
 C6H4Cl2 (对二氯苯) +HCl
C6H4Cl2 (对二氯苯) +HCl 
反应①和②的速率方程分别为:①
 ;②
;② ;k为速率常数且只与温度有关。图为①和②的
;k为速率常数且只与温度有关。图为①和②的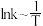 曲线。下列说法
曲线。下列说法
| A.若对二氯苯比邻二氯苯稳定,则∆H1>∆H2 |
B. (C6H5Cl)= (C6H5Cl)= (C6H4Cl2)(对二氯苯)+ (C6H4Cl2)(对二氯苯)+ (C6H4Cl2)(邻二氯苯) (C6H4Cl2)(邻二氯苯) |
| C.恒温恒容时,当体系中两种有机产物的浓度之比保持不变时说明反应达到平衡状态 |
| D.欲提高产物中对二氯苯的比例,可适当升高反应温度或改用选择性更高的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】恒温条件下的可逆反应:A(s)+2B(g)  2C(g)+D(g) △H<0,在甲容器充入2molA、2molB并保持压强不变,乙容器充入2molC、 1mol D并保持体积不变,起始时甲、乙两容器气体体积相等。为使平衡时两容器中B的浓度相等,下列措施不可行的是
2C(g)+D(g) △H<0,在甲容器充入2molA、2molB并保持压强不变,乙容器充入2molC、 1mol D并保持体积不变,起始时甲、乙两容器气体体积相等。为使平衡时两容器中B的浓度相等,下列措施不可行的是
 2C(g)+D(g) △H<0,在甲容器充入2molA、2molB并保持压强不变,乙容器充入2molC、 1mol D并保持体积不变,起始时甲、乙两容器气体体积相等。为使平衡时两容器中B的浓度相等,下列措施不可行的是
2C(g)+D(g) △H<0,在甲容器充入2molA、2molB并保持压强不变,乙容器充入2molC、 1mol D并保持体积不变,起始时甲、乙两容器气体体积相等。为使平衡时两容器中B的浓度相等,下列措施不可行的是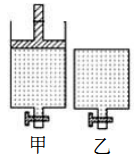
| A.乙容器中分离出一定量的D气体 |
| B.向甲谷器中再充入一定量的B气体 |
| C.将甲的活塞往下压至反应前的位置 |
| D.适当降低乙容器的温度 |
您最近一年使用:0次
【推荐2】某温度下密闭容器中发生反应2M(g)+N(g) 2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
 2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )
2E(g),若开始只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了10%;若开始只充入2 mol M和1 mol N混合气体,达平衡时M的转化率为( )| A.20% | B.60% | C.80% | D.90% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,反应: 的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
 的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是
的反应热和化学平衡常数分别为∆H和K,∆H<0,下列说法正确的是| A.升高温度,K增大 |
B.2molSO2和1molO2反应放出热量 |
C.其他条件不变,增大 的量,∆H和K均增大 的量,∆H和K均增大 |
D.相同温度时反应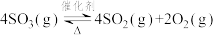 的反应热和化学平衡常数为-2∆H和 的反应热和化学平衡常数为-2∆H和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某学习小组在容积固定为2 L的密闭容器内充入1 mol N2和3 mol H2合成NH3。恒温下开始反应,并用压力传感器测定压强如下表所示:
下列说法不正确 的是
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
| A.不断地将NH3液化并移走,有利于反应正向进行 |
| B.其它条件不变,在30 min时,若压缩容器的体积,N2的平衡转化率增大 |
| C.从反应开始到10 min时,v(NH3)=0.035 mol·L−1·min−1 |
| D.在30 min时,再加入0.5 mol N2、1.5 mol H2和2 mol NH3,平衡向逆反应方向移动 |
您最近一年使用:0次

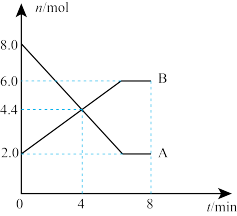


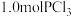 和
和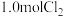 充入体积不变的1L密闭容器中,在一定条件下发生下述反应:
充入体积不变的1L密闭容器中,在一定条件下发生下述反应: 达到平衡时,
达到平衡时, 为
为 ,如果此时将
,如果此时将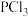 和
和 全部移走,在相同温度下再达平衡时
全部移走,在相同温度下再达平衡时

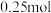
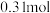
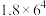 mol/L
mol/L

