某同学设计了如下实验方案探究化学反应速率的影响因素,下列有关说法错误的是
| 实验编号 | 温度/℃ | 硫酸 |  溶液 溶液 |
| ① | 25 | 2mL 0.01mol/L | 1mL 0.01mol/L |
| ② | 25 | 2mL 0.01mol/L | 1mL 0.02mol/L |
| ③ | 50 | 2mL 0.01mol/L | 1mL 0.02mol/L |
| A.实验中可通过记录溶液出现浑浊所需时间来判断反应速率的大小 |
| B.实验①②探究的是浓度对化学反应速率的影响 |
| C.实验①③探究的是温度对化学反应速率的影响 |
| D.实验③反应速率最快 |
更新时间:2021-11-04 16:56:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在密闭容器中进行反应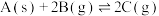
 ,逆反应的反应速率随时间变化的关系如图所示。下列有关说法正确的是
,逆反应的反应速率随时间变化的关系如图所示。下列有关说法正确的是

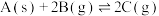
 ,逆反应的反应速率随时间变化的关系如图所示。下列有关说法正确的是
,逆反应的反应速率随时间变化的关系如图所示。下列有关说法正确的是
A. min时使用了催化剂 min时使用了催化剂 | B. min时一定降低了温度 min时一定降低了温度 |
C. min时反应向逆反应方向进行 min时反应向逆反应方向进行 | D.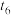 min时可能减小了生成物的浓度 min时可能减小了生成物的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列做法与调控化学反应速率无关 的是
| A.食盐中添加碘酸钾预防缺碘 | B.食物存放在冰箱里以保鲜食物 |
| C.在铁制品表面刷油漆防止生锈 | D.糕点包装内放置除氧剂延长保质期 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组用下图装置探究NaCl溶液对钢铁腐蚀的影响。

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
查阅资料:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。
下列说法不正确 的是:

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
| 实验 | a | b | 指针偏转方向 |
| Ⅱ | 0.1% | 0.01% | 向右 |
| Ⅲ | 0.1% | 3.5% | 向左 |
| Ⅳ | 3.5% | 饱和溶液 | 向右 |
下列说法
| A.实验Ⅰ加热后,指针发生偏转的原因可能是温度升高,Fe还原性增强,反应速率加快 |
| B.实验Ⅱ中b作正极 |
| C.甲同学由实验Ⅱ、Ⅲ、Ⅳ得出结论NaCl溶液的浓度越大,Fe越容易被腐蚀 |
| D.根据上述实验,对钢铁腐蚀有影响的因素是:温度、NaCl溶液的浓度、O2的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Ni可活化C2H6放出CH4,其反应历程如下图所示:
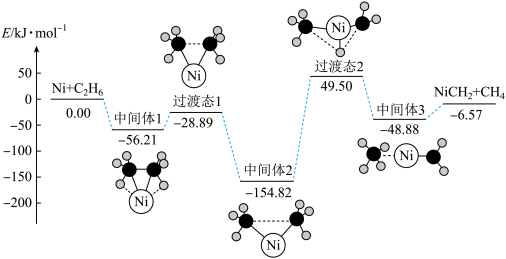
下列关于活化历程的说法正确的是

下列关于活化历程的说法正确的是
| A.决速步骤:中间体1→中间体2 | B.总反应为Ni+C2H6→NiCH2+CH4 |
| C.Ni−H键的形成对氢原子的迁移是不利的 | D.涉及非极性键的断裂和生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列生产或实验事实引出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 向5 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡,完全反应后,滴加 溶液,出现血红色 溶液,出现血红色 | 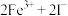  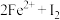 是可逆反应 是可逆反应 |
| B | 向淀粉-KI溶液中滴加氯水溶液变蓝色 | 氯水中含有次氯酸 |
| C | 其他条件相同, 溶液和 溶液和 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| D | 取 固体,溶解后滴加硝酸酸化的硝酸钡溶液,产生白色沉淀 固体,溶解后滴加硝酸酸化的硝酸钡溶液,产生白色沉淀 |  固体已变质 固体已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验设计不能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 验证牺牲阳极的阴极保护法 | 用Fe作被保护电极、Zn作辅助电极,以经过酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。一段时间后,取Fe电极区域的少量溶液于洁净试管中,滴加黄色 溶液 溶液 |
| B | 探究氯气与氢气的反应 | 在空气中点燃氢气,然后把导管缓缓伸入盛满氯气的集气瓶中 |
| C | 制备乙酸乙酯 | 在一支试管中加入2mL浓硫酸,然后边振荡试管边缓慢加入2mL乙醇和3mL乙酸,连接好装置,加热,将产生的蒸气经导管通到饱和 溶液的液面下 溶液的液面下 |
| D | 探究浓度对化学反应速率的影响 | 取编号为①、②的两支试管,各加入4mL 的酸性KMnO4溶液,然后向①试管中加入2mL 的酸性KMnO4溶液,然后向①试管中加入2mL 的 的 溶液;向②试管中加入2mL 溶液;向②试管中加入2mL 的 的 溶液,分别记录溶液褪色所需的时间 溶液,分别记录溶液褪色所需的时间 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】100mL6mol/LH2SO4跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量。可向反应物中加入适量的
| A.碳酸钠(固体) | B.水 | C.硫酸铜溶液 | D.硝酸钾(固体) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.1g水蒸气→1g液态水→1g冰,熵依次增加 |
| B.通过改变条件使可逆反应正向移动,反应物的转化率一定增大 |
| C.反应物浓度增大,单位体积内活化分子数增多,反应速率增大 |
| D.升高温度可降低化学反应的活化能,提高活化分子百分数,加快化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向两个体积相同的恒容密闭容器中各充入一定量X(g),发生反应X(g)⇌2Y(g) ΔH>0,一段时间后达到平衡。已知反应速率v正=k正c(X),v逆=k逆c2(Y),其中k正、k逆分别为正、逆反应的速率常数。只受温度影响。反应过程中X(g)的浓度随时间变化如图所示,下列说法正确的是


| A.T1>T2 |
| B.a点时v正大于b点时v逆 |
C.c点时,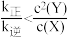 |
| D.若对原平衡体系减压,重新达到平衡时c(Y)将增大 |
您最近一年使用:0次

 酸性
酸性 溶液于两支试管中,分别加入10mL
溶液于两支试管中,分别加入10mL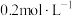
 的集气瓶
的集气瓶 溶液,再滴加少量碘水
溶液,再滴加少量碘水 和
和 溶液的
溶液的
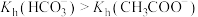
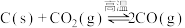 ,下列有关说法正确的是
,下列有关说法正确的是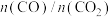 不再随时间而变化
不再随时间而变化

