已知25℃时有关弱酸的电离平衡常数如下表所示,则下列有关说法不正确的是
| 弱酸化学式 |  | HCN |  |
| 电离平衡常数 | 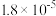 |  |  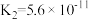 |
A.等物质的量浓度的各溶液pH关系为: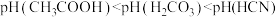 |
| B.0.1mol/L的醋酸溶液加水稀释,其电离程度增大 |
C.NaCN中通入少量CO2发生的化学反应为: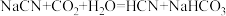 |
D. 的电离常数表达式: 的电离常数表达式: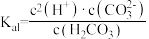 |
更新时间:2021-11-08 08:51:08
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】若将pH=2的酸溶液和pH=12的NaOH溶液等体积混和。混和液中的pH值为 ( )
| A.等于7 | B.大于等于7 | C.小于等于7 | D.无法判断 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定温度下,冰醋酸稀释过程中溶液的导电能力变化如图所示。下列说法错误的是
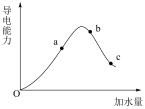

| A.加水前导电能力约为零的原因是冰醋酸中几乎没有自由移动的离子 |
| B.a、b、c三点对应的溶液中,CH3COOH电离程度最大的是c |
| C.a、b、c三点对应的溶液中,c(H+)由小到大的顺序是c<a<b |
| D.在b点加入浓硫酸,可使溶液中c(CH3COO-)增大、c(H+)增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】羟胺( )稀溶液中
)稀溶液中 的电离方程式为
的电离方程式为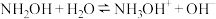 ,设
,设 的电离平衡常数为K。下列说法正确的是
的电离平衡常数为K。下列说法正确的是
 )稀溶液中
)稀溶液中 的电离方程式为
的电离方程式为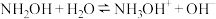 ,设
,设 的电离平衡常数为K。下列说法正确的是
的电离平衡常数为K。下列说法正确的是| A.常温下,加入少量NaOH固体,平衡向左移动,K减小 |
B.常温下,加入少量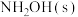 ,平衡向右移动, ,平衡向右移动, 的电离度增大 的电离度增大 |
| C.常温下,加少量水稀释,溶液中所有离子浓度都减小 |
D.常温下,通入少量HCl气体,平衡向右移动, 增大 增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列图象正确的是
A.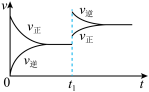 反应的正方向放热 反应的正方向放热 时升温 时升温 |
B.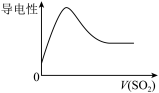  气体通入氯水中 气体通入氯水中 |
C. NaOH溶液滴加 NaOH溶液滴加 溶液中 溶液中 |
D.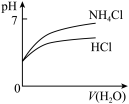 将pH相同的 将pH相同的 溶液和稀盐酸稀释时PH的变化 溶液和稀盐酸稀释时PH的变化 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】剧毒物氰化钠(NaCN)固体遇水或酸生成剧毒易燃的HCN气体,同时HCN又能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如表:
下列说法错误的是
| 弱酸 | HCOOH | HCN | H2S |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=1.3×10-7 |
| Ka2=7.1×10-15 |
| A.中和等体积、等浓度的 HCOOH 溶液和HCN溶液消耗NaOH的物质的量相等 |
| B.HCOO-、CN-、HS-在溶液中可以大量共存 |
| C.等体积、pH均为4的HCOOH和HCN的溶液分别与足量的锌粉反应,HCN放出的H2少 |
| D.等体积、pH均为4的HCOOH和HCN溶液均用水稀释100倍后,HCOOH的pH比HCN的大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将颗粒、大小相同的锌分别投入等体积、等pH的HA溶液和盐酸中 | HA溶液中产生气泡的速率比盐酸快 | 等浓度、等体积时溶液的酸性:HA>盐酸 |
| B | 常温下,将pH计置于 醋酸溶液中 醋酸溶液中 | pH计读数为2.9 | 醋酸是弱酸 |
| C | 将 溶液加入盛有2 mL浓度均为 溶液加入盛有2 mL浓度均为 的NaCl和NaI混合溶液的试管中 的NaCl和NaI混合溶液的试管中 | 混合溶液中出现黄色沉淀 | 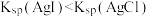 |
| D | 常温下,将滴有几滴酚酰试液的饱和碳酸钠溶液加热到50℃ | 溶液颜色加深,并产生大量气泡 |  的水解平衡正向移动 的水解平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A. 醋酸溶液加水稀释后, 醋酸溶液加水稀释后, 减小,醋酸的电离程度增大 减小,醋酸的电离程度增大 |
B.同温度下, 醋酸溶液 醋酸溶液 , , 醋酸溶液 醋酸溶液 ,则 ,则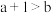 |
C.常温下,pH=2和pH=12的两种溶液等体积混合后,溶液中 的物质的量浓度一定等于 的物质的量浓度一定等于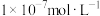 |
D. 溶液中: 溶液中: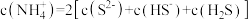 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,关于下列溶液说法中正确的是
A.向浓度为0.1mol/L的NaClO溶液中加入NaClO固体,溶液中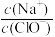 将增大 将增大 |
| B.向0.1mol/L的NH4Cl溶液中加水,溶液中所有离子的浓度均减小 |
| C.pH相等的NaF与CH3COOK溶液中,c(Na+)+c(CH3COO-)=c(K+)+c(F-) |
D.向NaHSO3溶液中加入少量的I2,溶液中 将减小 将减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列粒子浓度关系错误的是

A.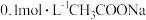 溶液中: 溶液中: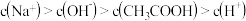 |
B. 的 的 和 和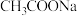 混合溶液中: 混合溶液中: |
C.将 溶液与 溶液与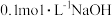 溶液等体积混合: 溶液等体积混合: |
D.向 溶液中通入 溶液中通入 至中性: 至中性: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱酸盐和弱酸”组成的缓冲溶液,其中存在pH=pKa-lg 。25℃时,用 0.1 mol·L-1的NaOH溶液滴定16.00 mL某未知浓度的HA溶液,滴定过程中消耗 NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pKa=-lgKa,100.48=3,酸性 HA>HCN)。下列说法错误的是
。25℃时,用 0.1 mol·L-1的NaOH溶液滴定16.00 mL某未知浓度的HA溶液,滴定过程中消耗 NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pKa=-lgKa,100.48=3,酸性 HA>HCN)。下列说法错误的是
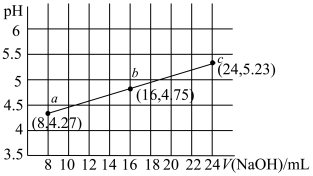
 。25℃时,用 0.1 mol·L-1的NaOH溶液滴定16.00 mL某未知浓度的HA溶液,滴定过程中消耗 NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pKa=-lgKa,100.48=3,酸性 HA>HCN)。下列说法错误的是
。25℃时,用 0.1 mol·L-1的NaOH溶液滴定16.00 mL某未知浓度的HA溶液,滴定过程中消耗 NaOH溶液的体积与混合溶液pH之间的关系如图所示(已知:pKa=-lgKa,100.48=3,酸性 HA>HCN)。下列说法错误的是
| A.HA电离常数的数量级为10-5 |
| B.b点溶液中存在 c(A-)+c(OH-)=c(Na+ )+c(H+) |
| C.c点溶液中离子浓度的大小关系为 c(A- )>c(HA)>c(H+)>c(OH-) |
| D.若将HA改为等体积等浓度的 HCN,则pH随NaOH溶液体积的变化曲线竖直下移 |
您最近半年使用:0次

 转化为
转化为 ,再氧化成
,再氧化成 。已知
。已知 的电离常数
的电离常数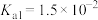 ,
, ,
, 的电离常数
的电离常数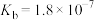 。下列说法正确的是
。下列说法正确的是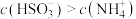
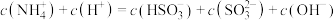
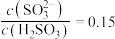 时,溶液的
时,溶液的



