由下列实验操作及现象能得出相应结论的是
| 实验操作 | 现象 | 结论 | |
| A | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
| B | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| C | 用pH计测定pH: ①NaHCO3溶液②CH3COONa溶液 | pH:①>② | H2CO3酸性弱于CH3COOH |
| D | 将一块未经打磨的铝片剪成相同的两小片,相同温度下分别投入5.0mL浓度均为2.0 mol∙L−1的CuSO4溶液和CuCl2溶液中 | CuSO4溶液中无明显现象;CuCl2溶液中反应剧烈,铝片表面有红色物质生成 | 则Cl-能加速破坏铝片表面的氧化膜 |
| A.A | B.B | C.C | D.D |
更新时间:2021-11-03 22:57:59
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】溴、碘均为卤族元素,下列关于溴、碘说法错误的是
| A.将F2分别通入到NaBr溶液和NaI溶液中,可以得到溴单质和碘单质 |
| B.通常将KIO3固体添加到食盐中来制作加碘盐 |
| C.溴单质和碘单质在四氯化碳中的溶解度均大于它们在水中的溶解度 |
| D.碘酒可以使淀粉碘化钾试纸变蓝 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图:
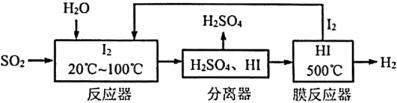
下列说法正确的是

下列说法正确的是
| A.H2、I2、H2O都属于非极性分子 |
| B.分离器中的物质分离的操作为分液 |
| C.碘循环工艺的总反应为2SO2+4H2O+I2=H2+2H2SO4+2HI |
| D.反应器中控制温度为20℃~100℃,温度过高会使I2升华,减少SO2的吸收 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列反应的离子方程式正确的是
| A.反萃取时向碘的CCl4溶液中加入浓NaOH溶液: I2+2OH-=I- +IO- +H2O |
| B.海带提碘时加H2O2氧化I-: 2I-+H2O2=I2+2OH- |
C.用淀粉KI试纸和食醋检验加碘盐中是否含有碘:5I-+IO +6CH3COOH=3I2+ 3H2O+ 6CH3COO- +6CH3COOH=3I2+ 3H2O+ 6CH3COO- |
| D.在氢氟酸中加入石英: SiO2+4H++ 4F-=SiF4↑+2 H2O |
您最近一年使用:0次
【推荐1】下列实验装置不能达到实验目的的是
| A | B | C | D |
 | 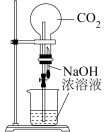 | 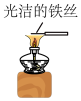 |  |
| 验证Na和水的反应是否为放热反应 | 用 做喷泉实验 做喷泉实验 | 观察纯碱的焰色反应 | 比较 、 、 的稳定性 的稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
| A.利用原子光谱上的特征谱线来鉴定元素,称为光谱分析 |
| B.焰色试验是与电子跃迁有关的物理现象 |
| C.用X射线衍射摄取玻璃和金刚石得到的图谱是相同的 |
| D.红外光谱可测定分子中官能团和化学键的信息 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】2022年度诺贝尔化学奖授予发现“点击化学(通过小单元的拼接,来快速可靠地完成形形色色分子的化学合成)和生物正交化学”的三位科学家。点击化学的概念对化学合成领域有很大的贡献。点击化学的原理如图所示。下列说法错误 的是
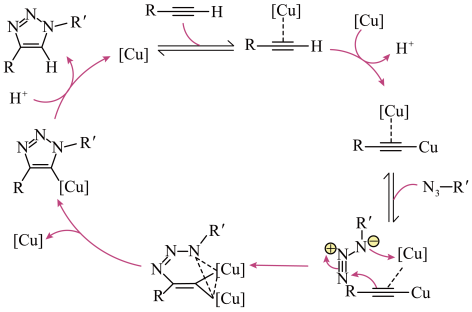

A.基态 的价电子排布式为 的价电子排布式为 |
B.中间产物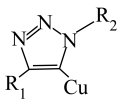 中N均采取 中N均采取 杂化 杂化 |
| C.该过程总反应的原子利用率为100% |
| D.铜改变了反应历程,但不改变总反应的焓变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】工业制硫酸的一步重要反应为 ,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,下列有关说法错误的是
,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,下列有关说法错误的是
 ,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,下列有关说法错误的是
,这是一个正反应放热的可逆反应。如果该反应在密闭容器中进行,下列有关说法错误的是| A.使用催化剂是为了增大反应速率,提高生产效率 |
B.提高反应时的温度,可以实现 的完全转化 的完全转化 |
| C.通过调控反应条件,可以提高该反应进行的程度 |
| D.在给定条件下,达到平衡时该反应完成程度达到最大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列离子不发生水解的是
| A.CO32- | B.CH3COO- | C.Cl- | D.Al3+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是
A. 的醋酸溶液和 的醋酸溶液和 的醋酸溶液,醋酸浓度前者是后者的10倍 的醋酸溶液,醋酸浓度前者是后者的10倍 |
B.升高温度, 盐溶液的 盐溶液的 减小,说明 减小,说明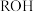 一定是弱电解质 一定是弱电解质 |
C. 氢氧化钠溶液与 氢氧化钠溶液与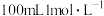 硫酸充分混合后,溶液 硫酸充分混合后,溶液 一定等于7 一定等于7 |
D. 的 的 溶液中加入少量 溶液中加入少量 晶体, 晶体, 水解程度增大,但溶液的 水解程度增大,但溶液的 减小 减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】NA代表阿伏加德罗常数的值,下列说法不正确 的是
| A.过氧化钠与水反应生成2.24LO2(标况下)时转移的电子数为0.2NA |
| B.100mL1mol·L-1FeCl3溶液中所含Fe3+的数目为0.1NA |
| C.密闭容器中23gNO2与N2O4的混合气体中氮原子数为0.5NA |
| D.常温常压下,124gP4中所含P—P键数目为6NA |
您最近一年使用:0次

 。下列说法错误的是
。下列说法错误的是

