化工生产中常用FeS作为沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+FeS(s) CuS(s)+Fe2+(aq),下列说法错误的是
CuS(s)+Fe2+(aq),下列说法错误的是
 CuS(s)+Fe2+(aq),下列说法错误的是
CuS(s)+Fe2+(aq),下列说法错误的是| A.FeS的Ksp比CuS的Ksp大 |
| B.该反应达到平衡时c(Fe2+)=c(Cu2+) |
| C.往平衡体系中加入少量CuSO4固体后,c(Fe2+)变大 |
D.该反应的平衡常数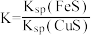 |
21-22高二上·重庆渝中·期中 查看更多[3]
更新时间:2021-11-27 08:44:29
|
相似题推荐
【推荐1】几种难溶电解质的溶度积常数(25℃)如下,下列说法不正确的是
| 难溶电解质 | AgCl | AgBr |  |
| Ksp |  |  | 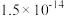 |

| A.Ksp与难溶电解质的性质、温度有关 |
B.由上述数据可知,溶解度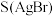 <S(Ag2SO3) <S(Ag2SO3) |
| C.在一定条件下,可实现AgCl转化为AgBr |
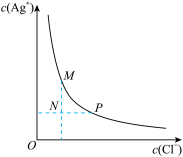
| D.AgCl在水中的沉淀溶解平衡曲线如图所示,向N点溶液中加入NaCl固体,能使溶液由N点变到M点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.25℃时,pH=2的硫酸与pH=12的NaOH溶液等体积混合溶液显酸性 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
| C.相同温度下,相同浓度的NH4Cl溶液与(NH4)2SO4溶液pH前者小于后者 |
| D.相同温度下,足量的氯化银固体分别溶于相同浓度的盐酸和氯化镁溶液中,Ag+的浓度:前者大于后者 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】由实验操作和现象,可得出相应正确结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 在50mL的注射器里充入20mLNO和10mLO2 再吸入5mL水,气体由无色变为红棕色,再变为无色 | 注射器内最后剩余气体为NO |
| B | 向酸性KMnO₄溶液中通入SO2,溶液紫色褪去 | SO2具有漂白性 |
| C | 向未知溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成 | 未知溶液中一定含有 |
| D | 向MgCl2溶液中滴加少量NaOH溶液,生成白色沉淀 再滴加FeCl3溶液,沉淀变为红褐色 | 溶解度:Mg(OH) 2<Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向等物质的量浓度的ZnSO4和CuSO4的混合溶液中,逐滴加入1.5 mol·L−1的Na2S溶液直至溶液中无沉淀产生,然后过滤。已知:Ksp(ZnS)=2.0×10−22,Ksp(CuS)=1.3×10−36。下列说法不正确的是
| A.先生成CuS后生成ZnS沉淀,属于沉淀的转化 |
B.当ZnS沉淀完全时,溶液中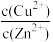 =6.5×10−15 =6.5×10−15 |
| C.过滤得到的沉淀是CuS和ZnS的混合物 |
| D.过滤后得到的溶液中仍有极少量的Cu2+和Zn2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
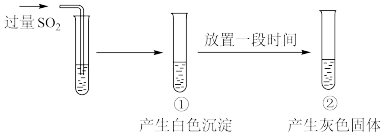
经检验,白色沉淀为 ;灰色固体中含有
;灰色固体中含有 。
。
下列说法错误的是
 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
经检验,白色沉淀为
 ;灰色固体中含有
;灰色固体中含有 。
。下列说法错误的是
A.①中生成白色沉淀的离子方程式为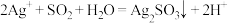 |
B.①中未生成 ,证明溶度积: ,证明溶度积: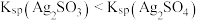 |
C.放置一段时间②中产生灰色固体是因为过量的 将部分 将部分 还原。 还原。 |
D.该实验条件下, 与 与 反应生成 反应生成 的速率大于生成 的速率大于生成 的速率 的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知Ksp(AgCl)=2×10-10,Ksp(AgI)=9×10-17。下列说法不正确 的是
| A.向0.01 mol∙L-1 AgNO3溶液中加入等体积0.01 mol∙L-1 NaCl溶液,有沉淀生成 |
| B.AgCl固体在0.01 mol∙L-1 MgCl2溶液中的溶解度小于在0.01 mol∙L-1 NaCl溶液中 |
| C.向浓度均为0.01 mol∙L-1的NaCl和KI混合溶液中逐滴滴加0.01 mol∙L-1 AgNO3溶液,开始时先析出黄色沉淀 |
| D.向AgCl固体中加入少量0.01 mol∙L-1 KI溶液,达新平衡时溶液中存在等式:c(Cl-)=c(I-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】二元有机酸(H2X)的电离常数Kal=1.67×10﹣8、Ka2=3.34×10﹣17。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中c2(H+)与c2(Ba2+)的关系如图所示。下列说法不正确的是
已知:HY是一元强酸,BaY2易溶于水。0.382=0.1444,0.192=0.0361
已知:HY是一元强酸,BaY2易溶于水。0.382=0.1444,0.192=0.0361

| A.NaHX溶液显碱性 |
| B.溶度积Ksp(BaX)=6.18×10﹣23mol2⋅L﹣2 |
| C.b点:2c(Ba2+)+c(H+)=2c(X2﹣)+c(HX﹣)+c(OH﹣) |
| D.若0.1 mol BaX溶于25 mLx mol⋅L﹣1HY溶液中得到c点溶液,则x≈8.38 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,用0.10mol·L-1NaOH溶液滴定40mL0.025mol·L-1CuSO4和0.025mol·L-1MgCl2的混合溶液(含有少量抑制金属离子水解的硫酸),pH变化曲线如图所示[已知:Cu(OH)2和Mg(OH)2的Ksp分别为2.2×10-20、5.6×10-12,当c(X2+)≤10-5mol·L-1时认为X2+沉淀完全,lg22=1.34,1g56=1.75]。下列说法错误的是
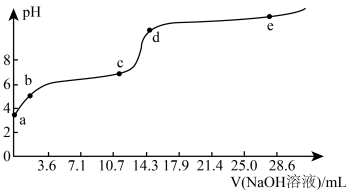

| A.a~b段主要发生反应:H++OH-=H2O |
| B.c点时,溶液的pH=7.34 |
| C.能通过调节pH分离Cu2+和Mg2+ |
| D.d~e段生成的沉淀为Mg(OH)2 |
您最近一年使用:0次

 Ca2+(aq)+2OH—(aq),当向此悬浊液中加入少量生石灰时,始终保持温度不变,则下列说法正确的是
Ca2+(aq)+2OH—(aq),当向此悬浊液中加入少量生石灰时,始终保持温度不变,则下列说法正确的是
 ×10-4
×10-4

