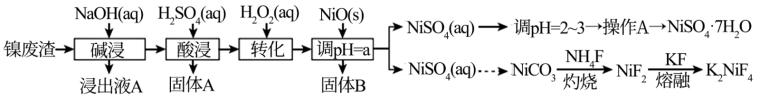
“翠矾”(NiSO4·7H2O)在印染工业作媒染剂,生产酞菁艳蓝络合剂;氟镍化钾(K2NiF4)是结构化学研究的热点物质。以镍废渣(主要成分为Ni,含少量Fe、Al、Fe3O4、Al2O3和不溶性杂质等)为原料合成“翠矾”和氟镍化钾的流程如下:
几种金属离子的氢氧化物沉淀pH如表:
请回答下列问题:
(1)“碱浸”过程中,为提高浸出率,可采取的措施是___________ (写一种即可)。
(2)“转化”过程中加入H2O2的目的是___________ (用离子方程式表示),经实验测定该过程温度高于40℃,转化率急速降低的原因可能是______________________ 。
(3)调节pH=a,其中a的取值范围是___________ 。
(4)写出“灼烧”NiCO3和NH4F的混合物时的化学反应方程式:___________ ,为避免污染环境,选择下列装置吸收尾气,最宜选择___________ (填选项)。
A.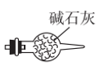 B.
B.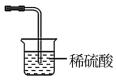
C.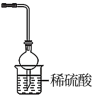 D.
D.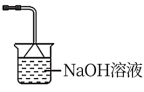

几种金属离子的氢氧化物沉淀pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 5.2 |
| Fe2+ | 7.6 | 9.7 |
| Ni2+ | 7.1 | 9.2 |
(1)“碱浸”过程中,为提高浸出率,可采取的措施是
(2)“转化”过程中加入H2O2的目的是
(3)调节pH=a,其中a的取值范围是
(4)写出“灼烧”NiCO3和NH4F的混合物时的化学反应方程式:
A.
 B.
B.
C.
 D.
D.
更新时间:2021-11-05 18:00:50
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使CO2转化为CH4。反应体系中主要反应的热化学方程式为:
反应Ⅰ:

反应Ⅱ:

(1)将反应后气体通入___________ (填试剂),可证明反应Ⅱ发生。
(2)计算

___________ (用 和
和 表示)。
表示)。
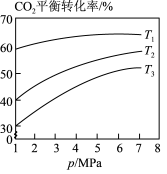
(3)相同投料比时,体系内 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为___________ 。
(4)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:
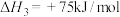
消碳反应:
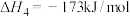
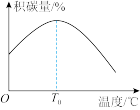
其他条件相同时,催化剂表面积碳量与温度的关系如图所示, ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是___________ 。
(5)向 恒容、密闭容器中通入
恒容、密闭容器中通入 和
和 ,测得有关物质的物质的量随温度变化如下图。
,测得有关物质的物质的量随温度变化如下图。
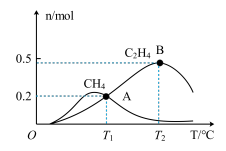
①催化剂在较低温度时主要选择___________ (填“反应Ⅰ”或“反应Ⅱ”)。
② 时
时 的转化率为
的转化率为___________ ,反应Ⅰ的平衡常数
___________ 。
反应Ⅰ:


反应Ⅱ:


(1)将反应后气体通入
(2)计算


 和
和 表示)。
表示)。(3)相同投料比时,体系内
 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
(4)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:

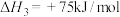
消碳反应:

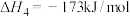
其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
 ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是
(5)向
 恒容、密闭容器中通入
恒容、密闭容器中通入 和
和 ,测得有关物质的物质的量随温度变化如下图。
,测得有关物质的物质的量随温度变化如下图。
①催化剂在较低温度时主要选择
②
 时
时 的转化率为
的转化率为
您最近一年使用:0次
【推荐2】某化工厂产生的废渣中含有PbSO4和Ag,为了回收这两种物质,某同学设计了如图过程:
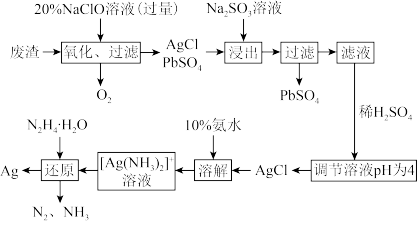
(1)写出NaClO的电子式____ 。
(2)“氧化”阶段需在80℃条件下进行,写出将废渣“氧化”的化学方程式____ 。
(3)已知:①“浸出”过程发生可逆反应:AgCl(s)+2SO (aq)
(aq) Ag(SO3)
Ag(SO3)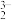 (aq)+Cl-(aq)。
(aq)+Cl-(aq)。
②浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如图。

①由图可知,pH=10时,浸出液中含银化合物总浓度随含硫化合物总浓度的增大而____ (填“增大”、“减小”或“基本不变”),产生该变化的原因是_____ 。
②依题意分析,下列说法合理的是____ 。
A.“浸出”过程中的反应平衡常数表达式为K=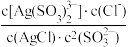
B.若“浸出”过程在敞口容器中进行,浸出时间过长会导致银的浸出率降低
C.pH=5时,随着含硫化合物总浓度的增大,浸出液中含银化合物总浓度基本不变
(4)“还原”阶段氧化产物与还原产物的物质的量之比为_____ 。

(1)写出NaClO的电子式
(2)“氧化”阶段需在80℃条件下进行,写出将废渣“氧化”的化学方程式
(3)已知:①“浸出”过程发生可逆反应:AgCl(s)+2SO
 (aq)
(aq) Ag(SO3)
Ag(SO3)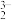 (aq)+Cl-(aq)。
(aq)+Cl-(aq)。②浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如图。

①由图可知,pH=10时,浸出液中含银化合物总浓度随含硫化合物总浓度的增大而
②依题意分析,下列说法合理的是
A.“浸出”过程中的反应平衡常数表达式为K=
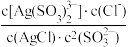
B.若“浸出”过程在敞口容器中进行,浸出时间过长会导致银的浸出率降低
C.pH=5时,随着含硫化合物总浓度的增大,浸出液中含银化合物总浓度基本不变
(4)“还原”阶段氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)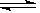 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)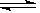 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)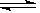 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=_______ kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_______ 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=_________ 。(保留2位小数)
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)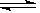 CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH_____ 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是___________________________________ 。
(1)已知:2SO2(g)+O2(g)
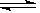 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-12NO(g)+O2(g)
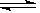 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1则反应NO2(g)+SO2(g)
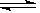 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
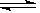 CH3OH(g)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在反应原理部分,我们经常以H2和I2的反应为例来研究化学反应速率和平衡。
(1)在2L的容器中充入H2、I2各1mol,对于反应:H2(g)+I2(g) 2HI(g),在323K和343K时H2的转化率随时间变化的结果如图所示。
2HI(g),在323K和343K时H2的转化率随时间变化的结果如图所示。
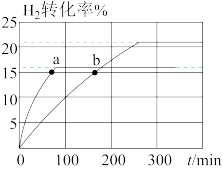
①323K时反应的平衡转化率 =
=__________ %。平衡常数K=____________ (保留2位小数)。
②在343K时,要提高I2转化率,可采取的措施是____ ( 答出两条);要缩短反应达到平衡的时间,可采取的措施有___ ( 答出两条)。
③比较a、b处反应速率大小:v(a)____ v(b)(填 “大于”“小于”或“等于”)。反应速率v正=k正x(H2)x(I2),v逆=k逆x2(HI),k正、 k逆分别为正、逆反应速率常数[k逆(323)=5,k逆(343)=7],x为物质的量分数,计算b处v正=________ mol/(L ∙ min)(保留1位小数)。
(2)对于反应:H2(g)+I2(g) 2HI(g)提出如下反应历程
2HI(g)提出如下反应历程
第一步:I2 I+I(快速平衡)
I+I(快速平衡)
第二步:H2+2I→2HI (慢反应)
其中可近似认为第二步反应不影响第一步的平衡。 下列表述正确的是______ ( 填字母序号)。
a.v(第一步的逆反应)<v(第二步的逆反应)
b.反应的中间产物只有I
c.第二步反应活化能较低
d.第二步中H2与I的碰撞仅部分有效
(3)已知反应2HI(g) H2(g)+I2(g)的能量变化如图所示,则1molHI(g)分子中化学键断裂时需吸收的能量为
H2(g)+I2(g)的能量变化如图所示,则1molHI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(1)在2L的容器中充入H2、I2各1mol,对于反应:H2(g)+I2(g)
 2HI(g),在323K和343K时H2的转化率随时间变化的结果如图所示。
2HI(g),在323K和343K时H2的转化率随时间变化的结果如图所示。
①323K时反应的平衡转化率
 =
=②在343K时,要提高I2转化率,可采取的措施是
③比较a、b处反应速率大小:v(a)
(2)对于反应:H2(g)+I2(g)
 2HI(g)提出如下反应历程
2HI(g)提出如下反应历程第一步:I2
 I+I(快速平衡)
I+I(快速平衡)第二步:H2+2I→2HI (慢反应)
其中可近似认为第二步反应不影响第一步的平衡。 下列表述正确的是
a.v(第一步的逆反应)<v(第二步的逆反应)
b.反应的中间产物只有I
c.第二步反应活化能较低
d.第二步中H2与I的碰撞仅部分有效
(3)已知反应2HI(g)
 H2(g)+I2(g)的能量变化如图所示,则1molHI(g)分子中化学键断裂时需吸收的能量为
H2(g)+I2(g)的能量变化如图所示,则1molHI(g)分子中化学键断裂时需吸收的能量为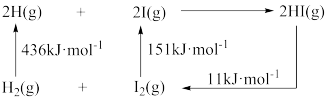
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】卤代烯烃是合成塑料的重要原料,研究合成卤代烯烃具有重要意义。T℃时,在10L的密闭容器中充入1mol2—丁炔(CH3—C≡C—CH3,可用X表示)和1molHCl,以Al2O3为催化剂发生如下反应:
Ⅰ.
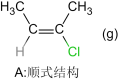 ΔH=akJ/mol(a<0)
ΔH=akJ/mol(a<0)
Ⅱ.
 ΔH=bkJ/mol(b<0)
ΔH=bkJ/mol(b<0)
已知B比A更稳定,且产物A、B在混合物中的物质的量随时间变化如图一所示。试回答下列问题。

(1)发生反应I、Ⅱ的同时,还有反应A转化为B,且焓变为△H'。则△H'_ 0(填“>”、“<”或“=”)。
(2)①从反应开始至20min时生成B的平均速率v(B)=___ ;
②反应至20min时CH3—C≡C—CH3的转化率=__ ;
③在T℃时,反应I的平衡常数为__ 。
(3)T℃时,E1和E2分别代表反应I,Ⅱ的正反应活化能。
①由图一得出:E1__ E2(填“>”、“<”或“;”);
②试从反应方向的角度分析,20min后A的物质的量减小的原因__ 。
(4)其它条件相同时,测出生成A、B的速率随温度变化如图二所示,则提高B在较低温度下产率的措施是__ 。
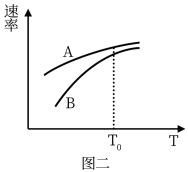
Ⅰ.

 ΔH=akJ/mol(a<0)
ΔH=akJ/mol(a<0)Ⅱ.

 ΔH=bkJ/mol(b<0)
ΔH=bkJ/mol(b<0)已知B比A更稳定,且产物A、B在混合物中的物质的量随时间变化如图一所示。试回答下列问题。

(1)发生反应I、Ⅱ的同时,还有反应A转化为B,且焓变为△H'。则△H'
(2)①从反应开始至20min时生成B的平均速率v(B)=
②反应至20min时CH3—C≡C—CH3的转化率=
③在T℃时,反应I的平衡常数为
(3)T℃时,E1和E2分别代表反应I,Ⅱ的正反应活化能。
①由图一得出:E1
②试从反应方向的角度分析,20min后A的物质的量减小的原因
(4)其它条件相同时,测出生成A、B的速率随温度变化如图二所示,则提高B在较低温度下产率的措施是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属钼具有高强度、高熔点、耐腐蚀、耐研磨等优点,主要作为钢的添加剂。工业上常用钼精矿(主要成分是 ,含有钙、硅等元素)制备金属钼,其中用氧化焙烧法提取钼的工艺流程如图:
,含有钙、硅等元素)制备金属钼,其中用氧化焙烧法提取钼的工艺流程如图:

已知:①焙烧后得到 、
、 、
、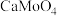 的混合物。
的混合物。
② 溶于氨水,钼酸钙(
溶于氨水,钼酸钙(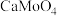 )不溶于氨水。
)不溶于氨水。
回答下列问题:
(1)“焙烧”产物中Mo元素的化合价为___________ 。尾气的主要成分为___________ 。
(2)“氨浸”过程中相关反应的离子方程式为___________ 。
(3)“氨浸”操作中,温度不宜过高,原因在于___________ 。其他条件一定时,钼的浸出率与氨浸温度、时间的关系如下图所示。“氨浸”条件宜采用___________ 。
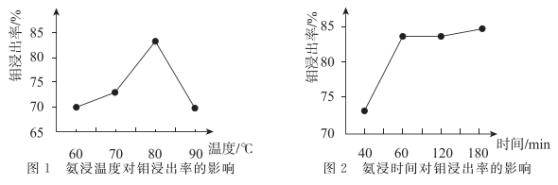
(4)“沉淀转溶”过程所得滤渣②的成分为___________ 。
(5)“沉钼”过程中发生反应的离子方程式为___________ 。
(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如下图。电解过程中阳极上发生的电极反应式为___________ 。

 ,含有钙、硅等元素)制备金属钼,其中用氧化焙烧法提取钼的工艺流程如图:
,含有钙、硅等元素)制备金属钼,其中用氧化焙烧法提取钼的工艺流程如图:
已知:①焙烧后得到
 、
、 、
、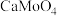 的混合物。
的混合物。②
 溶于氨水,钼酸钙(
溶于氨水,钼酸钙(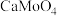 )不溶于氨水。
)不溶于氨水。回答下列问题:
(1)“焙烧”产物中Mo元素的化合价为
(2)“氨浸”过程中相关反应的离子方程式为
(3)“氨浸”操作中,温度不宜过高,原因在于

(4)“沉淀转溶”过程所得滤渣②的成分为
(5)“沉钼”过程中发生反应的离子方程式为
(6)电氧化法是一种极具发展前景的钼精矿冶金工艺,其工作原理如下图。电解过程中阳极上发生的电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:
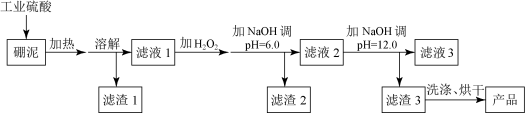
已知某些氢氧化物沉淀的pH如下表所示:
(1)MgO的电子式为__________ 。
(2)滤渣2的主要成分是__________ 。向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 ____________________________________ 。
(3)检验滤渣3是否洗涤干净的方法是______________________________________ 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为______________________________ 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为__________ (用含有a,b的代数式表示)。

已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | 开始沉淀的pH | 完全沉淀的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
(1)MgO的电子式为
(2)滤渣2的主要成分是
(3)检验滤渣3是否洗涤干净的方法是
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上以软锰矿(主要成分为MnO2,另含有少量FeCO3、Al2O3、SiO2)为原料制取金属锰的工艺流程如下:
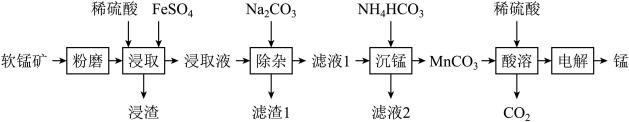
已知:Ⅰ.Mn(OH)2开始沉淀pH为8.3,完全沉淀pH为9.8。
Ⅱ.MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100 ℃开始分解。
(1)“粉磨”软锰矿的目的是______ 。
(2)“浸取液”经检测无Fe2+,“浸取”加入FeSO4作用是______ (用离子方程式表示)。
(3)“浸渣”的主要成分是______ 。
(4)“沉锰”中,不能用Na2CO3代替 NH4HCO3,其原因是______ ,得到纯净MnCO3的操作方法是:过滤、______ 。
(5)“沉锰”中,298 K、c(Mn2+)为1.05 mol·L−1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示。根据图中信息得出的结论是______ 。


已知:Ⅰ.Mn(OH)2开始沉淀pH为8.3,完全沉淀pH为9.8。
Ⅱ.MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100 ℃开始分解。
(1)“粉磨”软锰矿的目的是
(2)“浸取液”经检测无Fe2+,“浸取”加入FeSO4作用是
(3)“浸渣”的主要成分是
(4)“沉锰”中,不能用Na2CO3代替 NH4HCO3,其原因是
(5)“沉锰”中,298 K、c(Mn2+)为1.05 mol·L−1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示。根据图中信息得出的结论是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碘化亚铜(CuI)是一种白色固体,见光易分解变成棕黄色,不溶于水和乙醇,常用作有机反应催化剂、阳极射线管覆盖物、动物饲料添加剂等。某小组同学以冰铜(Cu2S 和FeS熔体)为原料制备无水CuI的流程如图。

(1)“调节pH”所用试剂为_______ ;若加入该试剂前溶液中阳离子浓度均为0.1mol/L,为使某阳离子完全沉淀为固体A,通过操作I与其它阳离子分离,理论上应调节溶液的pH在_______ 之间(常温下,Cu(OH)2、Fe(OH)3 的Ksp分别约为1×10-21和1×10 -38)。
(2)加入过量KI溶液时发生反应的离子方程式为_______ 。
(3)取CuI样品m g,加适量的FeCl3溶液恰好使其溶解,CuI 被完全氧化生成Cu2+和I2,待样品完全反应后,滴入几滴淀粉溶液,用c mol/L的Na2S2O3标准液滴定,达到终点时消耗标准液的体积平均值为VmL (已知:I2+ 2NaS2O3= Na2S4O6+ 2NaI )。
①达到滴定终点时的现象是_______
②样品中CuI的质量分数为_______ (用相关字母表示)。

(1)“调节pH”所用试剂为
(2)加入过量KI溶液时发生反应的离子方程式为
(3)取CuI样品m g,加适量的FeCl3溶液恰好使其溶解,CuI 被完全氧化生成Cu2+和I2,待样品完全反应后,滴入几滴淀粉溶液,用c mol/L的Na2S2O3标准液滴定,达到终点时消耗标准液的体积平均值为VmL (已知:I2+ 2NaS2O3= Na2S4O6+ 2NaI )。
①达到滴定终点时的现象是
②样品中CuI的质量分数为
您最近一年使用:0次
【推荐1】钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
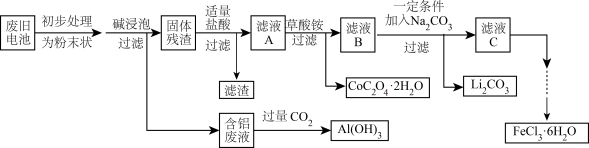
已知:还原性:Cl−>Co2+;
回答下列问题:
(1)废旧电池初步处理为粉末状的目的是___________ 。
(2)从含铝废液得到Al(OH)3的离子方程式为________ 。
(3)滤液A中的溶质除HCl、LiCl外还有FeCl3、CoCl2。写出LiCoO2和盐酸反应的化学方程式_______ 。
(4)滤渣的主要成分为______ (填化学式)。
(5)已知Li2CO3的溶度积常数Ksp=8.64×10−4,将浓度为0.02mol·L−1的Li2SO4和浓度为0.02 mol·L−1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为________ mol·L−1。
(6)从FeCl3溶液得到FeCl3·6H2O固体的操作关键是________ 。

已知:还原性:Cl−>Co2+;
回答下列问题:
(1)废旧电池初步处理为粉末状的目的是
(2)从含铝废液得到Al(OH)3的离子方程式为
(3)滤液A中的溶质除HCl、LiCl外还有FeCl3、CoCl2。写出LiCoO2和盐酸反应的化学方程式
(4)滤渣的主要成分为
(5)已知Li2CO3的溶度积常数Ksp=8.64×10−4,将浓度为0.02mol·L−1的Li2SO4和浓度为0.02 mol·L−1的Na2CO3溶液等体积混合,则溶液中的Li+浓度为
(6)从FeCl3溶液得到FeCl3·6H2O固体的操作关键是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某科研人员以废镍催化剂(主要成分为 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
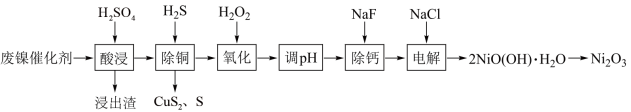
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表:
如表:
回答下列问题:
(1)浸出渣主要成分为___________ (填化学式)。
(2)“氧化”的目的是将溶液中的 氧化为
氧化为 ,温度需控制在
,温度需控制在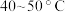 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为___________ 。
(4)“除钙”后,若溶液中 浓度为
浓度为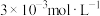 ,则
,则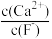 =
=___________ 。[已知常温下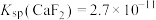 ]
]
(5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
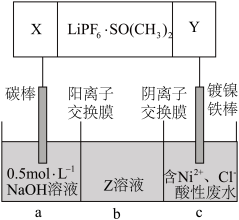
①中间隔室b可以得到的主要物质Z是___________ (填化学式)。
②阳极的电极反应式是___________ 。
 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的
 如表:
如表: |  |  |
| 1.5 | 6.5 | 7.7 |
| 3.7 | 9.7 | 9.2 |
回答下列问题:
(1)浸出渣主要成分为
(2)“氧化”的目的是将溶液中的
 氧化为
氧化为 ,温度需控制在
,温度需控制在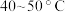 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为
(4)“除钙”后,若溶液中
 浓度为
浓度为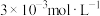 ,则
,则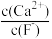 =
=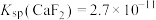 ]
](5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①中间隔室b可以得到的主要物质Z是
②阳极的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼是一种重要的过渡金属元素,钼酸钠晶体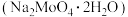 是一种重要的金属缓蚀剂。利用钼矿
是一种重要的金属缓蚀剂。利用钼矿 主要成分
主要成分 为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:

已知: 只能和HF反应,不能和其他酸反应。
只能和HF反应,不能和其他酸反应。
注:式量 Mo:96 :206
:206  :242
:242
 煅烧钼矿产生的气体为
煅烧钼矿产生的气体为 ,写出钼矿煅烧的化学方程式
,写出钼矿煅烧的化学方程式 ________________ 。
 用浓氨水溶解粗产品的离子方程式是
用浓氨水溶解粗产品的离子方程式是____________ ,由图中信息可以判断 是
是______________ 氧化物。 填“酸性”、“碱性”或“两性”
填“酸性”、“碱性”或“两性”
 操作I是
操作I是_________ ,操作Ⅱ所得料液的主要成分是__________  填化学式
填化学式 。
。
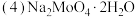 溶于水得到
溶于水得到 的水溶液在
的水溶液在 时密度为
时密度为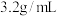 ,则该溶液中
,则该溶液中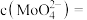
______ 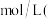 保留2位有效数字
保留2位有效数字
 流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是
流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是______ 。
 利用钼矿
利用钼矿 钼的质量分数为
钼的质量分数为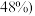 按照上述流程制备
按照上述流程制备 ,理论上,制得晶体
,理论上,制得晶体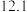 吨则需要的钼矿的质量是
吨则需要的钼矿的质量是_______________ 。
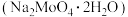 是一种重要的金属缓蚀剂。利用钼矿
是一种重要的金属缓蚀剂。利用钼矿 主要成分
主要成分 为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
为原料冶炼金属钼和制备钼酸钠晶体的主要流程图如下:
已知:
 只能和HF反应,不能和其他酸反应。
只能和HF反应,不能和其他酸反应。注:式量 Mo:96
 :206
:206  :242
:242 煅烧钼矿产生的气体为
煅烧钼矿产生的气体为 ,写出钼矿煅烧的化学方程式
,写出钼矿煅烧的化学方程式  用浓氨水溶解粗产品的离子方程式是
用浓氨水溶解粗产品的离子方程式是 是
是 填“酸性”、“碱性”或“两性”
填“酸性”、“碱性”或“两性”
 操作I是
操作I是 填化学式
填化学式 。
。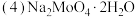 溶于水得到
溶于水得到 的水溶液在
的水溶液在 时密度为
时密度为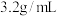 ,则该溶液中
,则该溶液中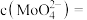
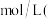 保留2位有效数字
保留2位有效数字
 流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是
流程中用 NaClO做氧化剂将矿石中的钼浸出,该过程的化学方程式是 利用钼矿
利用钼矿 钼的质量分数为
钼的质量分数为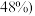 按照上述流程制备
按照上述流程制备 ,理论上,制得晶体
,理论上,制得晶体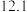 吨则需要的钼矿的质量是
吨则需要的钼矿的质量是
您最近一年使用:0次



