测定水样中 浓度的实验步骤如下:
浓度的实验步骤如下:
①向锥形瓶中加入25.00mL处理后的水样,加入几滴 溶液;
溶液;
②加入 溶液(过量),充分摇匀;
溶液(过量),充分摇匀;
③用 标准溶液进行滴定,至终点时消耗标准溶液
标准溶液进行滴定,至终点时消耗标准溶液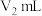 。
。
已知: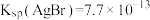 ;
; (白色),
(白色),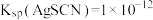 。下列说法错误的是
。下列说法错误的是
 浓度的实验步骤如下:
浓度的实验步骤如下:①向锥形瓶中加入25.00mL处理后的水样,加入几滴
 溶液;
溶液;②加入
 溶液(过量),充分摇匀;
溶液(过量),充分摇匀;③用
 标准溶液进行滴定,至终点时消耗标准溶液
标准溶液进行滴定,至终点时消耗标准溶液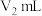 。
。已知:
 ;
; (白色),
(白色),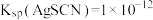 。下列说法错误的是
。下列说法错误的是| A.到达滴定终点时,溶液变为红色 |
| B.该滴定法需在酸性条件下进行 |
C.根据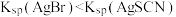 可知,反应 可知,反应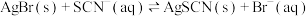 不能发生 不能发生 |
D.该水样中 的浓度 的浓度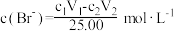 |
更新时间:2022-01-23 19:53:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.一般情况下,盐类越稀越易水解,所以稀释盐溶液,Kh(水解平衡常数)变大 |
| B.一般情况下,一元弱碱的Kb值越大碱性越弱 |
| C.Kw随着溶液中c(H+)和c(OH-)的改变而改变 |
| D.一般情况下,Ksp越大,难溶电解质在水中的溶解程度就越高 |
您最近一年使用:0次
【推荐2】已知相同温度下,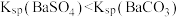 。某温度下,饱和溶液中
。某温度下,饱和溶液中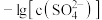 、
、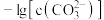 与
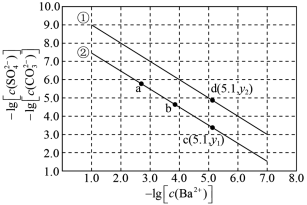
与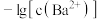 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
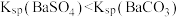 。某温度下,饱和溶液中
。某温度下,饱和溶液中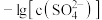 、
、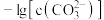 与
与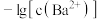 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
| A.曲线①表示硫酸钡的沉淀溶解曲线 |
B.该温度下: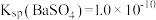 |
| C.加适量BaCl2固体可使溶液由b点变到c点 |
| D.曲线①中的y2 = 4.9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列表示对应化学反应的离子方程式正确的是
| A.用石墨电极电解饱和食盐水:2Cl-+2H2O=2OH-+H2↑+Cl2↑ |
B.向稀NaHCO3中加入过量Ca(OH)2溶液:2 +Ca2++2OH-=CaCO 3↓+2H2O+ +Ca2++2OH-=CaCO 3↓+2H2O+ |
C.用Na2CO3溶液预处理水垢中的CaSO4: +CaSO4=CaCO3+ +CaSO4=CaCO3+ |
D.向稀HNO3中滴加Na2SO3溶液: +2H+=SO2↑+H2O +2H+=SO2↑+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确 的是
A. 该图标是进行化学实验需要佩戴护目镜,以保护眼睛 该图标是进行化学实验需要佩戴护目镜,以保护眼睛 |
| B.向氯化银浊液中滴加1mol/L氨水至足量,溶液变澄清 |
| C.将盛有苯酚与水形成的浊液的试管浸泡在80℃热水中一段时间,浊液变澄清 |
| D.不能将实验室用剩的金属钠块放回原试剂瓶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、实验现象及解释或结论都正确且有因果关系的是
| 实验操作 | 实验现象 | 解释或结论 | |
| A | 向饱和硼酸溶液中加入少量NaHCO3粉末 | 无气泡冒出 | 酸性:碳酸>硼酸 |
| B | 常温下,用pH计分别测定等体积1.0mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 向5mL 0.1mol/L AgNO3溶液中滴加1mL 0.1mol/L NaCl溶液,再向其中滴加1mL 0.1mol/L KI溶液 | 先生成白色沉淀,后有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 向MgCl2溶液中加入NaOH溶液 | 有白色沉淀生成 | 碱性:NaOH>Mg(OH)2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将Na2CO3溶液由0.1mol/L稀释到0.01mol/L,测溶液pH | 溶液pH变小 | 稀释后 的水解程度减小 的水解程度减小 |
| B | 向一定浓度的CuSO4溶液中通入适量的H2S气体 | 出现黑色沉淀 | H2S的酸性比H2SO4强 |
| C | 将盛有棕红色NO2气体的注射器由10 mL 压缩至5 mL | 气体颜色比压缩前变浅 | 反应2NO2 N2O4向右移动 N2O4向右移动 |
| D | 在新生成的AgCl 沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp (AgCl )>Ksp (AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作、现象及结论均正确的是
实验操作 | 现象 | 结论 | |
A | 用石墨电极电解等浓度的 | 阴极开始会析出红色固体物质 | 金属活动性: |
B | 向2mL | 溶液变为血红色 | 能证明 |
C | 向盛有2mL | 先产生白色沉淀,后沉淀变为黄色 |
|
D | 常温下,用 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】探究硫及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 向 与 与 的混合溶液中加入硝酸 的混合溶液中加入硝酸 | 溶液变浑浊 |  将 将 氧化为S 氧化为S |
| B | 室温下用pH试纸分别测定浓度均为 的 的 和 和 两种溶液的pH 两种溶液的pH | pH: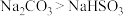 | 结合 能力: 能力: |
| C | 在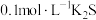 溶液中滴加少量等浓度的 溶液中滴加少量等浓度的 溶液,再加入少量等浓度的 溶液,再加入少量等浓度的 溶液 溶液 | 先产生白色沉淀,后产生黑色沉淀 |  |
| D | 已知 呈红棕色,将 呈红棕色,将 气体通入 气体通入 溶液中 溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色 |  与 与 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
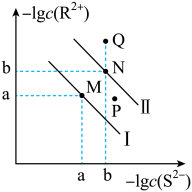
【推荐2】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(FeS)=6.0×10-18,其沉淀溶解平衡曲线如图所示(图中R表示Ni或Fe),下列说法正确的是
(已知: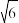 ≈2.4,
≈2.4,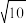 ≈3.2)
≈3.2)

(已知:
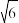 ≈2.4,
≈2.4,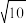 ≈3.2)
≈3.2)| A.曲线I代表NiS |
B.FeS+Ni2+ NiS+Fe2+的平衡常数K=60000 NiS+Fe2+的平衡常数K=60000 |
| C.与P点相对应的FeS的分散系是均一稳定的 |
| D.M点对应的溶液中,c(S2-)≈3.2×10-11 mol•L-1 |
您最近一年使用:0次

 混合溶液
混合溶液
 溶液充分反应,取少量混合液滴加
溶液充分反应,取少量混合液滴加 溶液
溶液 反应有一定限度
反应有一定限度 溶液的试管中滴加2滴
溶液的试管中滴加2滴 溶液,振荡后再滴加4滴
溶液,振荡后再滴加4滴
 计测量
计测量 酸性强于
酸性强于



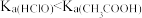 ,
, 的电离度一定比HClO的大
的电离度一定比HClO的大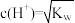 的溶液任何温度下均为中性
的溶液任何温度下均为中性

