氨的合成反应是一个可逆反应:N2(g)+3H2(g) 2NH3(g)。已知298K时:∆H=-92.2kJ·mol-1,∆S=-198.2J·K·mol-1。
2NH3(g)。已知298K时:∆H=-92.2kJ·mol-1,∆S=-198.2J·K·mol-1。
请与同学们交流研讨:
(1)根据反应的焓变和熵变分析298K下氨的合成反应能否正向自发进行____ 。
(2)利用化学平衡移动的知识分析什么条件有利于氨的合成____ 。
 2NH3(g)。已知298K时:∆H=-92.2kJ·mol-1,∆S=-198.2J·K·mol-1。
2NH3(g)。已知298K时:∆H=-92.2kJ·mol-1,∆S=-198.2J·K·mol-1。请与同学们交流研讨:
(1)根据反应的焓变和熵变分析298K下氨的合成反应能否正向自发进行
(2)利用化学平衡移动的知识分析什么条件有利于氨的合成
21-22高二·全国·课前预习 查看更多[2]
更新时间:2022-02-12 08:51:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】变量控制方法是研究化学变化规律的重要思想方法。请仔细观察下表中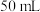 稀盐酸和
稀盐酸和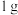 碳酸钙反应的实验数据:
碳酸钙反应的实验数据:
分析上述数据,回答下列问题:
(1)该反应属于____________________ 反应(填“吸热”或“放热”)。
(2)实验6和7表明,____________ 对反应速率有影响,__________________ ,反应速率越大。
(3)根据实验1、3、4、6可以得出外界条件对反应速率的影响规律是___________________________________________ 。
(4)该实验中影响反应速率的因素还有__________________________________________________ ,能表明这一规律的实验序号是1和2与__________________________________________________ 。
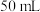 稀盐酸和
稀盐酸和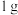 碳酸钙反应的实验数据:
碳酸钙反应的实验数据:| 实验序号 | 碳酸钙状态 | 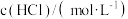 | 溶液温度/℃ | 碳酸钙消失所用的时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 |  | 20 | 39 | 400 |
| 2 | 粉末 |  | 20 | 40 | 60 |
| 3 | 粒状 | 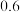 | 20 | 41 | 280 |
| 4 | 粒状 |  | 20 | 40 | 200 |
| 5 | 粉末 |  | 20 | 40 | 30 |
| 6 | 粒状 |  | 20 | 40 | 120 |
| 7 | 粒状 |  | 30 | 50 | 40 |
(1)该反应属于
(2)实验6和7表明,
(3)根据实验1、3、4、6可以得出外界条件对反应速率的影响规律是
(4)该实验中影响反应速率的因素还有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】烟气中SO2和NO的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
①写出NaClO2溶液将NO氧化为NO 的离子方程式:
的离子方程式:___________ 。
②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________ 。
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是___________ 。
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。
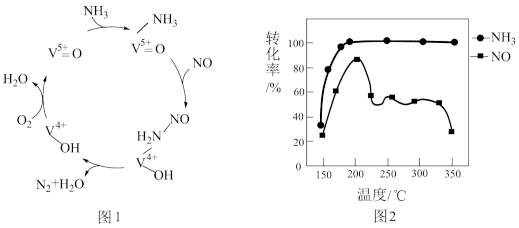
①根据图1机理,NO、NH3在有氧条件下的总化学方程式是___________ 。
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是___________ 。
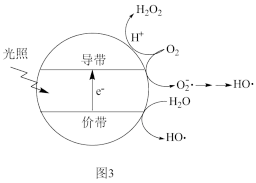
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:___________ 。
(1)采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,在一定浓度的NaClO2溶液中通入含有SO2和NO的烟气,反应温度为323K。
已知: 4H++ClO
 =4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。
=4ClO2+Cl-+2H2O;ClO2氧化性大于NaClO2。①写出NaClO2溶液将NO氧化为NO
 的离子方程式:
的离子方程式:②已知脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是
③当调节溶液初始pH由7升至12时,通入烟气后,NO转化率由100%降为51%,可能的原因是
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂(V2O5)作用下的脱硝反应机理如图1所示。

①根据图1机理,NO、NH3在有氧条件下的总化学方程式是
②按上述图1中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图2所示,200℃后,NO转化率急剧下降的原因是
(3)羟基自由基(HO·)也可以用于脱硫脱硝。图3表示光催化氧化技术可生成HO·:光照时,价带失去电子产生有强氧化性的空穴,价带上生成HO·;描述产生HO·的另一种过程:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ 氮及其化合物的转化过程如图1所示,其中图2为反应①过程中能量变化的曲线图。
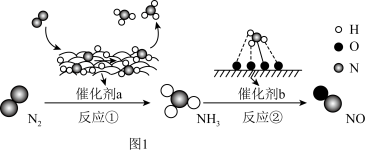
(1)图2中曲线_______ (填字母)是加入催化剂a时的能量变化曲线,该反应破坏生成物全部化学键所需要的总能量_______ (填“大于”或“小于”或“等于”)破坏反应物全部化学键所需要的总能量

(2)标准状况下进行反应②,若有1.25mol电子发生转移,则参加反应的NH3的体积为_______
(3)下列说法正确的是
Ⅱ.以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径

(4)请写出CO2的电子式_______ ,该反应的机理及各分子化学键完全断裂时的能量变化如图所示,根据数据计算,分解1molCO2需_______ (填“吸收”或“放出”) _______ kJ的能量。


(1)图2中曲线

(2)标准状况下进行反应②,若有1.25mol电子发生转移,则参加反应的NH3的体积为
(3)下列说法正确的是
| A.合成氨在工业生产中常将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.工业合成氨中,为加快化学反应速率,压强和温度越高越好 |
| C.合成氨工业要用合适的催化剂,目的是降低该反应的活化能 |
| D.工业合成氨中反应物不能百分之百转化为生成物 |
Ⅱ.以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径

(4)请写出CO2的电子式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应方向的综合判据是判断反应能否白专进行的关键。由于反应的焓变、熵变随温度的变化较小,假设它们不随温度变化,根据下表数据。
(1)根据表中数据可知:反应①在______ 下(填“高温”、“低温”、“任何温度)正向能自发进行。
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?___________ (填“是”或“否”)。阐述判断的理由___________ 。
(3)利用综合判据,计算反应③能正向自发进行的温度范围___________ 。(写出过程)
| 化学反应 | AH/kJ·mol—1 | 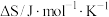 |
①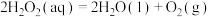 | -98 | 57.2 |
②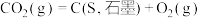 | 393.5 | -2.86 |
③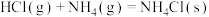 | -176 | -285 |
(2)有人提出采用适当的催化剂,用热分解法分解CO2,以减少CO2的排放,你认为是否可行?
(3)利用综合判据,计算反应③能正向自发进行的温度范围
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一氧化碳是一种重要的化工原料。
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)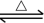 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。
温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将______
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应_______ .
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)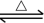 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0
若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为_______ 。
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。_______
(1)高炉炼铁中发生的反应之一是:
FeO(s)+CO(g)
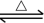 Fe(s)+CO2(g) △H=-1kJ/mol。
Fe(s)+CO2(g) △H=-1kJ/mol。温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比将
(填“增大”、“减小”或“不变”)。
已知1100℃时,该反应平衡常数K=0.263,现测得高炉中(CO2)=0.025mol/L,c(CO)=0.1mol/L,此时该反应
A.向正反应向向进行 B.处于平衡状态 C.向逆反应方向进行
(2)合成氨工业中需将原料气中的CO变成CO2除去。在密闭密器中将CO和H2O混合加热到800℃,达到下列平衡:
CO(g)+H2O(g)
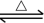 CO2(g)+H2(g) K=1.0
CO2(g)+H2(g) K=1.0若平衡时n(H2O)/n(CO)=1,则CO转化为CO2的转化率为
(3)用CO和H2经如下两步反应制得甲酸甲醛:
CO+2H2→CH3OH
CO+CH3OH→HCOOCH3
已知反应①中CO的转化率为80%,反应②中两种反应物的转化率均为85%,则2.52tCO最多可制得甲酸甲醛多少吨?(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
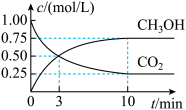
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____ mol/(L·min)。
②该反应的平衡常数表达式为K=_________ 。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________ 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案_______ (填“是”、“否”)可行,理由是:_______ 。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=
②该反应的平衡常数表达式为K=
③下列措施中能使n(CH3OH)/n(CO2)增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案
您最近一年使用:0次



