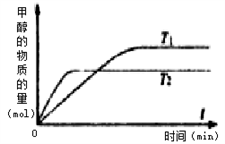
在保持体系总压为105Pa的条件下进行反应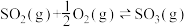 ,原料气中SO2和O2的物质的量之比
,原料气中SO2和O2的物质的量之比 不同时,SO2的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是
不同时,SO2的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是 ,
, ,
, ,下列有关说法正确的是(已知:用平衡分压代替平衡浓度表示的平衡常数为Kp,分压=总压×物质的量分数)
,下列有关说法正确的是(已知:用平衡分压代替平衡浓度表示的平衡常数为Kp,分压=总压×物质的量分数)
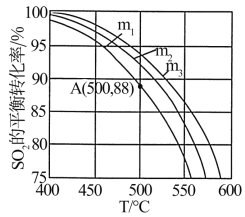
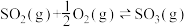 ,原料气中SO2和O2的物质的量之比
,原料气中SO2和O2的物质的量之比 不同时,SO2的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是
不同时,SO2的平衡转化率与温度(T)的关系如图所示。图中A点原料气的成分是 ,
, ,
, ,下列有关说法正确的是(已知:用平衡分压代替平衡浓度表示的平衡常数为Kp,分压=总压×物质的量分数)
,下列有关说法正确的是(已知:用平衡分压代替平衡浓度表示的平衡常数为Kp,分压=总压×物质的量分数)
| A.该反应是吸热反应 |
B.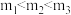 |
C.A点时SO2分压 |
D.在500℃,2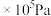 ,m1的条件下,该反应SO2转化率大于88% ,m1的条件下,该反应SO2转化率大于88% |
更新时间:2022-01-08 10:09:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示不同温度(T)和压强(p)对可逆反应2L(g) 2M(g)+2N(g) ΔH>0的影响,且p1>p2。则图中纵轴表示的意义可能是
2M(g)+2N(g) ΔH>0的影响,且p1>p2。则图中纵轴表示的意义可能是
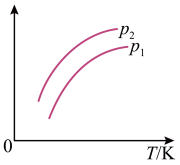
①一定条件下L的转化率 ②混合气体中M的百分含量
③混合气体中L的百分含量 ④混合气体的平均摩尔质量
 2M(g)+2N(g) ΔH>0的影响,且p1>p2。则图中纵轴表示的意义可能是
2M(g)+2N(g) ΔH>0的影响,且p1>p2。则图中纵轴表示的意义可能是
①一定条件下L的转化率 ②混合气体中M的百分含量
③混合气体中L的百分含量 ④混合气体的平均摩尔质量
| A.①③ | B.②④ | C.①② | D.②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下在密闭容器中发生反应:
 。当到达平衡时,下列各项措施中能提高
。当到达平衡时,下列各项措施中能提高 的转化率的是
的转化率的是

 。当到达平衡时,下列各项措施中能提高
。当到达平衡时,下列各项措施中能提高 的转化率的是
的转化率的是A.恒压状态下通入 | B.及时分离 |
C.增大 的物质的量 的物质的量 | D.加入催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将固体NH4HS置于密闭容器中,在某温度下发生下列反应:NH4HS(s)⇌NH3(g)+H2S(g), H2S(g)⇌H2(g)+S(g)。当反应达到平衡时C(H2)=0.5 mol/L,C(H2S)=4.0 mol/L,则第一步的平衡常数为
| A.16 (mol/L)2 | B.18 (mol/L)2 |
| C.20.25 (mol/L)2 | D.22 (mol/L)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: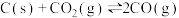 ,平衡时,体系中气体体积分数与温度的关系如图所示:
,平衡时,体系中气体体积分数与温度的关系如图所示:
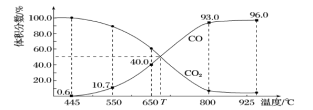
已知:气体分压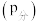
 气体总压
气体总压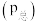
 体积分数。下列说法正确的是
体积分数。下列说法正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: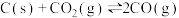 ,平衡时,体系中气体体积分数与温度的关系如图所示:
,平衡时,体系中气体体积分数与温度的关系如图所示:
已知:气体分压
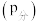
 气体总压
气体总压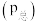
 体积分数。下列说法正确的是
体积分数。下列说法正确的是A.550℃时,若充入惰性气体, 、 、 均减小,平衡不移动 均减小,平衡不移动 |
B.650℃时,反应达平衡后 的转化率为 的转化率为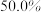 |
C. ℃时,若充入等体积的 ℃时,若充入等体积的 和 和 ,平衡不移动 ,平衡不移动 |
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数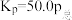 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g)  N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
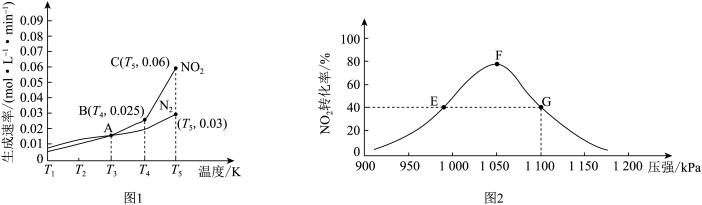
下列说法错误的是
 N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
下列说法错误的是
| A.图1中的A、B、C三个点中只有C点达平衡状态 |
| B.图2中E点的v逆小于F点的v正 |
| C.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| D.在恒温恒容下,向图2中G点平衡体系中充入一定量的NO2,与原平衡相比,NO2的平衡转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定压强下,对于反应2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH,SO2的平衡转化率[α(SO2)]与投料比的比值[ ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
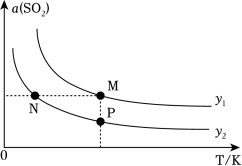
 ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
| A.ΔH>0 | B.温度相同时,y1>y2 |
| C.CO的平衡转化率:N<M | D.逆反应速率:N>P |
您最近一年使用:0次

 (g)和
(g)和
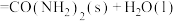 ,测得反应物的浓度随时间变化如图所示。下列说法不正确的是
,测得反应物的浓度随时间变化如图所示。下列说法不正确的是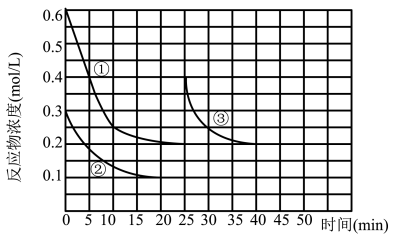

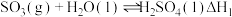 ,浓度平衡常数
,浓度平衡常数
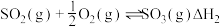 ,浓度平衡常数
,浓度平衡常数
 ,浓度平衡常数
,浓度平衡常数
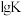 随温度的变化如图所示。下列说法错误的是
随温度的变化如图所示。下列说法错误的是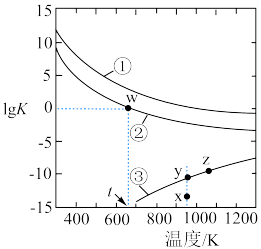
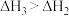
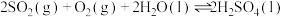 的
的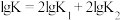
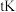 时,反应②在容器中当
时,反应②在容器中当 时,则一定有
时,则一定有
 和
和 进行反应③,三点压强的大小关系为
进行反应③,三点压强的大小关系为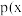 点
点 点
点 点
点