Ⅰ.(化学与生活)材料是人类赖以生存和发展的重要物质基础。
(1)生产水泥的主要原料是___________ 和___________ (填名称)。
(2)有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种___________ 。(选填“橡胶”或“纤维”或“塑料”)
(3)上海世博会中国馆用到一种涂料一氟碳涂层聚酯(FEP),它的单体为CF3—CF=CF2,这种涂料具有___________ (选填“热塑性”或“热固性”)。
(4)由聚氯乙烯等塑料垃圾引起的污染称为“___________ ”。
(5)玻璃钢具有耐腐蚀、质量轻、强度高的性能,它属于___________ 材料(选填“合金”或“复合”)。
Ⅱ.(化学反应原理)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(6)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小的顺序为___________ 。
(7)B为0.1mol·L-1的Na2CO3溶液,实验测得该溶液的pH___________ 7(填“>”“=”或“<”)
(8)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入盐酸,目的是___________ ;若把该溶液加热蒸干,得到的固体物质为___________ (填化学式)。
(9)D为含有足量AgCl固体的饱和溶液,请写出AgCl在水中存在溶解平衡的表达式:___________ 。
(1)生产水泥的主要原料是
(2)有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种
(3)上海世博会中国馆用到一种涂料一氟碳涂层聚酯(FEP),它的单体为CF3—CF=CF2,这种涂料具有
(4)由聚氯乙烯等塑料垃圾引起的污染称为“
(5)玻璃钢具有耐腐蚀、质量轻、强度高的性能,它属于
Ⅱ.(化学反应原理)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(6)A为0.1mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小的顺序为
(7)B为0.1mol·L-1的Na2CO3溶液,实验测得该溶液的pH
(8)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入盐酸,目的是
(9)D为含有足量AgCl固体的饱和溶液,请写出AgCl在水中存在溶解平衡的表达式:
更新时间:2022-03-21 21:27:08
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)磁铁矿的主要成分是_______ ;
(2)钾云母的化学式是K2H4Al6Si6O24,以氧化物形式可表示为_________________________ ;
(3)向FeSO4溶液中滴加NaOH溶液,实验现象是__________________________________ ;
(4)高温分解碳酸钙,选择合适的坩埚_____ (A.瓷坩埚 B.铁坩埚 C.氧化铝坩埚)
(5)生产玻璃的原料有_________ 、________ 、石灰石
(6)用于太阳能电池板,进行光电转化的重要半导体材料,其主要成分是________ ,
(7)写出一种和氯水漂白原理相同的物质______ 。
(2)钾云母的化学式是K2H4Al6Si6O24,以氧化物形式可表示为
(3)向FeSO4溶液中滴加NaOH溶液,实验现象是
(4)高温分解碳酸钙,选择合适的坩埚
(5)生产玻璃的原料有
(6)用于太阳能电池板,进行光电转化的重要半导体材料,其主要成分是
(7)写出一种和氯水漂白原理相同的物质
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 90%以上。
(1)可用于制作计算机芯片的是___________ (填化学式,下同)可用于制作太阳能电池的是___________ ,光导纤维的主要成分是___________ 。
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为___________ 。
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:___________ 。
(4)高纯度单晶硅可以按下列方法制备: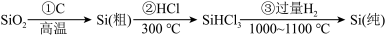
写出步骤①的化学方程式:___________ 。
(1)可用于制作计算机芯片的是
(2)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(3)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(4)高纯度单晶硅可以按下列方法制备:
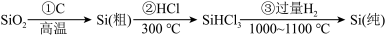
写出步骤①的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业制玻璃主要原料有石英、纯碱和石灰石.在玻璃窑中发生主要反应的化学方程式为:Na2CO3+SiO2 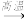 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2 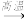 CaSiO3+CO2↑
CaSiO3+CO2↑
(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为________ ,则原料中SiO2、Na2CO3、CaCO3的物质的量之比为_________________________ 。
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式___________________ ,有_____________ 种不同类型的晶体(填数字)
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径___________ (填“大”或“小”),该元素与铝元素两者的最高价氧化物的水化物之间发生反应的离子方程式为__________________________ 。
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有________ 种不同运动状态的电子、________ 种不同能级的电子。
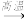 Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2 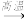 CaSiO3+CO2↑
CaSiO3+CO2↑(1)普通玻璃的成分是Na2CaSi6O14,它的氧化物形式为
(2)在上述反应的反应物和生成物中,属于非极性分子的电子式
(3)在上述普通玻璃的组成元素中某元素与铝元素同周期且原子半径比铝原子半径大,该元素离子半径比铝离子半径
(4)在上述普通玻璃的组成元素中,与铝元素同周期的另一元素的原子最外层共有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】正误判断
1.明矾能水解生成Al(OH)3胶体,可用作净水剂_______
2.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法_______
3.实验室保存Na2S溶液用带有玻璃塞的试剂瓶_______
4.泡沫灭火器中的试剂是Al2(SO4)3溶液与Na2CO3溶液_______
5.焊接时用NH4Cl溶液除锈与盐类水解无关_______
6.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理_______
7.实验室配制FeCl3溶液时,需将FeCl3(s)溶解在较浓盐酸中,然后加水稀释_______
1.明矾能水解生成Al(OH)3胶体,可用作净水剂
2.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
3.实验室保存Na2S溶液用带有玻璃塞的试剂瓶
4.泡沫灭火器中的试剂是Al2(SO4)3溶液与Na2CO3溶液
5.焊接时用NH4Cl溶液除锈与盐类水解无关
6.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理
7.实验室配制FeCl3溶液时,需将FeCl3(s)溶解在较浓盐酸中,然后加水稀释
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】电离常数是研究弱电解质的重要工具,25℃时一些酸的电离常数如下表所示。
请回答:
(1)浓度相同的阴离子在水溶液中结合H+的能力:
_______  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(2)25℃时,pH相同的NaClO和 两种溶液的浓度大小:
两种溶液的浓度大小: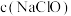
_______  (填“<”、“>”或“=”)。。
(填“<”、“>”或“=”)。。
(3)硫酸在水溶液中是强酸,在冰醋酸中部分电离,写出硫酸在冰醋酸中的电离方程式_______ 。
(4)向NaClO溶液中通入少量的 气体,写出发生反应的离子方程式
气体,写出发生反应的离子方程式_______ 。
(5)25℃时, 的水解平衡常数
的水解平衡常数
_______ (结果保留2位有效数字)。
| 化学式 |  |  | HClO |
电离常数( ) ) |  | 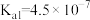 、 、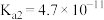 |  |
(1)浓度相同的阴离子在水溶液中结合H+的能力:

 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(2)25℃时,pH相同的NaClO和
 两种溶液的浓度大小:
两种溶液的浓度大小: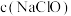
 (填“<”、“>”或“=”)。。
(填“<”、“>”或“=”)。。(3)硫酸在水溶液中是强酸,在冰醋酸中部分电离,写出硫酸在冰醋酸中的电离方程式
(4)向NaClO溶液中通入少量的
 气体,写出发生反应的离子方程式
气体,写出发生反应的离子方程式(5)25℃时,
 的水解平衡常数
的水解平衡常数
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
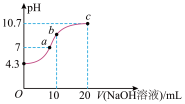
①写出H2N2O2在水溶液中的电离方程式:__ 。
②c点时溶液中各离子浓度由大到小的顺序为__ 。
③b点时溶液中c(H2N2O2)__ c(N2O22-)。(填“>”“<”或“=”,下同)
④a点时溶液中c(Na+)__ c(HN2O)+c(N2O22-)。
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中 =
=__ 。[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5]
(3)有时我们将NaHCO3溶液中的平衡表示为:2HCO3- H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理
H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理___ (填序号)
A.适当浓度的盐酸
B.适当浓度Ba(OH)2溶液
C.适当浓度BaCl2溶液
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②c点时溶液中各离子浓度由大到小的顺序为
③b点时溶液中c(H2N2O2)
④a点时溶液中c(Na+)
(2)硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
 =
=(3)有时我们将NaHCO3溶液中的平衡表示为:2HCO3-
 H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理
H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理A.适当浓度的盐酸
B.适当浓度Ba(OH)2溶液
C.适当浓度BaCl2溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量溶度相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ 。
(3)NaClO溶液中的电荷守恒关系为_______ 。
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因_______ 。
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则V1:V2=
,则V1:V2=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10−4 | 4.7×10−8 | K1=4.3×10−7 K2=5.6×10−11 | Kb=1.7×10−5 |
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)NaClO溶液中的电荷守恒关系为
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
 ,则V1:V2=
,则V1:V2=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知25℃时,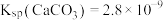 ,
, 式量为100。
式量为100。
(1)书写表示 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式___________ 。
(2)计算25℃ 的溶解度
的溶解度___________  水。(保留2位有效数字)
水。(保留2位有效数字)
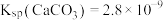 ,
, 式量为100。
式量为100。(1)书写表示
 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式(2)计算25℃
 的溶解度
的溶解度 水。(保留2位有效数字)
水。(保留2位有效数字)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式 ________________________ 。
(2)写出难溶电解质的溶度积表达式,Mg(OH)2:____________ ;在Mg(OH)2悬浊液中加入MgCl2固体,平衡________ 移动(填“正向”“逆向”或“不”),Ksp________ (填“增大”“减小”或“不变”)。
(3)1 g固体炭与水蒸气反应生成CO气体和H2气体,需吸收a kJ热量,此反应的热化学方程式为____ 。
(2)写出难溶电解质的溶度积表达式,Mg(OH)2:
(3)1 g固体炭与水蒸气反应生成CO气体和H2气体,需吸收a kJ热量,此反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】写出下列物质在水溶液中的水解离子方程式及沉淀溶解平衡方程式:
(1)NaClO水解离子方程式___________________________
(2)NH4Cl水解离子方程式____________________________
(3)KAl(SO4)2·12H2O水解离子方程式__________________________
(4)CaCO3沉淀溶解平衡方程式__________________________
(5)Fe(OH)3沉淀溶解平衡方程式__________________________
(1)NaClO水解离子方程式
(2)NH4Cl水解离子方程式
(3)KAl(SO4)2·12H2O水解离子方程式
(4)CaCO3沉淀溶解平衡方程式
(5)Fe(OH)3沉淀溶解平衡方程式
您最近一年使用:0次



