已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量溶度相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其pH由大到小的顺序是_______ (填序号)。
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ 。
(3)NaClO溶液中的电荷守恒关系为_______ 。
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因_______ 。
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则V1:V2=
,则V1:V2=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10−4 | 4.7×10−8 | K1=4.3×10−7 K2=5.6×10−11 | Kb=1.7×10−5 |
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)NaClO溶液中的电荷守恒关系为
(4)用离子方程式说明碳酸氢钠溶液呈碱性的原因
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
 ,则V1:V2=
,则V1:V2=
更新时间:2022-09-22 08:22:12
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】室温下,向 100 mL NaOH、Ba(OH)2 的混合溶液中加入 100 mL 0.3 mol·L-1 的 H2SO4 溶液,充分反应,得沉淀 2.33 g,反应后测得溶液的 pH=13(假设反应后溶液的总体积为 200 mL)。 请计算:
(1)原混合溶液中所含的Ba(OH)2物质的量是_______ mol。
(2)原混合溶液中 NaOH 的物质的量浓度是_______ mol·L-1
(1)原混合溶液中所含的Ba(OH)2物质的量是
(2)原混合溶液中 NaOH 的物质的量浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题。
(1)CH3COOH、H2CO3、 、HClO的酸性由强到弱的顺序:
、HClO的酸性由强到弱的顺序:___________
(2)CH3COO-、 、
、  、 ClO-结合H+的能力由强到弱的顺序:
、 ClO-结合H+的能力由强到弱的顺序:___________
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)CH3COOH、H2CO3、
 、HClO的酸性由强到弱的顺序:
、HClO的酸性由强到弱的顺序:(2)CH3COO-、
 、
、  、 ClO-结合H+的能力由强到弱的顺序:
、 ClO-结合H+的能力由强到弱的顺序:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案并记录了实验现象:取少量Na2CO3固体,加入无水酒精,充分振荡、静置,取上层清液,滴加酚酞试液,溶液仍无色,然后加入少量水,溶液变为红色。向该红色溶液中滴加足量BaCl2溶液(中性),红色褪去。
(1)该实验表明,Na2CO3溶液显碱性的原因是___ (填代号)。
(2)从形成盐的酸和碱的强弱角度看,Na2CO3属于____ (填代号)。
(3)硫酸铝具有净水作用,是因为___ 。
(4)实验室为了确定Na2CO3•xH2O的组成,取1.43gNa2CO3•xH2O溶于水配成10.00mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.00mL,并收集到112mLCO2(标准状况)。试计算(写出解题过程)
①x的值___ 。
②所用稀盐酸的物质的量浓度___ 。
(1)该实验表明,Na2CO3溶液显碱性的原因是
| A.Na2CO3溶液提供Na+ | B.Na2CO3提供CO |
| C.Na2CO3提供OH- | D.CO 与水反应生成OH- 与水反应生成OH- |
| A.强酸强碱盐 | B.强酸弱碱盐 | C.弱酸强碱盐 | D.弱酸弱碱盐 |
(4)实验室为了确定Na2CO3•xH2O的组成,取1.43gNa2CO3•xH2O溶于水配成10.00mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.00mL,并收集到112mLCO2(标准状况)。试计算(写出解题过程)
①x的值
②所用稀盐酸的物质的量浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】 是常见的强碱弱酸盐,可由醋酸和
是常见的强碱弱酸盐,可由醋酸和 反应得到。
反应得到。
(1) 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示); 溶液呈电中性,请用等式表示这一现象:
溶液呈电中性,请用等式表示这一现象:___________ 。
(2)常温下,用 溶液分别滴定
溶液分别滴定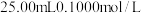 盐酸和
盐酸和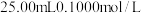 醋酸,滴定过程中
醋酸,滴定过程中 变化曲线如图所示。
变化曲线如图所示。


①由图中数据判断滴定盐酸的pH变化曲线为___________ (填“图1”或“图2”),判断的理由:
a.起始未滴加 溶液时,
溶液时, 盐酸的
盐酸的
___________ 。
b.加入 溶液恰好反应时,所得
溶液恰好反应时,所得 溶液的
溶液的
___________ 。
②滴定 溶液的过程中,当滴加
溶液的过程中,当滴加 溶液时,溶液中各离子浓度由大到小的顺序是
溶液时,溶液中各离子浓度由大到小的顺序是___________ ,此时溶液中
___________ 。
 是常见的强碱弱酸盐,可由醋酸和
是常见的强碱弱酸盐,可由醋酸和 反应得到。
反应得到。(1)
 溶液呈碱性的原因是
溶液呈碱性的原因是 溶液呈电中性,请用等式表示这一现象:
溶液呈电中性,请用等式表示这一现象:(2)常温下,用
 溶液分别滴定
溶液分别滴定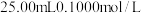 盐酸和
盐酸和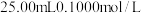 醋酸,滴定过程中
醋酸,滴定过程中 变化曲线如图所示。
变化曲线如图所示。

①由图中数据判断滴定盐酸的pH变化曲线为
a.起始未滴加
 溶液时,
溶液时, 盐酸的
盐酸的
b.加入
 溶液恰好反应时,所得
溶液恰好反应时,所得 溶液的
溶液的
②滴定
 溶液的过程中,当滴加
溶液的过程中,当滴加 溶液时,溶液中各离子浓度由大到小的顺序是
溶液时,溶液中各离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】25℃时,有0.10mol·L 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
回答下列相关问题
(1)③中溶液的pH_____ 1(填“>”、“<”或“=”),请用电离方程式解释_____
(2)②中溶液的
_____ ,则溶液由水电离出的
_____ mol/L。②与④混合后 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为_____ 。
(3)向溶液①中加入等体积水稀释,稀释后溶液中的 比稀释前
比稀释前_____ (填“增大”“减小”或“不变”),原因_____ 。(用化学用语表示)
(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是_____ 。
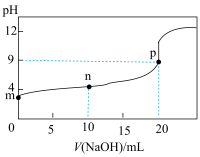
a.点m溶液中离子浓度关系: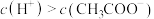
b.点n溶液中存在如下关系:
c.点p溶液反应的离子方程式:
d.点p溶液中,由水电离出的 是
是 mol⋅L
mol⋅L
 的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。
的下列4种溶液①氨水②盐酸③醋酸溶液④氢氧化钠溶液。回答下列相关问题
(1)③中溶液的pH
(2)②中溶液的


 ,则盐酸和氢氧化钠体积比为
,则盐酸和氢氧化钠体积比为(3)向溶液①中加入等体积水稀释,稀释后溶液中的
 比稀释前
比稀释前(4)25℃时,取20mL溶液③,向其中逐滴滴入溶液④,过程中pH随溶液④体积的变化如下图所示。下列说法正确的是

a.点m溶液中离子浓度关系:
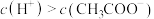
b.点n溶液中存在如下关系:

c.点p溶液反应的离子方程式:

d.点p溶液中,由水电离出的
 是
是 mol⋅L
mol⋅L
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO 、SO
、SO 、Cl-中的若干种离子,该小组同学取100 mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如图所示:
、Cl-中的若干种离子,该小组同学取100 mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如图所示:
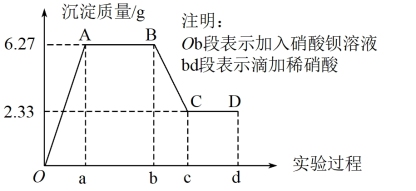
(1)水样中一定含有的阴离子是___________ ,其物质的量浓度之比为___________ 。
(2)写出BC段曲线所表示反应的离子方程式:___________ 。
(3)由B点到C点变化过程中消耗硝酸的体积为___________ 。
(4)试根据实验结果推测K+是否存在?___________ (填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是___________ (若K+不存在,则不必回答)。
 、SO
、SO 、Cl-中的若干种离子,该小组同学取100 mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如图所示:
、Cl-中的若干种离子,该小组同学取100 mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如图所示:
(1)水样中一定含有的阴离子是
(2)写出BC段曲线所表示反应的离子方程式:
(3)由B点到C点变化过程中消耗硝酸的体积为
(4)试根据实验结果推测K+是否存在?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)25℃时,浓度为0.1mol·L-1的5种溶液:①HCl;②CH3COOH;③Ba(OH)2;④Na2CO3;⑤KCl,溶液pH由小到大的顺序为___ (填编号)。
(2)MgCl2·6H2O制无水MgCl2要在___ 气流中加热。
(3)普通泡沫灭火器内的玻璃筒里﹣盛硫酸铝溶液,铁筒里﹣盛碳酸氢钠溶液,其化学反应的原理是___ (用离子方程式表示)。
(4)常温下,若1体积的硫酸与2体积pH=11的氢氧化钠溶液混合后的溶液的pH=3(混合后体积变化不计),则二者物质的量浓度之比为___ 。
(5)常温下,0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(A-)=___ mol/L(填精确计算结果的具体数字)。
(6)为证明盐的水解是吸热的,三位同学分别设计了如下方案,其中正确的是___ (填序号)。
a.甲同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的
b.乙同学:在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的
c.丙同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的
(2)MgCl2·6H2O制无水MgCl2要在
(3)普通泡沫灭火器内的玻璃筒里﹣盛硫酸铝溶液,铁筒里﹣盛碳酸氢钠溶液,其化学反应的原理是
(4)常温下,若1体积的硫酸与2体积pH=11的氢氧化钠溶液混合后的溶液的pH=3(混合后体积变化不计),则二者物质的量浓度之比为
(5)常温下,0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(A-)=
(6)为证明盐的水解是吸热的,三位同学分别设计了如下方案,其中正确的是
a.甲同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的
b.乙同学:在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的
c.丙同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】汽车是人们出行的重要交通工具,其中蕴含着大量的化学知识,回答下列问题:
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于_______ (填“天然”或“合成”)橡胶。
(2)汽车安全气囊启动时发生的反应有: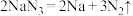 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:_______ 。
(3)在催化剂作用下,汽车尾气中的 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式_______ 。
(4)汽车排放的 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当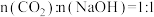 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是_______ ,
_______ 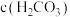 (填“>”或“<”)。
(填“>”或“<”)。
(5)使用燃料电池汽车可解决 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式_______ 。
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于
(2)汽车安全气囊启动时发生的反应有:
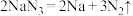 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:(3)在催化剂作用下,汽车尾气中的
 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式(4)汽车排放的
 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当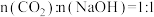 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是
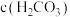 (填“>”或“<”)。
(填“>”或“<”)。(5)使用燃料电池汽车可解决
 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1)25℃时,在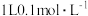 的HA溶液中,有
的HA溶液中,有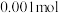 的HA电离成离子,则该温度下的电离平衡常数约为
的HA电离成离子,则该温度下的电离平衡常数约为___________ 。
(2)在25℃时,将pH=11的 溶液
溶液 与pH=2的HCl溶液
与pH=2的HCl溶液 混合,若所得溶液为中性,则
混合,若所得溶液为中性,则 。
。
(3)常温下将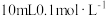 的NaOH溶液与
的NaOH溶液与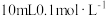 的醋酸溶液混合,则混合后溶液中各离子浓度的大小顺序为
的醋酸溶液混合,则混合后溶液中各离子浓度的大小顺序为___________ 。
(4)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
①上述四种酸酸性由强到弱的顺序为___________ ;
②将少量的 通入
通入 溶液中,反应的离子方程式:
溶液中,反应的离子方程式:___________ 。
(5)已知在25℃时,将浓度相等的HF与NaF溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因___________ 。
(1)25℃时,在
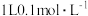 的HA溶液中,有
的HA溶液中,有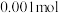 的HA电离成离子,则该温度下的电离平衡常数约为
的HA电离成离子,则该温度下的电离平衡常数约为(2)在25℃时,将pH=11的
 溶液
溶液 与pH=2的HCl溶液
与pH=2的HCl溶液 混合,若所得溶液为中性,则
混合,若所得溶液为中性,则 。
。(3)常温下将
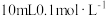 的NaOH溶液与
的NaOH溶液与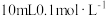 的醋酸溶液混合,则混合后溶液中各离子浓度的大小顺序为
的醋酸溶液混合,则混合后溶液中各离子浓度的大小顺序为(4)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
| 化学式 |  |  |  |  |
| 电离平衡常数 | 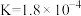 | 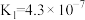 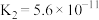 |  | 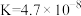 |
②将少量的
 通入
通入 溶液中,反应的离子方程式:
溶液中,反应的离子方程式:(5)已知在25℃时,将浓度相等的HF与NaF溶液等体积混合,溶液呈酸性。解释溶液呈酸性的原因
您最近一年使用:0次



