磷与氯气在一定条件下反应,可以生成PCl3、PCl5。
(1)写出磷原子的电子排布式:___________ 。
(2)PCl3分子中磷原子采用的杂化方式是___________ ,分子的空间构型为___________ 。
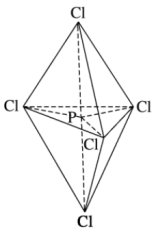
(3)磷原子在形成PCl5分子时,除最外层s、p轨道参与杂化外,其3d轨道也有1个参加了杂化,称为sp3d杂化。成键电子对数与孤电子对数总和为5的原子常采用sp3d杂化。PCl5分子中5个杂化轨道分别与氯原子配对成键,PCl5的空间构型为三角双锥形(如下图所示)。下列关于PCl5分子的说法正确的有___________。
(4)N、P是同一族元素,P能形成PCl3、PCl5两种氯化物,而N只能形成一种氯化物NCl3,而不能形成NCl5,原因是___________ 。
(1)写出磷原子的电子排布式:
(2)PCl3分子中磷原子采用的杂化方式是
(3)磷原子在形成PCl5分子时,除最外层s、p轨道参与杂化外,其3d轨道也有1个参加了杂化,称为sp3d杂化。成键电子对数与孤电子对数总和为5的原子常采用sp3d杂化。PCl5分子中5个杂化轨道分别与氯原子配对成键,PCl5的空间构型为三角双锥形(如下图所示)。下列关于PCl5分子的说法正确的有___________。

| A.PCl5分子中磷原子没有孤对电子 |
| B.PCl5分子中没有形成π键 |
| C.PCl5分子中所有的Cl—P—Cl键角都相等 |
| D.SF4分子中S原子也采用sp3d杂化 |
更新时间:2022-03-25 10:52:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E六种元素:
(1)A元素基态原子最外层有3个未成对电子,次外层有2个电子。该元素在周期表中的位置是_______ 。基态原子电子排布式式_______ 。
(2)B元素是周期表前四周期中未成对电子数最多的元素,B元素名称为_______ ,B的价电子排布式_______ 。
(3)C元素的+3价离子的3d能级半充满,C元素位于周期表中_______ 区,具体位置是_______ ,C元素的+3价离子的符号_______ ,该离子结构示意图_______ ,C元素的核外电子排布式_______ 。
(4)D元素基态原子M层全充满,N层没有成对电子,只有一个未成对电子,该元素简化电子排布式_______ ,位于周期表_______ 区,价电子排布图_______ 。
(5)E元素的最外层电子排布式为nsnnpn+1,则n等于_______ ,原子中能量最高的是_______ 电子。
(1)A元素基态原子最外层有3个未成对电子,次外层有2个电子。该元素在周期表中的位置是
(2)B元素是周期表前四周期中未成对电子数最多的元素,B元素名称为
(3)C元素的+3价离子的3d能级半充满,C元素位于周期表中
(4)D元素基态原子M层全充满,N层没有成对电子,只有一个未成对电子,该元素简化电子排布式
(5)E元素的最外层电子排布式为nsnnpn+1,则n等于
您最近一年使用:0次
【推荐2】每个时代的发展都离不开化学材料。黄铜是人类最早使用的合金之一,主要由锌和铜组成。回答下列问题:
(1)基态锌原子的价电子排布式为___ ,属于周期表___ 区元素。电子占据最高能层的电子云轮廓图形状为___ 。
(2)第一电离能I1(Zn)___ I1(Cu)(填“大于”或“小于”)。
(3)向[Cu(H2O)4]2+溶液(天蓝色)中加入过量氨水将生成更稳定的[Cu(NH3)4]2+溶液(深蓝色),原因是___ ;向深蓝色溶液中逐滴加入稀盐酸,观察到的现象是___ 。
(1)基态锌原子的价电子排布式为
(2)第一电离能I1(Zn)
(3)向[Cu(H2O)4]2+溶液(天蓝色)中加入过量氨水将生成更稳定的[Cu(NH3)4]2+溶液(深蓝色),原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】指出下列物质中的过氧键,并标出氧元素的化合价。
(1)过氧乙酸_______

(2)过二硫酸_______
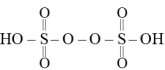
(1)过氧乙酸

(2)过二硫酸
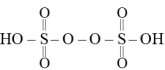
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)CH4中的化学键从形成的过程来看属于_____ (填“σ”或“π”)键,从其极性来看属于_____ (填“极性”或“非极性”)键。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为_____ 。与CH4互为等电子体的阳离子是____ ;与CO2互为等电子体的阴离子是____ 。
(3)在①CH2=CH2、②HC≡CH、③HCHO三种物质中,其碳原子采取sp2杂化的分子有_____ (填序号)。
(4)碳有多种同素异形体,其中石墨烯的结构如图所示:
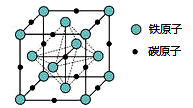

在石墨烯晶体中,每个六元环含有_____ 个C原 子,一种铁碳的化合物晶胞如图,该化合物的化学式为______ 。
(1)CH4中的化学键从形成的过程来看属于
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为
(3)在①CH2=CH2、②HC≡CH、③HCHO三种物质中,其碳原子采取sp2杂化的分子有
(4)碳有多种同素异形体,其中石墨烯的结构如图所示:


在石墨烯晶体中,每个六元环含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有下列8种晶体,用序号回答下列问题:
A.水晶 B.白磷 C.冰醋酸 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)含有非极性键的原子晶体是_____ ,属于原子晶体的化合物是___ ,不含化学键的分子晶体是______ ,属于分子晶体的单质是_________ 。
(2)含有离子键、共价键、配位键的化合物是___________ ,受热熔化,需克服共价键的是___________ 。
(3)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有_____ 个硅原子,______ 个碳原子;金刚石熔点高于金刚砂的原因_____________________________________ 。

金刚石结构
A.水晶 B.白磷 C.冰醋酸 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)含有非极性键的原子晶体是
(2)含有离子键、共价键、配位键的化合物是
(3)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有

金刚石结构
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CF2=CF2和聚四氟乙烯(ETFE)分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】磷化硼(BP)是一种受到高度关注的金属保护层耐磨材料,可由三溴化硼和三溴化磷在氢气中高温制得。
(1)合成BP的反应中,基态原子未成对电子最多的元素符号为____ ,核外电子数最多的元素的基态原子电子占据最高能级上的电子数为____ 。B所在的周期第一电离能最大的元素名称为____ 。
(2)三溴化磷分子的中心原子价层电子对数为____ ,分子空间结构为____ 形。BBr3空间结构为____ 形,PBr3分子中键角比BBr3分子中键角____ (填>、<或=)。
(3)N与P同主族。科学家在一定条件下把氮气(氮氮三键键能为942kJ•mol-1)聚合为固体高聚氮,全部以N-N键相连且键能为160kJ•mol-1,这种固体高聚氮可能潜在的用途是____ ,这是因为____ 。
(4)BP晶胞,磷原子在晶胞中采用金属铜原子的堆积方式,硼原子填充在其四面体空隙中,则其四面体填充率为____ ,已知晶胞参数a=478pm,则硼和磷原子的核间距为____ pm(保留整数)。
(1)合成BP的反应中,基态原子未成对电子最多的元素符号为
(2)三溴化磷分子的中心原子价层电子对数为
(3)N与P同主族。科学家在一定条件下把氮气(氮氮三键键能为942kJ•mol-1)聚合为固体高聚氮,全部以N-N键相连且键能为160kJ•mol-1,这种固体高聚氮可能潜在的用途是
(4)BP晶胞,磷原子在晶胞中采用金属铜原子的堆积方式,硼原子填充在其四面体空隙中,则其四面体填充率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】黑火药的主要成分为木炭(C)、硫黄(S)和火硝(KNO3).请回答下列问题。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为___________ 。
(3)C、N、O、K四种元素的第一电离能由大到小的顺序为___________ 。
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为___________ ;
②H2Se的中心原子杂化类型是:___________ , SeO32-的立体构型是___________ ;
③比较H2S与H2O沸点高低,并说明原因:___________ 。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为
(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为(3)C、N、O、K四种元素的第一电离能由大到小的顺序为
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为
②H2Se的中心原子杂化类型是:
③比较H2S与H2O沸点高低,并说明原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是短式元素周期表的一部分。
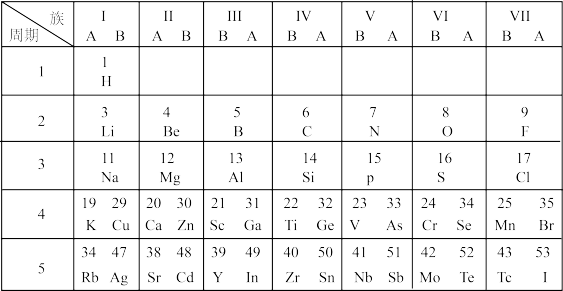
(1) H和
H和 H互为
H互为___________ 。
(2)H2O的电子式为___________ ,GeH4分子的空间结构为___________ 。
(3)向NaBr溶液中滴加___________ (填试剂名称),若发生反应___________ (用离子方程式表示),则证明Cl原子得电子能力比Br原子强。
(4)在实验室用无水乙醇和冰醋酸制备乙酸乙酯的化学方程式为___________ 。
(5)前三周期元素X、Y原子序数依次增大,原子X、Y的最外层电子数均为K层的2倍。工业上利用单质X制备单质Y的化学方程式为___________ 。
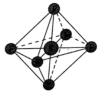
(6)SF6分子的空间结构为正八面体形,如图所示。1 mol SF6中含有___________ mol S—F键,它的二氯代物SF4Cl2有___________ 种。

(1)
 H和
H和 H互为
H互为(2)H2O的电子式为
(3)向NaBr溶液中滴加
(4)在实验室用无水乙醇和冰醋酸制备乙酸乙酯的化学方程式为
(5)前三周期元素X、Y原子序数依次增大,原子X、Y的最外层电子数均为K层的2倍。工业上利用单质X制备单质Y的化学方程式为
(6)SF6分子的空间结构为正八面体形,如图所示。1 mol SF6中含有

您最近一年使用:0次