将NO2装入带活塞的密闭容器中,当反应2NO2(g) N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
 N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是
N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是| A.压缩气体体积,平衡向右移动,混合气体颜色变浅 |
| B.恒温恒压时,充入稀有气体,平衡向左移动,混合气体颜色变深 |
| C.恒温恒容时,充入稀有气体,压强增大,平衡向右移动,混合气体的颜色变浅 |
| D.升高温度,气体颜色加深,则此反应为放热反应 |
21-22高二上·陕西宝鸡·期中 查看更多[5]
陕西省宝鸡市长岭中学2021-2022学年高二上学期期中考试化学试题陕西省渭南高级中学2021-2022学年高一下学期第三阶段考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】60(已下线)【2022】【高二化学】【期中考】-179甘肃省天水市第二中学2023-2024学年高二上学期第一次月考化学试题
更新时间:2022-03-22 17:57:38
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】CO2催化重整CH4的反应:
(Ⅰ)CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1,
2CO(g)+2H2(g) ΔH1,
主要副反应:(Ⅱ)H2(g)+CO2(g) CO(g)+H2O(g) ΔH2>0,
CO(g)+H2O(g) ΔH2>0,
(Ⅲ)4H2(g)+CO2(g) CH4(g)+2H2O(g) ΔH3<0。
CH4(g)+2H2O(g) ΔH3<0。
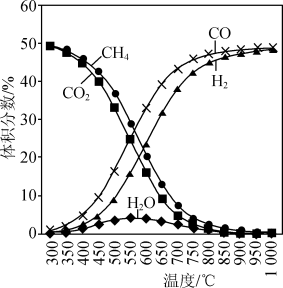
在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法不正确 的是
(Ⅰ)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1,
2CO(g)+2H2(g) ΔH1,主要副反应:(Ⅱ)H2(g)+CO2(g)
 CO(g)+H2O(g) ΔH2>0,
CO(g)+H2O(g) ΔH2>0,(Ⅲ)4H2(g)+CO2(g)
 CH4(g)+2H2O(g) ΔH3<0。
CH4(g)+2H2O(g) ΔH3<0。在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法

| A.ΔH1=2ΔH2-ΔH3>0 |
| B.其他条件不变,适当增大起始时V(CH4)∶V(CO2),可抑制副反应(Ⅱ)、(Ⅲ)的进行 |
| C.300~580℃时,H2O的体积分数不断增大,是由于反应(Ⅲ)生成H2O的量大于反应(Ⅱ)消耗的量 |
| D.T℃时,在2.0L容器中加入2molCH4、2molCO2以及催化剂进行重整反应,测得CO2的平衡转化率为75%,则反应(Ⅰ)的平衡常数小于81 |
您最近一年使用:0次
单选题
|
较难
(0.4)
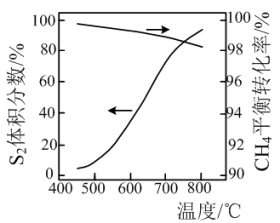
【推荐2】在工业生产上通常利用硫(S8)与CH4为原料制备CS2,主要发生以下两个反应: 反应I:S8(g)=4S2(g);反应II:2S2(g)+CH4(g)  CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法不正确 的是
 CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
CS2(g)+2H2S(g)。一定条件下,S8分解产生S2的体积分数、CH4与S2反应中CH4的平衡转化率与温度的关系如图所示。下列说法
| A.反应II的正反应为放热反应 |
| B.某温度下若S8完全分解成S2,在恒容密闭容器中,n(S2)∶n(CH4)=2∶1开始反应,当CS2体积分数为10%时,CH4转化率为60% |
| C.通过增大S8的浓度可以提高CH4的转化率 |
| D.制备CS2时温度需高于600℃的原因是:此温度CH4平衡转化率已很高,低于此温度,S2浓度小,反应速率慢 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】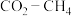 催化重整可获得合成气
催化重整可获得合成气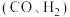 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为
反应①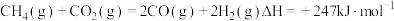
反应②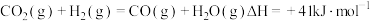
反应③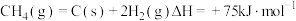
反应④
研究发现在密闭容器中 下,
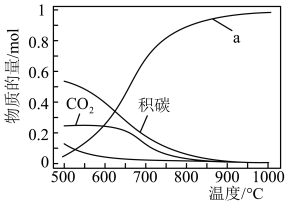
下,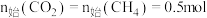 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
 催化重整可获得合成气
催化重整可获得合成气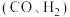 。重整过程中主要反应的热化学方程式为
。重整过程中主要反应的热化学方程式为反应①
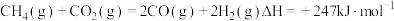
反应②
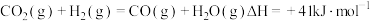
反应③
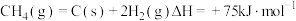
反应④

研究发现在密闭容器中
 下,
下,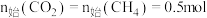 ,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
,平衡时各含碳物种的物质的量随温度的变化如图所示。下列说法正确的是
A.图中a表示 |
B. 的 的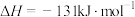 |
C.其他条件不变,在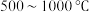 范围,随着温度的升高,平衡时 范围,随着温度的升高,平衡时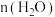 不断增大 不断增大 |
D.当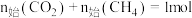 ,其他条件不变时,提高 ,其他条件不变时,提高 的值,能减少平衡时积碳量 的值,能减少平衡时积碳量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某实验小组将足量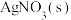 置于温度为T℃、体积为V的密闭容器中,发生反应
置于温度为T℃、体积为V的密闭容器中,发生反应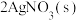
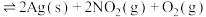 ,测出总压p随时间的变化如下图中A曲线所示。下列有关说法正确的是
,测出总压p随时间的变化如下图中A曲线所示。下列有关说法正确的是
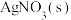 置于温度为T℃、体积为V的密闭容器中,发生反应
置于温度为T℃、体积为V的密闭容器中,发生反应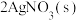
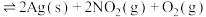 ,测出总压p随时间的变化如下图中A曲线所示。下列有关说法正确的是
,测出总压p随时间的变化如下图中A曲线所示。下列有关说法正确的是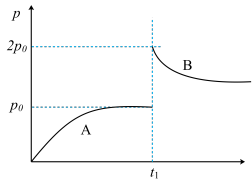
A.在T℃时,该反应压强平衡常数为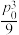 |
B.若在 时刻减小体积为 时刻减小体积为 ,则容器内压强变化为曲线B ,则容器内压强变化为曲线B |
C.若减少适量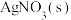 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.若充入少量 ,发生反应 ,发生反应 ,T℃达平衡时,与原平衡相比, ,T℃达平衡时,与原平衡相比, 的分压减小, 的分压减小, 的分压增大 的分压增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一定温度下,向容积固定不变的密闭容器中充入a mol A,发生反应:2A(g)  B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
 B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
B(g) ΔH<0。达平衡后再向容器中充入a mol A,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )| A.平均相对分子质量增大 |
| B.A的转化率提高 |
| C.A的质量分数增大 |
| D.反应放出的总热量大于原来的2倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s) + CO2(g) 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
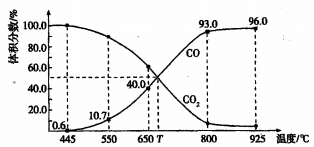
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
| A.550℃时,若充入惰性气体,V正、V逆均减小,平衡不移动 |
| B.650℃时,反应达平衡后CO2的转化率为40.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列事实能用勒夏特列原理解释的是
| A.红棕色的NO2,加压后颜色变深 |
B.对于反应2HI(g) H2 (g)+I2(g),达到平衡后,缩小容器的体积可使体系颜色变深 H2 (g)+I2(g),达到平衡后,缩小容器的体积可使体系颜色变深 |
| C.实验室中常用排饱和食盐水的方法收集氯气 |
| D.500℃左右比室温更利于合成氨反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】200℃时,向体积可变的密闭容器中加入足量草酸锰固体(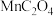 ),发生反应:
),发生反应: 。达到平衡时,
。达到平衡时,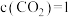 mol·L
mol·L 。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
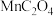 ),发生反应:
),发生反应: 。达到平衡时,
。达到平衡时,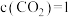 mol·L
mol·L 。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是| A.平衡常数不变 | B. 不变 不变 | C.MnO的质量不变 | D.逆反应速率增大 |
您最近一年使用:0次

 HBr+HBrO,当加入硝酸银溶液后(AgBr是淡黄色沉淀),溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后(AgBr是淡黄色沉淀),溶液颜色变浅

