常温下,向 溶液中滴加
溶液中滴加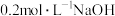 溶液。有关微粒的物质的量变化如图(其中Ⅰ代表
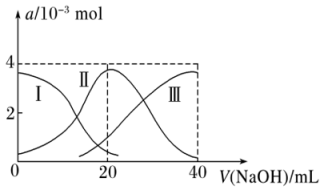
溶液。有关微粒的物质的量变化如图(其中Ⅰ代表 ,Ⅱ代表
,Ⅱ代表 ,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
 溶液中滴加
溶液中滴加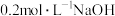 溶液。有关微粒的物质的量变化如图(其中Ⅰ代表
溶液。有关微粒的物质的量变化如图(其中Ⅰ代表 ,Ⅱ代表
,Ⅱ代表 ,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
,Ⅲ代表A2-)。根据图示判断,下列说法不正确的是
A.当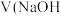 溶液 溶液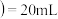 时,溶液中离子浓度大小关系: 时,溶液中离子浓度大小关系: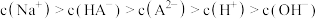 |
B.NaHA溶液中: |
C.当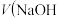 溶液 溶液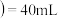 时,其溶液中水的电离程度比纯水大 时,其溶液中水的电离程度比纯水大 |
D.向 溶液加入水的过程中,pH减小 溶液加入水的过程中,pH减小 |
更新时间:2022-04-07 17:43:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃,向20 mL 0.01 mol·L−1 CH3COOH溶液滴入0.01 mol·L-1 NaOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示,已知CH3COOH的Ka=1.8×10−5,下列说法不正确 的是


| A.b点溶液中:c(CH3COO-) < c(CH3COOH) |
| B.x=20,c点溶液中,c(Na+) = c(CH3COO-)+c(CH3COOH) |
| C.e点溶液中:c(Na+) >c(OH-)>c(CH3COO-)>c(H+) |
| D.滴定过程中,c(CH3COO-)与c(OH-)的比值逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在给定条件下,下列离子组的离子共存判断及反应的离子方程式均正确的是
| 选项 | 条件 | 离子组 | 离子共存判断及的离子方程式 |
| A | 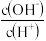 =1的溶液中 =1的溶液中 | Fe2+、NO 、Al3+、CO 、Al3+、CO | 不能大量共存,3Fe2++4H++NO =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
| B | 由水电离出c(H+) =1×10-13mol·L-1 | K+、NH 、Cl-、[Al(OH)4]- 、Cl-、[Al(OH)4]- | 能大量共存 |
| C | 有大量Fe3+的溶液 | Na+、NH 、SO 、SO 、Cl- 、Cl- | 能大量共存 |
| D | 通入少量SO2气体 | K+、Na+、ClO-、SO | 不能大量共存,2ClO-+SO2+H2O=2HClO+SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,用浓度为 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随 (
( )的变化曲线如图所示。下列说法错误的是
)的变化曲线如图所示。下列说法错误的是
 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 的
的 和
和 的混合溶液,滴定过程中溶液的
的混合溶液,滴定过程中溶液的 随
随 (
( )的变化曲线如图所示。下列说法错误的是
)的变化曲线如图所示。下列说法错误的是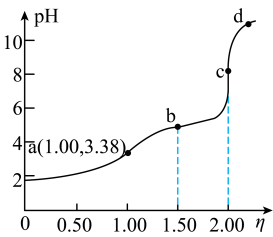
A.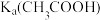 约为 约为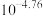 |
B.点a: |
C.点b: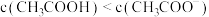 |
D.水的电离程度: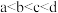 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】百里酚蓝(以下记为H2A)是一种有机弱酸,结构如图1所示,其电离平衡可表示为: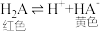

25°C时0.1 mol·L-1溶液中,H2A、HA-、A2-的分布分数 δ与pH的变化关系如图2所示。 已知: δ(A2-) =

下列说法不正确的是
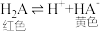

25°C时0.1 mol·L-1溶液中,H2A、HA-、A2-的分布分数 δ与pH的变化关系如图2所示。 已知: δ(A2-) =


下列说法不正确的是
| A.溶液由黄色变为蓝色原因是酚羟基发生了变化 |
B.δ(HA-)=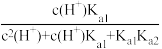 |
| C.pH=7.0:c(HA-) >c(A2-) >c(H2A) >c(H+) =c(OH- ) |
| D.NaOH 滴定CH3COOH,可用H2A作指示剂,溶液由红色变为橙色且半分钟内不复原即为滴定终点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,向浓度均为 的两种钾盐
的两种钾盐 溶液中加水,溶液的
溶液中加水,溶液的 与稀释倍数
与稀释倍数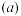 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 的两种钾盐
的两种钾盐 溶液中加水,溶液的
溶液中加水,溶液的 与稀释倍数
与稀释倍数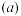 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是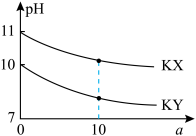
A.常温下, 的水解常数 的水解常数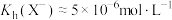 |
B.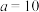 时, 时, 溶液中 溶液中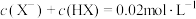 |
C.HY溶液可以与 溶液反应 溶液反应 |
D.浓度均为 的 的 和 和 溶液中离子总浓度: 溶液中离子总浓度: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】苯胺(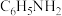 )是一种有机弱碱,可与盐酸反应生成盐酸盐(
)是一种有机弱碱,可与盐酸反应生成盐酸盐(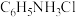 )。下列叙述正确的是
)。下列叙述正确的是
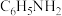 )是一种有机弱碱,可与盐酸反应生成盐酸盐(
)是一种有机弱碱,可与盐酸反应生成盐酸盐(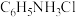 )。下列叙述正确的是
)。下列叙述正确的是A.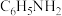 中碳原子的杂化轨道类型为 中碳原子的杂化轨道类型为 |
B.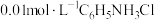 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
C.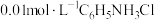 水溶液中: 水溶液中: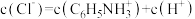 |
D.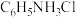 在水中的电离方程式为: 在水中的电离方程式为: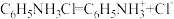 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】25°C时,向某Na2CO3溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分情况如图所示。

下列说法正确的是

下列说法正确的是
A.Na2CO3溶液中: c(Na+)> c(OH—)> c( )> c( )> c( )> c(H+) )> c(H+) |
B.pH=8时,c(Na+)= c( ) ) |
C.pH= 7时,c(Na+)= c( ) + 2c( ) + 2c( ) ) |
D.25 °C时, + H2O + H2O   + OH—的平衡常数为10-4 + OH—的平衡常数为10-4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】探究草酸(H2C2O4)的性质,室温下进行以下两组实验:(已知:室温下,H2C2O4的电离平衡常数Ka1=5.0×10-2,Ka2=5.4×10-5)
下列有关实验说法正确的是( )
| 实验 | 装置 | 试剂a |
| ① |  | 0.1mol·L-1NaOH溶液VmL |
| ② | 0.01mol·L-1酸性KMnO4溶液mL |
| A.若实验①中V=2,则混合后溶液中:c(C2O42-)>c(H2C2O4) |
| B.若实验①中V=4,则混合后溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-) |
| C.实验②反应的离子方程式为5C2O42-+16H++2MnO4-=2Mn2++10CO2↑+8H2O |
| D.若实验②测得KMnO4溶液的褪色时间为40s,则这段时间内的平均反应速率v(KMnO4)=2.5×10-4mol•L-1•s-1 |
您最近一年使用:0次

 溶液混合,若所得混合液的pH=7,则NaOH溶液与
溶液混合,若所得混合液的pH=7,则NaOH溶液与 溶液中,由水电离产生的c(OH)均为
溶液中,由水电离产生的c(OH)均为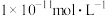
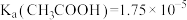 ,该温度下,用
,该温度下,用 的
的 溶液滴定
溶液滴定 的MOH溶液,滴定过程中加入
的MOH溶液,滴定过程中加入 的关系如图所示[
的关系如图所示[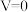 时,
时,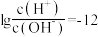 ]。下列说法错误的是
]。下列说法错误的是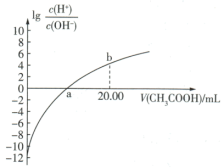
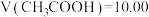

 的水解平衡常数约为
的水解平衡常数约为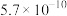
 的是
的是 的氨水和硫酸铵的混合溶液中,铵根离子和硫酸根离子浓度之比
的氨水和硫酸铵的混合溶液中,铵根离子和硫酸根离子浓度之比 的
的 溶液与
溶液与 溶液中溶质的物质的量浓度之比
溶液中溶质的物质的量浓度之比

