下列叙述及解释正确的是
A.2NO2(红棕色) N2O4(无色) △H<0,在达到平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 N2O4(无色) △H<0,在达到平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 |
B.H2(g)+I2(g) 2HI(g) △H<0,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 2HI(g) △H<0,在达到平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 |
C.N2(g)+3H2(g) 2NH3(g),在达到平衡后,保持压强不变,充入He,平衡向左移动 2NH3(g),在达到平衡后,保持压强不变,充入He,平衡向左移动 |
D.2C(s)+O2(g) 2CO(g)在达到平衡后,加入碳,平衡向正反应方向移动 2CO(g)在达到平衡后,加入碳,平衡向正反应方向移动 |
更新时间:2022-04-14 15:04:52
|
相似题推荐
【推荐1】在容积为2 L的恒容密闭容器中充入P(g)和Q(g),发生反应P(g)+2Q(g)⇌3R(g)+4S(s) ΔH.所得数据如下表。下列说法不正确的是
| 组号 | 温度/℃ | 起始量/mol | 平衡量/mol | ||
| n(P) | n(Q) | n(R) | n(S) | ||
| ① | 500 | 0.10 | 0.80 | 0.24 | 0.32 |
| ② | 500 | 0.20 | 1.60 | x | 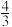 x x |
| ③ | 700 | 0.10 | 0.30 | 0.18 | 0.24 |
| A.该反应的ΔH>0 |
| B.反应达到平衡后增大压强,平衡逆向移动 |
| C.②中x的值可以算出 |
| D.700℃,若P、Q、R、S的物质的量均为0.2 mol,则平衡正移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】燃煤和工业生产中产生的 过量排放会形成酸雨。
过量排放会形成酸雨。 是重要的化工原料,可作漂白剂。在接触法制硫酸的工业中,
是重要的化工原料,可作漂白剂。在接触法制硫酸的工业中, 发生的反应为:
发生的反应为:
 。下图表示在有、无催化剂条件下
。下图表示在有、无催化剂条件下 氧化成
氧化成 过程中能量的变化。450℃、
过程中能量的变化。450℃、 催化时,该反应机理为:
催化时,该反应机理为:

反应①

反应②

下列说法正确的是
 过量排放会形成酸雨。
过量排放会形成酸雨。 是重要的化工原料,可作漂白剂。在接触法制硫酸的工业中,
是重要的化工原料,可作漂白剂。在接触法制硫酸的工业中, 发生的反应为:
发生的反应为:
 。下图表示在有、无催化剂条件下
。下图表示在有、无催化剂条件下 氧化成
氧化成 过程中能量的变化。450℃、
过程中能量的变化。450℃、 催化时,该反应机理为:
催化时,该反应机理为:
反应①


反应②


下列说法正确的是
A. 催化时,反应②的速率大于反应① 催化时,反应②的速率大于反应① |
B. |
C.升高温度,反应 的化学平衡常数增大 的化学平衡常数增大 |
D.增大压强或选择更高效的催化剂,可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一定温度下,某同学欲探究浓度对化学平衡的影响,设计实验如下:
Ⅰ.向5mL0.05mol·L-1FeCl3溶液中加入5mL0.05mol·L-1KI溶液,反应达到平衡后分成两等份。
Ⅱ.向其中一份中加入KSCN溶液,变红,加入CCl4,振荡,静置,下层显极浅的紫色。
Ⅲ.向另外一份中加入CCl4,振荡,静置,下层显紫色。
下列说法错误的是
Ⅰ.向5mL0.05mol·L-1FeCl3溶液中加入5mL0.05mol·L-1KI溶液,反应达到平衡后分成两等份。
Ⅱ.向其中一份中加入KSCN溶液,变红,加入CCl4,振荡,静置,下层显极浅的紫色。
Ⅲ.向另外一份中加入CCl4,振荡,静置,下层显紫色。
下列说法错误的是
A.实验Ⅰ中发生的反应为2Fe3++2I- 2Fe2++I2 2Fe2++I2 |
| B.水溶液中的c平(I-):Ⅱ<Ⅲ |
| C.水溶液中的c平(Fe3+):Ⅰ>Ⅱ |
| D.若在实验Ⅰ中加入少量FeCl3固体,c平(Fe2+)会增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列措施或事实不能用勒夏特列原理解释的是
| A.新制的氯水在光照下颜色变浅 |
| B.NO2和N2O4平衡混合气缩小体积加压后颜色先变深后变浅一点 |
| C.高锰酸钾溶液与草酸发生化学反应刚开始缓慢,随后反应迅速加快 |
| D.硫酸工业上SO2氧化成SO3,通入过量的空气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列能用勒夏特列原理解释的是
| A.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| B.工业合成氨的反应为放热反应,为提高氨的产率,使用高温的条件 |
| C.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D.H2、I2、HI平衡混和气加压后颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】对于平衡体系mA(g)+nB(g) pC(g)+qD(g) ΔH<0。下列结论中不正确的是( )
pC(g)+qD(g) ΔH<0。下列结论中不正确的是( )
 pC(g)+qD(g) ΔH<0。下列结论中不正确的是( )
pC(g)+qD(g) ΔH<0。下列结论中不正确的是( )| A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
| C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a |
| D.若温度不变时,压强增大到原来的2倍,达到新平衡时,反应物、生成物总物质的量一定比原来的1/2要小 |
您最近一年使用:0次



