“空气变馒头不是梦”,中国科学家在国际上首次实现了 到淀粉的从头合成,不依赖植物光合作用,原料只需
到淀粉的从头合成,不依赖植物光合作用,原料只需 、
、 和电,相关成果发表在《科学》上。请回答下列问题:
和电,相关成果发表在《科学》上。请回答下列问题:
(1) 的空间构型为
的空间构型为_______ ,其中C原子的杂化方式为_______ 。基态氧原子的最外层的成单电子和成对电子之比为_______ 。
(2)试推测
_______ (填“能”或“不能”)溶于 ,理由是
,理由是_______ 。
(3)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是_______ (用离子方程式表示)。
(4)淀粉在一定条件下可水解成葡萄糖( ),葡萄糖分子中键角
),葡萄糖分子中键角
_______ 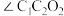 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(5)干冰的晶胞结构如下图所示,1个 分子周围与其距离相等且最近的
分子周围与其距离相等且最近的 分子个数为
分子个数为_______ 。若干冰晶胞沿x轴投影,试在图中画出 的投影位置(用“·”表示
的投影位置(用“·”表示 分子)。
分子)。_______
 到淀粉的从头合成,不依赖植物光合作用,原料只需
到淀粉的从头合成,不依赖植物光合作用,原料只需 、
、 和电,相关成果发表在《科学》上。请回答下列问题:
和电,相关成果发表在《科学》上。请回答下列问题:(1)
 的空间构型为
的空间构型为(2)试推测

 ,理由是
,理由是(3)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是
(4)淀粉在一定条件下可水解成葡萄糖(
 ),葡萄糖分子中键角
),葡萄糖分子中键角
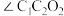 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(5)干冰的晶胞结构如下图所示,1个
 分子周围与其距离相等且最近的
分子周围与其距离相等且最近的 分子个数为
分子个数为 的投影位置(用“·”表示
的投影位置(用“·”表示 分子)。
分子)。
2022·河北唐山·三模 查看更多[3]
河北省唐山市2022届高三第三次模拟考试化学试题(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编江西省南昌市第十九中学2022-2023学年高二下学期3月第一次月考化学试卷
更新时间:2022-05-21 09:06:12
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D是元素周期表中原子序数依次递增的前四周期元素。A原子最外层电子数为内层电子数的3倍;B的焰色反应呈黄色;C未成对电子数与B相同,其氢化物是一种强酸;D是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
(1)D的基态原子价层电子排布式为___________ 。
(2)C的氢化物的沸点比其上一周期同族元素的氢化物低,是因为_____ 。
(3)A、C电负性大小顺序是_____ (用元素符号表示),C的最高价含氧酸根的空间构型为_____ ,其中心原子的杂化类型为_____ 。
(4)BC形成的晶体在50-300GPa的高压下可以和B或C的单质继续反应,形成不同组成、不同结构的晶体。下图给出其中三种不同晶体的晶胞(小球代表B离子,大球代表C离子),试写出其化学式①___________ ②___________ ③___________ 。

(5)在超高压下(300GPa),B和氦可形成化合物。结构中,B离子按简单立方排布,形成B8立方体空隙(如下图所示),电子对(2e-)和氦原子交替分布填充在立方体的中心。

已知晶胞边长a 约为400 pm,计算此结构中B与He的间距d___________ (单位:pm)和晶体的密度ρ___________ (单位: g/cm3)。
(1)D的基态原子价层电子排布式为
(2)C的氢化物的沸点比其上一周期同族元素的氢化物低,是因为
(3)A、C电负性大小顺序是
(4)BC形成的晶体在50-300GPa的高压下可以和B或C的单质继续反应,形成不同组成、不同结构的晶体。下图给出其中三种不同晶体的晶胞(小球代表B离子,大球代表C离子),试写出其化学式①

(5)在超高压下(300GPa),B和氦可形成化合物。结构中,B离子按简单立方排布,形成B8立方体空隙(如下图所示),电子对(2e-)和氦原子交替分布填充在立方体的中心。

已知晶胞边长a 约为400 pm,计算此结构中B与He的间距d
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为_________ ;
(2)SiO2晶体的空间构型是____________ ,氧原子的杂化方式为___________ ,硅氧之间原子轨道的重叠方式是___________ 。
(3)C、Si、Sn三种元素的单质中,属于分子晶体的是___________ (填化学式)。
(4)CCl4与水不互溶发生分层,SiCl4与CCl4分子结构相似,但遇水极易发生水解反应,导致二者性质不同的原因是________________ 。
(5)金刚石的晶胞结构如右图。 该晶胞中C原子数为
该晶胞中C原子数为_____ 。若金刚石晶胞中立方体的边长为a pm,阿伏伽德罗常数为NA,则金刚石的密度为________ g·cm-3。(用含a、NA的式子表示)
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为
(2)SiO2晶体的空间构型是
(3)C、Si、Sn三种元素的单质中,属于分子晶体的是
(4)CCl4与水不互溶发生分层,SiCl4与CCl4分子结构相似,但遇水极易发生水解反应,导致二者性质不同的原因是
(5)金刚石的晶胞结构如右图。
 该晶胞中C原子数为
该晶胞中C原子数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。

ATP分子中属于sp2杂化的N原子是______ (填序号)。
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 中N原子均为sp3杂化,请推测N4H
中N原子均为sp3杂化,请推测N4H 的结构式:
的结构式:______ 。
(3)某种磁性氮化铁的晶胞结构如图所示:

①基态Fe原子的电子排布式为______ 。
②该化合物的化学式为______ 。
③若晶胞底面边长为anm,高为cnm,NA为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为______ g•cm-3(用含a、c、NA的代数式表示)。
(1)ATP(三磷酸腺苷)是一种高能磷酸化合物,在细胞中,它与ADP的相互转化实现贮能和放能,从而保证了细胞各项生命活动的能量供应。

ATP分子中属于sp2杂化的N原子是
(2)2001年德国专家从硫酸铵中检出一种组成为N4H4(SO4)2的物质,经测定,该物质易溶于水,在水中以SO
 和N4H
和N4H 两种离子的形式存在。N4H
两种离子的形式存在。N4H 中N原子均为sp3杂化,请推测N4H
中N原子均为sp3杂化,请推测N4H 的结构式:
的结构式:(3)某种磁性氮化铁的晶胞结构如图所示:

①基态Fe原子的电子排布式为
②该化合物的化学式为
③若晶胞底面边长为anm,高为cnm,NA为阿伏加德罗常数的值,则该磁性氮化铁的晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】磷酸铁锂电池是绿色环保型电池,电池的总反应为:Li1-xFePO4+LixC6=LiFePO4+C6。
(1)LiFePO4中Fe2+的核外电子排布式为___ ,该电池反应物中所涉及第二周期元素的第一电离能由大到小的顺序是___ (用元素符号表示)。
(2)H3PO4和H2CO3中P和C原子的杂化方式___ (填“相同”或“不相同”)。
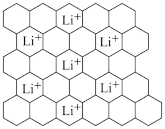
(3)石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物,某石墨嵌入化合物的平面结构如图所示,则x=___ ;若每个六元环都对应一个Li+,则化学式为___ 。
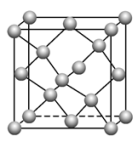
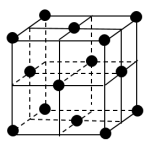
(4)碳的另一种同素异形体——金刚石,其晶胞如图所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是图___ (从A~D图中选填)。
(5)某金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,阴离子是由12个硼原子和12个氢原子所构成的离子团。阴离子在晶胞中位置如图所示,其堆积方式为___ ,Li+占据阴离子组成的所有正四面体空隙中心,该化合物的化学式为___ (用最简整数比表示)。假设晶胞边长为anm,则两个最近的Li+的距离为___ nm。
(1)LiFePO4中Fe2+的核外电子排布式为
(2)H3PO4和H2CO3中P和C原子的杂化方式
(3)石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物,某石墨嵌入化合物的平面结构如图所示,则x=

(4)碳的另一种同素异形体——金刚石,其晶胞如图所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是图

A.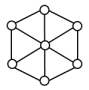 | B.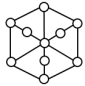 | C. | D. |

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】地壳中含量排在前七位的元素分别是O、Si、Al、Fe、Ca、Na、K,占到地壳总质量的95%以上。回答下列问题:
(1)铁元素的基态原子价电子排布式为_______ 。
(2)“棕色环”现象是检验溶液中 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 、随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为
、随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为 。
。
① 中S元素采取
中S元素采取_______ 杂化,其立体构型为_______ (填名称)。
② 中含有的作用力类型有(填序号)
中含有的作用力类型有(填序号)________ 。
a.离子键 b.金属键 c.极性键 d.非极性键 e.配位键
③ 中Fe元素的化合价为+1,则铁的配体为
中Fe元素的化合价为+1,则铁的配体为_______ (填化学式)。
④ 易被氧化成
易被氧化成 ,试从原子结构角度解释:
,试从原子结构角度解释:_______ 。
(3)硅酸盐中的硅酸根通常以[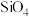 ]四面体(如图甲)的方式形成链状、环状或网络状复杂阴离子。图乙为一种环状硅酸根离子,写出其化学式:
]四面体(如图甲)的方式形成链状、环状或网络状复杂阴离子。图乙为一种环状硅酸根离子,写出其化学式:_______ 。

(4)离子晶体能否成为快离子导体取决于离子能否离开原位迁移到距离最近的空位上去,迁移过程中必须经过由其他离子围成的最小窗孔。KCl属于NaCl型晶体, 占据由
占据由 围成的八面体空隙。已知
围成的八面体空隙。已知 和
和 的半径分别为0.130nm和0.170nm,晶体中阴阳离子紧密相切。若KCl晶体产生了阳离子空位(如图丙),请计算
的半径分别为0.130nm和0.170nm,晶体中阴阳离子紧密相切。若KCl晶体产生了阳离子空位(如图丙),请计算 围成的最小窗孔的半径为
围成的最小窗孔的半径为_______ nm,则KCl晶体_______ (填“能”或“不能”)成为快离子导体。(已知: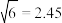 )
)

(1)铁元素的基态原子价电子排布式为
(2)“棕色环”现象是检验溶液中
 的一种方法。向含有
的一种方法。向含有 溶液的试管中加入
溶液的试管中加入 、随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为
、随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为 。
。①
 中S元素采取
中S元素采取②
 中含有的作用力类型有(填序号)
中含有的作用力类型有(填序号)a.离子键 b.金属键 c.极性键 d.非极性键 e.配位键
③
 中Fe元素的化合价为+1,则铁的配体为
中Fe元素的化合价为+1,则铁的配体为④
 易被氧化成
易被氧化成 ,试从原子结构角度解释:
,试从原子结构角度解释:(3)硅酸盐中的硅酸根通常以[
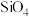 ]四面体(如图甲)的方式形成链状、环状或网络状复杂阴离子。图乙为一种环状硅酸根离子,写出其化学式:
]四面体(如图甲)的方式形成链状、环状或网络状复杂阴离子。图乙为一种环状硅酸根离子,写出其化学式:
(4)离子晶体能否成为快离子导体取决于离子能否离开原位迁移到距离最近的空位上去,迁移过程中必须经过由其他离子围成的最小窗孔。KCl属于NaCl型晶体,
 占据由
占据由 围成的八面体空隙。已知
围成的八面体空隙。已知 和
和 的半径分别为0.130nm和0.170nm,晶体中阴阳离子紧密相切。若KCl晶体产生了阳离子空位(如图丙),请计算
的半径分别为0.130nm和0.170nm,晶体中阴阳离子紧密相切。若KCl晶体产生了阳离子空位(如图丙),请计算 围成的最小窗孔的半径为
围成的最小窗孔的半径为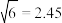 )
)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】Co元素的某些化合物在电池、光电材料、催化剂等方面有广泛应用。回答下列问题:
(1)一种具有光催化作用的配合物A结构简式如图所示:

①与Co同周期,基态原子有1个未成对电子的元素有___________ 种。
②配离子 的空间构型为
的空间构型为___________ ,钴元素价态为___________ ,通过螯合作用形成的配位键有___________ 个。
③配合物A无顺磁性,则中心离子的杂化方式为___________ (填标号)。(若中心离子具有单电子,则配合物为顺磁性物质。)
A. B.
B. C.
C. D.
D.
④咪唑( )具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是________ 。
(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为___________ 。 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  (用计算式表示)。
(用计算式表示)。
(1)一种具有光催化作用的配合物A结构简式如图所示:

①与Co同周期,基态原子有1个未成对电子的元素有
②配离子
 的空间构型为
的空间构型为③配合物A无顺磁性,则中心离子的杂化方式为
A.
 B.
B. C.
C. D.
D.
④咪唑(
 )具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的芳香性,①号N比②号N更易与钴形成配位键的原因是(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用计算式表示)。
(用计算式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铜及其化合物在机械制造、国防建设中有着广泛的应用。回答下列问题:
(1)写出氢氧化铜溶于氨水的离子方程式___________ 。
(2)若[Cu(NH3)4]2+中两个NH3分别被C1-取代,能得到(m)、(n)两种不同结构的Cu(NH3)2C12:

则[Cu(NH3)4]2+的空间构型是___________ ;不同结构的Cu(NH3)2C12在水中的溶解度:(m)___________ (n)(填“>”、“=”或“<”)。
(3)Cu2+与乙二胺可形成如图所示配离子。

Cu2+的配位数为___________ ;Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是___________ (填字母代号)。
a.配位键 b.极性键 c.离子键 d.非极性键
(4)NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,理由是___________ 。
(1)写出氢氧化铜溶于氨水的离子方程式
(2)若[Cu(NH3)4]2+中两个NH3分别被C1-取代,能得到(m)、(n)两种不同结构的Cu(NH3)2C12:

则[Cu(NH3)4]2+的空间构型是
(3)Cu2+与乙二胺可形成如图所示配离子。

Cu2+的配位数为
a.配位键 b.极性键 c.离子键 d.非极性键
(4)NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,理由是
您最近一年使用:0次
【推荐2】现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个方向,C简单离子核外有___________ 种运动状态不同的电子。
(2) 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ , 分子的VSEPR模型名称为
分子的VSEPR模型名称为___________ 。
(4)下列气态分子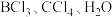 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为___________ 。
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外P电子数与s电子数相等 |
| C | 基态原子的价电子排布为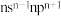 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由(3)
 分子的空间构型为
分子的空间构型为 分子的VSEPR模型名称为
分子的VSEPR模型名称为(4)下列气态分子
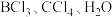 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】纯净四碘化锡(SnI4)为橙红色立方晶体,广泛应用于黑磷烯材料的制备。某同学在实验室中对其进行合成,实验报告如图:
根据该实验报告回答下列问题:
(1)分析药品性质可知SnI4可形成____ (填“分子晶体”“离子晶体”或“共价晶体”)。
(2)装置A的名称是____ 。
(3)装置C中盛放的药品可以是____ (填字母)。
a.碱石灰 b.五水硫酸铜 c.硅胶 d.块状无水氯化钙
(4)步骤①的目的是____ 。
(5)步骤⑤中,过滤得到残渣D的主要成分是____ 。该步骤中合并滤液和洗涤液后,“浓缩液体”所采用的实验操作名称是____ 。
(6)根据报告中提供的数据,此次实验的实际收率为____ 。
(7)书写实验报告后,该同学检查时发现未记录向球形冷凝管中通入冷凝水的操作,该操作应位于____ (填字母)。
a.步骤①之前 b.步骤①之后,②之前
c.步骤②之后,③之前 d.步骤③之后,④之前
(8)查阅文献发现,用乙酸乙酸酐( )代替CS2作反应溶剂能得到更高的产率,但需将锡粒处理为极碎的锡箔。若仍然用锡粒,反应引发后很容易停止,产生这种现象的原因是
)代替CS2作反应溶剂能得到更高的产率,但需将锡粒处理为极碎的锡箔。若仍然用锡粒,反应引发后很容易停止,产生这种现象的原因是____ 。
时间:2022年3月1日环境温度、压强:25℃、101kPa 【实验目的】四碘化锡的制备 【实验原理】Sn+2I2  SnI4 SnI4【药品性质】
 【实验步骤】 ①按装置图组装好仪器,打开玻璃塞B,向装置A中小心加入1.5mL无水乙醚,塞好玻璃塞B,用电吹风加热A的底部至乙醚完全挥发; ②快速打开玻璃塞B,将7.50g锡粒、25.40g碘、35.0mLCS2及一颗磁子(用于搅拌)加入装置A中; ③打开电加热磁力搅拌器缓慢加热引发反应,待装置A中混合物微沸后,停止加热,反应仍可继续进行; ④当混合物停止沸腾时,再次打开电加热磁力搅拌器,直至烧瓶中的蒸气和冷凝管滴下的液体都不再有碘的颜色为止; ⑤取下装置A,趁热迅速进行热过滤得到残渣D。用15.0mLCS2分多次洗涤装置A及残渣D,合并滤液和洗涤液,浓缩溶液体积至20.0mL,用冰水浴冷却; ⑥将析出的结晶过滤分离,得橙红色粉末25.08g。 |
(1)分析药品性质可知SnI4可形成
(2)装置A的名称是
(3)装置C中盛放的药品可以是
a.碱石灰 b.五水硫酸铜 c.硅胶 d.块状无水氯化钙
(4)步骤①的目的是
(5)步骤⑤中,过滤得到残渣D的主要成分是
(6)根据报告中提供的数据,此次实验的实际收率为
(7)书写实验报告后,该同学检查时发现未记录向球形冷凝管中通入冷凝水的操作,该操作应位于
a.步骤①之前 b.步骤①之后,②之前
c.步骤②之后,③之前 d.步骤③之后,④之前
(8)查阅文献发现,用乙酸乙酸酐(
 )代替CS2作反应溶剂能得到更高的产率,但需将锡粒处理为极碎的锡箔。若仍然用锡粒,反应引发后很容易停止,产生这种现象的原因是
)代替CS2作反应溶剂能得到更高的产率,但需将锡粒处理为极碎的锡箔。若仍然用锡粒,反应引发后很容易停止,产生这种现象的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】锗(Ge)、碲化镉(CdTe)等是优良的半导体材料。回答下列问题:
(1)Ge在元素周期表中的位置___________ ,Ge的逐级电离能I4≪I5的原因是___________ 。
(2)经X射线衍射实验证明在碲酸( )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为___________ 。
(3)锗可以形成无机化合物 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为___________ ,锗也可以形成类似于烷烃结构的 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为___________ , 该分子中含有的
该分子中含有的 键数目为
键数目为___________ 。
(4)锗的氯化物 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是___________ , 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有___________ 个。
(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为___________ 空隙(填几何构型名称),若CdTe的摩尔质量为 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离___________ nm。(用含M、 、
、 的代数式表示)
的代数式表示)

(1)Ge在元素周期表中的位置
(2)经X射线衍射实验证明在碲酸(
 )分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为
)分子内的6个羟基排列在碲原子的周围呈八面体结构,碲酸中碲原子的价层电子对数为(3)锗可以形成无机化合物
 ,化合物中阴离子的空间构型为
,化合物中阴离子的空间构型为 (n一般小于5),化合物中Ge的杂化类型为
(n一般小于5),化合物中Ge的杂化类型为 该分子中含有的
该分子中含有的 键数目为
键数目为(4)锗的氯化物
 常温下为无色液体,其沸点高于
常温下为无色液体,其沸点高于 ,原因是
,原因是 晶体采用ABC式的密堆积方式,则距离一个
晶体采用ABC式的密堆积方式,则距离一个 最近且等距离的
最近且等距离的 有
有(5)CdTe的晶胞属立方晶系,晶胞如图所示,Te原子填充在Cd原子围成的空隙中该空隙的类型为
 ,该晶体的密度为
,该晶体的密度为 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则最近的两个Te原子的距离
,则最近的两个Te原子的距离 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硅、锗(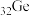 ,熔点937℃)和镓(
,熔点937℃)和镓( )都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
(1)硅的基态原子价层电子轨道表示式_______ ,镓的基态原子电子排布式_______ 。
(2)硅和锗与氯元素都能形成氯化物,沸点 ,解释原因。
,解释原因。_______ 。
(3)镓( )的同族元素
)的同族元素 ,其气态单个
,其气态单个 分子的空间构型为
分子的空间构型为_______ ,事实证明熔融态氯化铝可挥发出二聚分子 ,其结构如图所示,请在图上用“→”标出其配位键
,其结构如图所示,请在图上用“→”标出其配位键_______ 。 和
和 都是第3周期元素,在第3周期所有元素中,第一电离能比
都是第3周期元素,在第3周期所有元素中,第一电离能比 高的有
高的有_______ 种。

(4)自然界矿石中锗浓度非常低,因此从锗加工废料(含游离态锗)中回收锗是一种非常重要的方法。下面是一种提取锗的流程:

① 溶液浸取含锗废料中的锗时发生反应的离子方程式为
溶液浸取含锗废料中的锗时发生反应的离子方程式为_______ ,为了加快 溶液浸取含锗废料的速率可以采取的措施有
溶液浸取含锗废料的速率可以采取的措施有_______ 。
②操作1和操作2是_______ 。
③ 的熔点为1086℃,利用氢气还原
的熔点为1086℃,利用氢气还原 ,每生成
,每生成 的
的 放出
放出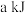 的热量,该反应的热化学方程式为
的热量,该反应的热化学方程式为_______ 。
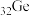 ,熔点937℃)和镓(
,熔点937℃)和镓( )都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。(1)硅的基态原子价层电子轨道表示式
(2)硅和锗与氯元素都能形成氯化物,沸点
 ,解释原因。
,解释原因。(3)镓(
 )的同族元素
)的同族元素 ,其气态单个
,其气态单个 分子的空间构型为
分子的空间构型为 ,其结构如图所示,请在图上用“→”标出其配位键
,其结构如图所示,请在图上用“→”标出其配位键 和
和 都是第3周期元素,在第3周期所有元素中,第一电离能比
都是第3周期元素,在第3周期所有元素中,第一电离能比 高的有
高的有
(4)自然界矿石中锗浓度非常低,因此从锗加工废料(含游离态锗)中回收锗是一种非常重要的方法。下面是一种提取锗的流程:

①
 溶液浸取含锗废料中的锗时发生反应的离子方程式为
溶液浸取含锗废料中的锗时发生反应的离子方程式为 溶液浸取含锗废料的速率可以采取的措施有
溶液浸取含锗废料的速率可以采取的措施有②操作1和操作2是
③
 的熔点为1086℃,利用氢气还原
的熔点为1086℃,利用氢气还原 ,每生成
,每生成 的
的 放出
放出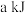 的热量,该反应的热化学方程式为
的热量,该反应的热化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】铁、钛、镁等金属及其化合物有广泛用途。回答下列问题:
(1)基态Ti原子的价电子排布图是_______ ,基态Fe原子共有_______ 种不同能级的电子。
(2)TiCl4是工业上制备钛的重要原料,常温下为无色液体,与SiCl4互为等电子体。TiCl4的空间构型是_______ 。TiCl4的沸点高于SiCl4,原因是_______ 。
(3)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如下图所示:

(R)
①组成R的元素中,电负性最大的是_______ (填元素符号),氧原子的杂化方式是_______ 。
②R中含有的化学键有_______ (填标号)。
A.π键 B.σ键 C.离子键 D.配位键 E.金属键
(4)铁镁合金是目前储氢密度最高的储氢材料之一,其晶胞结构如下图所示,晶体中Fe原子和Mg原子之间的最近距离为anm。储氢时,H2分子在晶胞的体心和棱的中点位置。

①该晶胞中Fe的配位数是_______ 。
②该合金储满氢后所得晶体的化学式是_______ ,理论上1cm3铁镁合金最多能储存H2_______ kg(用NA表示阿伏加德罗常数,写出计算表达式即可)。
(1)基态Ti原子的价电子排布图是
(2)TiCl4是工业上制备钛的重要原料,常温下为无色液体,与SiCl4互为等电子体。TiCl4的空间构型是
(3)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如下图所示:

(R)
①组成R的元素中,电负性最大的是
②R中含有的化学键有
A.π键 B.σ键 C.离子键 D.配位键 E.金属键
(4)铁镁合金是目前储氢密度最高的储氢材料之一,其晶胞结构如下图所示,晶体中Fe原子和Mg原子之间的最近距离为anm。储氢时,H2分子在晶胞的体心和棱的中点位置。

①该晶胞中Fe的配位数是
②该合金储满氢后所得晶体的化学式是
您最近一年使用:0次



