回答下列问题:
(1)钌(Ru)基催化剂在低温下活性高,工业上常用该催化剂替代铁系催化剂催化合成氨,以RuCl3/SiO2为模板制备钌基催化剂及催化合成氨过程如图所示,请回答下列问题。
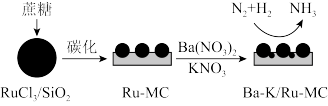
Ru在Fe的下一周期且与Fe同族。
①Ru在元素周期表中的位置为____ 。
②一个基态Fe2+和Fe3+未成对电子数之比为____ 。
③NH3的键角____ (填“大于”或“小于”)PH3,其原因为____ 。
④NO 有多种等电子体,其中和NO
有多种等电子体,其中和NO 互为等电子体的分子有
互为等电子体的分子有___ 。
⑤多原子分子中,若原子都在同一平面上,且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成大π键。大π元键可用π 表示,其中m、n分别代表参与形成大π元键的原子个数和电子个数,则NO
表示,其中m、n分别代表参与形成大π元键的原子个数和电子个数,则NO 的大π元键可表示为
的大π元键可表示为___ 。
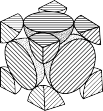
(2)经X射线衍射测定发现,晶体钻在417℃以上堆积方式的剖面图如图所示,则晶体钴堆积方式为____ ,钴原子的配位数是____ ,若该堆积方式下的晶胞参数为acm,(阿伏加德罗常数为NA),则钴原子的半径为___ pm。
(1)钌(Ru)基催化剂在低温下活性高,工业上常用该催化剂替代铁系催化剂催化合成氨,以RuCl3/SiO2为模板制备钌基催化剂及催化合成氨过程如图所示,请回答下列问题。
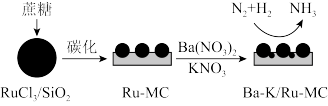
Ru在Fe的下一周期且与Fe同族。
①Ru在元素周期表中的位置为
②一个基态Fe2+和Fe3+未成对电子数之比为
③NH3的键角
④NO
 有多种等电子体,其中和NO
有多种等电子体,其中和NO 互为等电子体的分子有
互为等电子体的分子有⑤多原子分子中,若原子都在同一平面上,且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成大π键。大π元键可用π
 表示,其中m、n分别代表参与形成大π元键的原子个数和电子个数,则NO
表示,其中m、n分别代表参与形成大π元键的原子个数和电子个数,则NO 的大π元键可表示为
的大π元键可表示为(2)经X射线衍射测定发现,晶体钻在417℃以上堆积方式的剖面图如图所示,则晶体钴堆积方式为

更新时间:2022-06-15 23:47:00
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
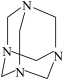
【推荐1】(1)盐酸中加入六次甲基四胺对钢铁有一定缓蚀作用,如图为其结构简式,其分子式为(CH2)6N4,其中碳原子采用________ 杂化,其缓蚀作用是因为分子中________ 原子的孤对电子能与铁原子形成配位键,覆盖在钢铁表面。
(2)CO与N2属于等电子体,1个CO分子中含有的π键数目是________ 个。C、N、O三种元素的第一电离能最大的是________ 。
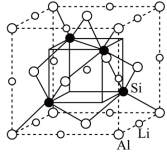
(3)如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。
①该化合物的化学式是________ 。
②Al元素基态原子的电子排布式是________ 。
③已知晶胞边长为5.93×10-8 cm,Si与Al之间的共价键键长是______ cm(只要求列算式,不必计算出数值,下同),晶体的密度是______ g·cm-3

(2)CO与N2属于等电子体,1个CO分子中含有的π键数目是
(3)如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。
①该化合物的化学式是
②Al元素基态原子的电子排布式是
③已知晶胞边长为5.93×10-8 cm,Si与Al之间的共价键键长是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】Ⅰ.元素Fe、C、卤素元素等形成的材料在工业、生活、国防中有很大的作用。请回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有_______ 种,实验室常用邻二氮菲(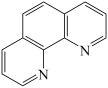 )检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为
)检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为_______ 。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(2)拟卤素( CN)2、( SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H- S- C≡N )的沸点低于异硫氰酸(H -N=C=S),其原因是_______ 。
(3)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为_______ ; 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为_______ 。
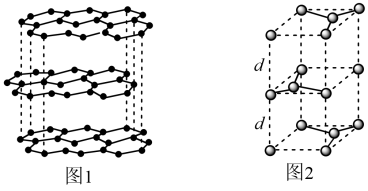
(4)碳的一种同素异形体---石墨,其晶体结构及晶胞如图1、图2所示。则石墨晶胞含碳原子个数为_______ 个。已知石墨的密度为ρg· cm-3 ,C-C键键长为r cm ,阿伏加德罗常数的值为NA,计算石墨晶体的层间距d为_______ cm。
(1)基态Fe原子核外电子的空间运动状态有
 )检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为
)检验Fe2+ ,生成橙红色的邻二氮菲亚铁络离子,邻二氮菲中N原子参与杂化的原子轨道为Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(2)拟卤素( CN)2、( SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H- S- C≡N )的沸点低于异硫氰酸(H -N=C=S),其原因是
(3)卤化物RbICl2在加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为
 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为(4)碳的一种同素异形体---石墨,其晶体结构及晶胞如图1、图2所示。则石墨晶胞含碳原子个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】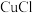 和
和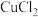 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①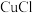 可以由
可以由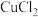 用适当的还原剂如
用适当的还原剂如 等还原制得:
等还原制得:
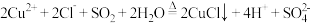
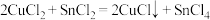
②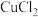 溶液与乙二胺
溶液与乙二胺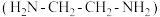 可形成配离子:
可形成配离子:
请回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为_______ ;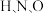 三种元素的电负性由大到小的顺序是
三种元素的电负性由大到小的顺序是_______ 。
(2)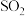 分子的空间构型为
分子的空间构型为_______ ;与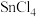 互为等电子体的一种离子的化学式为
互为等电子体的一种离子的化学式为_______ 。
(3)乙二胺分子中氮原子轨道的杂化类型为_______ 。乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_______ 。
(4)②中所形成的配离子中含有的化学键类型有_______。
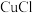 和
和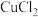 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:①
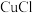 可以由
可以由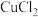 用适当的还原剂如
用适当的还原剂如 等还原制得:
等还原制得: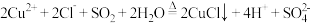
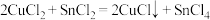
②
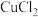 溶液与乙二胺
溶液与乙二胺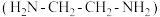 可形成配离子:
可形成配离子:
请回答下列问题:
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为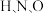 三种元素的电负性由大到小的顺序是
三种元素的电负性由大到小的顺序是(2)
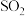 分子的空间构型为
分子的空间构型为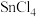 互为等电子体的一种离子的化学式为
互为等电子体的一种离子的化学式为(3)乙二胺分子中氮原子轨道的杂化类型为
 均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是(4)②中所形成的配离子中含有的化学键类型有_______。
| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为_____ 。
(2)NO3-中氮原子轨道的杂化类型是_____ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为_____ 。
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是_____ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有_____ 。
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为_____ 。

(1)Mn3+基态核外电子排布式为
(2)NO3-中氮原子轨道的杂化类型是
(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】近期,中国中科院天津工业生物技术研究所,首次实现人工通过二氧化碳合成淀粉。请回答下列问题:
(1)基态碳原子的核外电子排布图为___________ 。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为___________ 。
(3)①结合如表所示键能数据,分析CO比 相对更活泼的原因是
相对更活泼的原因是___________ ;
②Si的氧化物( )比干冰(
)比干冰( )熔点高的原因是
)熔点高的原因是___________ ;
③甲醇( )是
)是 合成淀粉的中间产物,与甲醇(
合成淀粉的中间产物,与甲醇( )互为等电子体的有机物分子式为
)互为等电子体的有机物分子式为___________ 。
(4)葡萄糖( )也是
)也是 合成淀粉的中间产物。若2个葡萄糖分子间脱水形成麦芽糖(
合成淀粉的中间产物。若2个葡萄糖分子间脱水形成麦芽糖(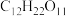 ),10个葡萄糖分子通过分子间脱水所形成的链状化合物的分子式为___________。
),10个葡萄糖分子通过分子间脱水所形成的链状化合物的分子式为___________。
(5)一种新型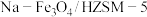 多功能复合催化剂成功实现了
多功能复合催化剂成功实现了 直接加氢制取高辛烷值汽油。该催化剂成分
直接加氢制取高辛烷值汽油。该催化剂成分 的晶胞如图所示:
的晶胞如图所示:
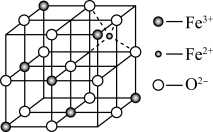
①晶胞中 处于
处于 围成的
围成的___________ (填“正四面体”“正八面体”或“正十二面体”)空隙;
②若晶胞体对角线为anm,阿伏加德罗常数值为 ,晶体的密度为
,晶体的密度为___________  写出表达式)。
写出表达式)。
(1)基态碳原子的核外电子排布图为
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为(3)①结合如表所示键能数据,分析CO比
 相对更活泼的原因是
相对更活泼的原因是| CO | C—O |  | 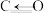 |
键能/( ) ) | 357.7 | 798.9 | 1071.9 |
| N2 | N—N |  |  |
键能/( ) ) | 154.8 | 418.4 | 941.7 |
 )比干冰(
)比干冰( )熔点高的原因是
)熔点高的原因是③甲醇(
 )是
)是 合成淀粉的中间产物,与甲醇(
合成淀粉的中间产物,与甲醇( )互为等电子体的有机物分子式为
)互为等电子体的有机物分子式为(4)葡萄糖(
 )也是
)也是 合成淀粉的中间产物。若2个葡萄糖分子间脱水形成麦芽糖(
合成淀粉的中间产物。若2个葡萄糖分子间脱水形成麦芽糖(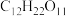 ),10个葡萄糖分子通过分子间脱水所形成的链状化合物的分子式为___________。
),10个葡萄糖分子通过分子间脱水所形成的链状化合物的分子式为___________。A.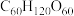 |
B. |
C.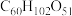 |
D.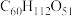 |
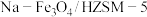 多功能复合催化剂成功实现了
多功能复合催化剂成功实现了 直接加氢制取高辛烷值汽油。该催化剂成分
直接加氢制取高辛烷值汽油。该催化剂成分 的晶胞如图所示:
的晶胞如图所示:
①晶胞中
 处于
处于 围成的
围成的②若晶胞体对角线为anm,阿伏加德罗常数值为
 ,晶体的密度为
,晶体的密度为 写出表达式)。
写出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
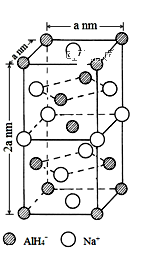
【推荐3】氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15. 2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如图所示。
(1)基态Ti原子的价电子轨道排布图为___________ 。
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于_____ 晶体,其电子式为____________ 。
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为______________ (标明配位键)
(4)AlH4-中,Al的轨道杂化方式为_______ ;例举与AlH4-空间构型相同的两种离子_________ (填化学式)。
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有______ 个;NaAlH4晶体的密度为______________ g·cm-3(用含a的代数式表示)。

(1)基态Ti原子的价电子轨道排布图为
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为
(4)AlH4-中,Al的轨道杂化方式为
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)基态Cu原子的价层电子的轨道表达式为___________ 。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体H2S产生。
①H2S分子的立体构型是___________ ,中心原子杂化类型为___________ ,属于___________ (填极性"或“非极性”)分子。
②H2S分子量比水大,沸点却比水低,主要原因是___________ 。
(3)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为___________ ,键角___________ 120°(填“>”或“=”或“<"),原因是___________ 。
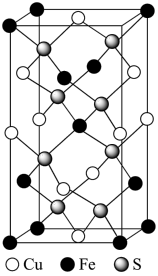
(4)CuFeS2晶胞结构如图所示。___________ 。
②已知:晶胞为长方体,三个边长分别为anm、bnm、cnm,NA为阿伏加德罗常数,CuFeS2晶体的密度___________ g·cm-3(列出计算式)。(1nm=10-9m)
(1)基态Cu原子的价层电子的轨道表达式为
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体H2S产生。
①H2S分子的立体构型是
②H2S分子量比水大,沸点却比水低,主要原因是
(3)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
(4)CuFeS2晶胞结构如图所示。
②已知:晶胞为长方体,三个边长分别为anm、bnm、cnm,NA为阿伏加德罗常数,CuFeS2晶体的密度
您最近一年使用:0次
【推荐2】氮及其化合物在生产生活中应用广泛。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式____ ;基态铬、氮原子的核外未成对电子数之比为____ 。
(2)氮化铬的晶体结构类型与氯化钠相同,但氮化铬熔点(1282℃)比氯化钠 (801'C)的高,主要原因是________ 。
(3)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为_______ ,其中NH4+的空间构型为____________
(4)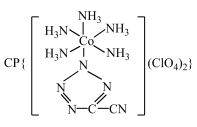 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由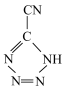 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为 _______ , CP的中心Co3+的配位数为 ______ 。
(5)铁氮化合物是磁性材料研究中的热点课题之一,因其具有高饱和磁化强度、低矫顽力,有望获得较高的微波磁导率,具有极大的市场潜力,其四子格结构如图所示,已知晶体密度为ρg∙cm-3,阿伏加 德罗常数为NA。
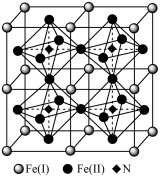
①写出氮化铁中铁的堆积方式为____ 。
②该化合物的化学式为___ 。
③计算出 Fe(II)围成的八面体的体积为____ cm3。
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式
(2)氮化铬的晶体结构类型与氯化钠相同,但氮化铬熔点(1282℃)比氯化钠 (801'C)的高,主要原因是
(3)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为
(4)
 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为 (5)铁氮化合物是磁性材料研究中的热点课题之一,因其具有高饱和磁化强度、低矫顽力,有望获得较高的微波磁导率,具有极大的市场潜力,其四子格结构如图所示,已知晶体密度为ρg∙cm-3,阿伏加 德罗常数为NA。

①写出氮化铁中铁的堆积方式为
②该化合物的化学式为
③计算出 Fe(II)围成的八面体的体积为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Fe、Co、Ni 是几种重要的金属元素。请回答下列问题:
(1)基态 Ni 原子的价电子排布式为_______ 。
(2)Ni(CO)4常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4 是_______ 分子(填“极性”或“非极性”)。
(3)实验室常用 KSCN 溶液或苯酚(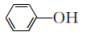 )检验
)检验 。
。
①第一电离能:N_______ O(填“>”或“<”)
②苯酚中碳原子杂化类型为_______ 。
(4)配位化合物 中心原子Co的配位数为
中心原子Co的配位数为_______ ,配位原子为_______ 。
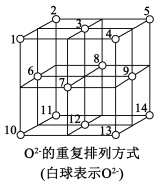
(5)如图所示,Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7围成)和正八面体空隙(3、6、7、8、9、12围成),Fe3O4中有一半的 填充在正四面体空隙中,
填充在正四面体空隙中, 和另一半
和另一半 填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为
填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为_______ 。
(6)已知 Ni可以形成多种氧化物,其中一种 NixO 晶体的晶胞结构为 NaCl 型,由于晶体缺陷导致x=0.88,晶胞参数为a nm,则晶体密度为_______ g·cm-3(NA 表示阿伏加德罗常数的值,只需列出表达式)。
(1)基态 Ni 原子的价电子排布式为
(2)Ni(CO)4常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4 是
(3)实验室常用 KSCN 溶液或苯酚(
 )检验
)检验 。
。①第一电离能:N
②苯酚中碳原子杂化类型为
(4)配位化合物
 中心原子Co的配位数为
中心原子Co的配位数为(5)如图所示,Fe3O4晶体中,O2-围成正四面体空隙(1、3、6、7围成)和正八面体空隙(3、6、7、8、9、12围成),Fe3O4中有一半的
 填充在正四面体空隙中,
填充在正四面体空隙中, 和另一半
和另一半 填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为
填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为
(6)已知 Ni可以形成多种氧化物,其中一种 NixO 晶体的晶胞结构为 NaCl 型,由于晶体缺陷导致x=0.88,晶胞参数为a nm,则晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。
(1)铜的熔点比钙的高,其原因是_______ 。
(2)金属铜的堆积方式为图中的_______ (填字母)。
A.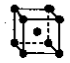 B.
B.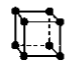 C.
C.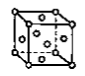 D.
D.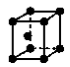
(3)某磷青铜晶胞结构如图所示。

①则其化学式为_______ 。
②该晶体中距离Cu原子最近的Sn原子有_______ 个,这些Sn原子所呈现的空间结构为_______ 。
(1)铜的熔点比钙的高,其原因是
(2)金属铜的堆积方式为图中的
A.
 B.
B. C.
C. D.
D.
(3)某磷青铜晶胞结构如图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
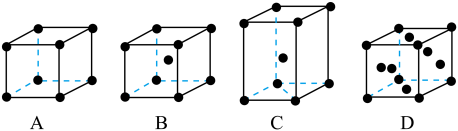
【推荐2】从下图中选择:
(1)金属钠的晶胞模型是____________ ,每个Na原子周围有________ 个紧邻的Na原子。
(2)金属铜的晶胞模型是____________ ,每个Cu原子周围有________ 个紧邻的Cu原子。
(3)金属导电靠_________________________________ , 电解质溶液导电靠____________________________ ;
(4)根据下列叙述,判断一定为金属晶体的是___________________ 。
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、导热性和延展性
(5)已知下列金属晶体: Po、K、Mg、Au,其堆积方式为:
①简单立方堆积的是________ ;
②体心立方堆积的是________ ;
③六方堆积的是________ ;
④面心立方堆积的是________ 。
(1)金属钠的晶胞模型是
(2)金属铜的晶胞模型是

(3)金属导电靠
(4)根据下列叙述,判断一定为金属晶体的是
A.由分子间作用力形成,熔点很低
B.由共价键结合形成网状晶体,熔点很高
C.固体有良好的导电性、导热性和延展性
(5)已知下列金属晶体: Po、K、Mg、Au,其堆积方式为:
①简单立方堆积的是
②体心立方堆积的是
③六方堆积的是
④面心立方堆积的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁、钴、镍及化合物在机械制造、磁性材料、新型电池或高效催化剂等许多领域都有着广泛的应用。请回答下列问题:
(1)基态Ni原子核外的最高能层符号是______ ,基态Ni2+最外层电子排布式为_______ ,未成对电子数为________________ 。
(2)[Co(NO )4]2–中各元素的第一电离能由小到大的顺序为
)4]2–中各元素的第一电离能由小到大的顺序为______ (填元素符号),配体中N的杂化方式为______________ 。
(3)铁的三种晶体的晶胞均为立方晶胞,三种晶体的晶胞如图所示:
①上述三种晶体的晶胞中属于体心立方晶胞的是______ (填“α”“δ”或“γ”)-Fe。
②γ-Fe晶胞中铁原子的配位数为_______________ 。
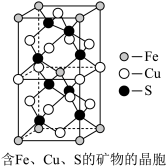
(4)一种含有Fe、Cu、S 三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________ 。若晶胞的底面边长为Apm,高为C pm,阿伏加 德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
(5)二茂铁[(C5H5)2Fe]可用作火箭燃料添加剂、汽油抗爆剂。二茂铁熔点172℃,沸点249℃,易升华,难溶于水,易溶于有机溶剂,它属于__________ 晶体。分子中的大π键可用符号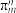 表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H
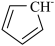
表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H )结构如图所示,其中的大π键可以表示为
)结构如图所示,其中的大π键可以表示为_______ 。
(1)基态Ni原子核外的最高能层符号是
(2)[Co(NO
 )4]2–中各元素的第一电离能由小到大的顺序为
)4]2–中各元素的第一电离能由小到大的顺序为(3)铁的三种晶体的晶胞均为立方晶胞,三种晶体的晶胞如图所示:
①上述三种晶体的晶胞中属于体心立方晶胞的是
②γ-Fe晶胞中铁原子的配位数为
(4)一种含有Fe、Cu、S 三种元素的矿物的晶胞(如图所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为

(5)二茂铁[(C5H5)2Fe]可用作火箭燃料添加剂、汽油抗爆剂。二茂铁熔点172℃,沸点249℃,易升华,难溶于水,易溶于有机溶剂,它属于
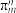 表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H
表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H )结构如图所示,其中的大π键可以表示为
)结构如图所示,其中的大π键可以表示为
您最近一年使用:0次



