依据下图中氮元素及其化合物的转化关系,回答问题:
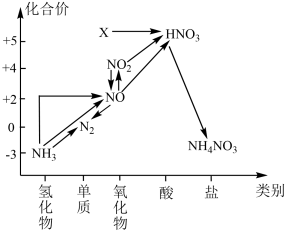
(1)图1中,X的化学式为_______ ,从化合价上看,X与水反应所得产物具有_______ 性(填“氧化”或“还原”)。写出稀HNO3与Cu反应的方程式_______ ;NH3与NO2加热反应的化学方程式_______ 。
(2)已知化学反应N2+3H2 2NH3的能量变化如图所示,回答下列问题:
2NH3的能量变化如图所示,回答下列问题:
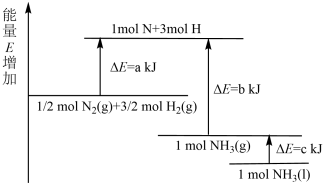
则0.5molN2(g)和1.5molH2(g)生成1molNH3(g)的过程____ (填“吸收”或“放出”)____ kJ能量。
(3)在一个容积3L的密闭容器里进行如下反应N2(g)+3H2(g)⇌2NH3(g),反应开始时n(N2)=1.5mol,n(H2)=4.4mol,2min末n(H2)=0.8mol。
①前2min内用NH3表示该反应的反应速率_______ ;
②到2min末N2的转化率为_______ ;
③下列条件能加快该反应的反应速率的有_______ ;
A.保持体积不变,再向容器中充N2
B.保持体积不变,再向容器中充He
C.保持压强不变,再向容器中充He
D.选择合适的催化剂

(1)图1中,X的化学式为
(2)已知化学反应N2+3H2
 2NH3的能量变化如图所示,回答下列问题:
2NH3的能量变化如图所示,回答下列问题:
则0.5molN2(g)和1.5molH2(g)生成1molNH3(g)的过程
(3)在一个容积3L的密闭容器里进行如下反应N2(g)+3H2(g)⇌2NH3(g),反应开始时n(N2)=1.5mol,n(H2)=4.4mol,2min末n(H2)=0.8mol。
①前2min内用NH3表示该反应的反应速率
②到2min末N2的转化率为
③下列条件能加快该反应的反应速率的有
A.保持体积不变,再向容器中充N2
B.保持体积不变,再向容器中充He
C.保持压强不变,再向容器中充He
D.选择合适的催化剂
更新时间:2022-06-20 18:28:28
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】用方铅矿(主要成分为PbS,含有杂质FeS等)和软锰矿(主要成分为MnO2,还有少量Fe2O3,A12O3等杂质)制备PbSO4和Mn3O4的工艺流程如下:

已知:PbCl2难溶于冷水,易溶于热水:PbC12(S)+2Cl-(aq) PbCl
PbCl (aq) △H>0
(aq) △H>0

(1)Mn元素在周期表中位于___________ 区。
(2)“浸取”过程中 MnO2和 PbS 反应生成浅黄色固体,写出有关的化学方程式:___________ 。
(3)除杂。上述酸浸液中 Mn2+的浓度为 1.6 mol·L-1,加 MnCO3调节 pH,使酸浸液中 Fe3+、Al3+完全沉淀(离子浓度小于 10-5 mol·L-1)与 Mn2+分离,调节溶液 pH 范围为___________ (不考虑体积的变化)。已知:Ksp[Fe(OH)3]=1.0×10-38,Ksp[Al(OH)3]=1.0×10-32,Ksp[Mn(OH)2]=1.6×10-13
(4)“趁热抽滤”的目的是___________ 。
(5)制备 Mn3O4。将滤液 X 水浴加热并保持 50 ℃,用氨水调节溶液 pH并维持在 8.5 左右,在不断搅拌下边通空气边加氨水,直至有大量沉淀生成,过滤洗涤,真空干燥得到产品 Mn3O4。如果 pH 控制不当会导致有碱式锰盐生成。
①写出制备 Mn3O4的化学方程式___________ 。
②pH 在 7.5-8.5 间,pH 值越低时 Mn3O4产品纯度越低的原因___________ 。

已知:PbCl2难溶于冷水,易溶于热水:PbC12(S)+2Cl-(aq)
 PbCl
PbCl (aq) △H>0
(aq) △H>0
(1)Mn元素在周期表中位于
(2)“浸取”过程中 MnO2和 PbS 反应生成浅黄色固体,写出有关的化学方程式:
(3)除杂。上述酸浸液中 Mn2+的浓度为 1.6 mol·L-1,加 MnCO3调节 pH,使酸浸液中 Fe3+、Al3+完全沉淀(离子浓度小于 10-5 mol·L-1)与 Mn2+分离,调节溶液 pH 范围为
(4)“趁热抽滤”的目的是
(5)制备 Mn3O4。将滤液 X 水浴加热并保持 50 ℃,用氨水调节溶液 pH并维持在 8.5 左右,在不断搅拌下边通空气边加氨水,直至有大量沉淀生成,过滤洗涤,真空干燥得到产品 Mn3O4。如果 pH 控制不当会导致有碱式锰盐生成。
①写出制备 Mn3O4的化学方程式
②pH 在 7.5-8.5 间,pH 值越低时 Mn3O4产品纯度越低的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】采矿废水中常含有氢氰酸(HCN)和亚砷酸(H3AsO3)等有害物质,必须经过处理达标后才能排放。
Ⅰ.金矿提金时,用NaCN溶液浸取获得Na[Au(CN)2]进一步处理时产生氢氰酸(HCN,电离常数K=5×10-10)。
(1)NaCN中σ键与π键数目之比为_______ 。
(2)通过电激发产生羟基自由基(HO*)和OH-可处理废水中的CN-,可能的反应机理如图所示。
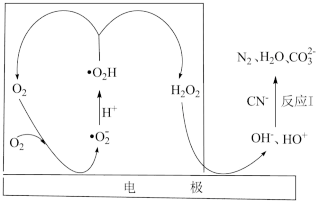
①反应I的离子方程式为_______ 。
②虚线方框内的过程可描述为_______ 。
Ⅱ.工业上常将废水中的亚砷酸(H3AsO3)氧化成砷酸(H3AsO4),再调节到合适的pH范围内用吸附剂脱除。砷酸(H3AsO4)溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图所示。
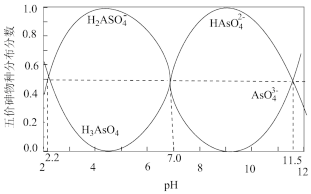
(3)砷元素基态原子的电子排布式为:_______ 。
(4)当溶液pH=4.1时,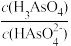 =
=_______ 。
(5)在25℃时,在浓度均为0.1 mol/L的NaCN溶液和NaH2AsO4溶液中,pH较大的是_______ 。
Ⅰ.金矿提金时,用NaCN溶液浸取获得Na[Au(CN)2]进一步处理时产生氢氰酸(HCN,电离常数K=5×10-10)。
(1)NaCN中σ键与π键数目之比为
(2)通过电激发产生羟基自由基(HO*)和OH-可处理废水中的CN-,可能的反应机理如图所示。

①反应I的离子方程式为
②虚线方框内的过程可描述为
Ⅱ.工业上常将废水中的亚砷酸(H3AsO3)氧化成砷酸(H3AsO4),再调节到合适的pH范围内用吸附剂脱除。砷酸(H3AsO4)溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如图所示。

(3)砷元素基态原子的电子排布式为:
(4)当溶液pH=4.1时,
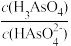 =
=(5)在25℃时,在浓度均为0.1 mol/L的NaCN溶液和NaH2AsO4溶液中,pH较大的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】连二亚硫酸钠( )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ. 的制备
的制备 时选用上图所示装置中的
时选用上图所示装置中的________ (填标号)。选用以下试剂中的________ (填标号)。
A.铜粉 B. 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
Ⅱ. 的制备
的制备
制用如图所示实验装置(加热、搅拌及夹持装置省略)制备 ,实验步骤如下:
,实验步骤如下: 一段时间;
一段时间;
ii.然后持续通入 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;
iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入 的目的是
的目的是________ (答出两点)。
(3)装置d中发生的主要反应的化学方程式为________ 。
(4)步骤iv中“洗涤”时,洗涤剂为________ (填“水”或“乙醇”),进一步提纯 的方法为
的方法为________ 。
Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用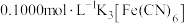 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
(5)滴定过程中发生反应的离子方程式为________ 。
(6)产品中 的质量分数为
的质量分数为________ 。
(7)下列情况会造成测定结果偏小的是________ (填标号)。
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用 标准液润洗酸式滴定管
标准液润洗酸式滴定管
C.滴定终点时俯视读数
 )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ.
 的制备
的制备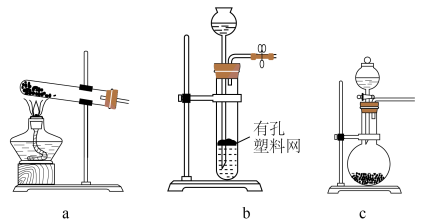
 时选用上图所示装置中的
时选用上图所示装置中的A.铜粉 B.
 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸Ⅱ.
 的制备
的制备制用如图所示实验装置(加热、搅拌及夹持装置省略)制备
 ,实验步骤如下:
,实验步骤如下: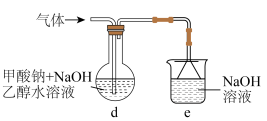
 一段时间;
一段时间;ii.然后持续通入
 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入
 的目的是
的目的是(3)装置d中发生的主要反应的化学方程式为
(4)步骤iv中“洗涤”时,洗涤剂为
 的方法为
的方法为Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量
 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用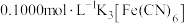 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。(5)滴定过程中发生反应的离子方程式为
(6)产品中
 的质量分数为
的质量分数为(7)下列情况会造成测定结果偏小的是
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用
 标准液润洗酸式滴定管
标准液润洗酸式滴定管C.滴定终点时俯视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学课外小组的同学通过实验探究温度和浓度对反应速率的影响。实验原理及方案:在酸性溶液中,KIO3和Na2SO3可发生反应生成I2,生成的I2可用淀粉溶液检验,根据出现蓝色的时间来衡量该反应的速率。
回答下列问题:
(1)实验①③中V1=_______ ,V2=_______ 。
(2)出现蓝色的时间t1与t3大到小关系_______ 。
(3)实验②③的目的是_______ 。
(4)实验中加水的目的是_______ 。
(5)资料显示序号①的反应进行至10 s时,测得Na2SO3溶液的浓度为0.02 mol·L-1,则5 s内消耗Na2SO3的平均速率v(Na2SO3)=_______ 。
| 实验序号 | 0.1 mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.1 mol·L-1Na2SO3溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 | V1 | 5 | t1 |
| ② | 5 | 5 | 30 | 25 | t2 |
| ③ | 5 | V2 | 20 | 25 | t3 |
(1)实验①③中V1=
(2)出现蓝色的时间t1与t3大到小关系
(3)实验②③的目的是
(4)实验中加水的目的是
(5)资料显示序号①的反应进行至10 s时,测得Na2SO3溶液的浓度为0.02 mol·L-1,则5 s内消耗Na2SO3的平均速率v(Na2SO3)=
您最近一年使用:0次
【推荐2】完成下列问题。
(1)①甲烷可用于生产合成气,反应为:
 ,已知几种物质中化学键的键能如下表所示:则a=
,已知几种物质中化学键的键能如下表所示:则a=___________ 。
②科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:

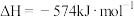
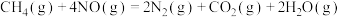
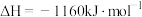
则甲烷直接将 还原为
还原为 的热化学方程式为
的热化学方程式为___________
(2)铁在一定条件下可与 反应:
反应: 。向
。向 恒容密闭容器中加入还原性铁粉并充入一定量的
恒容密闭容器中加入还原性铁粉并充入一定量的 气体,恒温条件下,反应过程中的气体浓度随时间变化如图所示。
气体,恒温条件下,反应过程中的气体浓度随时间变化如图所示。

①下列条件的改变能使上述反应的化学反应速率降低的是___________ (填标号)。
a.降低反应温度 b.充入 气 c.充入
气 c.充入 d.用铁块代替铁粉
d.用铁块代替铁粉
② 内,用
内,用 表示的反应速率为
表示的反应速率为___________ (填含 的表达式)
的表达式)
③下列描述中能说明上述反应已达到化学平衡状态的是___________ (填标号)。
a.
b.容器中混合气体的密度不随时间而变化
c.容器中混合气体的压强不随时间而变化
d单位时间内生成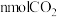 的同时生成
的同时生成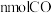
e.容器中混合气体的平均相对分子质量不随时间而变化
(3)近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是 )和水分子通过。其工作原理的示意图如图,请回答下列问题:
)和水分子通过。其工作原理的示意图如图,请回答下列问题:

①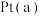 电极是电池的
电极是电池的___________ (填“正”或“负”)极。电解质溶液中的 向
向___________ (填“a”或“b”)极移动
②该电池工作时通入甲醇( )一极的电极反应式为
)一极的电极反应式为___________ 。
(1)①甲烷可用于生产合成气,反应为:

 ,已知几种物质中化学键的键能如下表所示:则a=
,已知几种物质中化学键的键能如下表所示:则a=| 化学键 |  |  |  |  |
键能/( ) ) | 436 | 465 | a | 1076 |

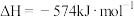
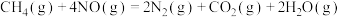
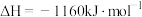
则甲烷直接将
 还原为
还原为 的热化学方程式为
的热化学方程式为(2)铁在一定条件下可与
 反应:
反应: 。向
。向 恒容密闭容器中加入还原性铁粉并充入一定量的
恒容密闭容器中加入还原性铁粉并充入一定量的 气体,恒温条件下,反应过程中的气体浓度随时间变化如图所示。
气体,恒温条件下,反应过程中的气体浓度随时间变化如图所示。
①下列条件的改变能使上述反应的化学反应速率降低的是
a.降低反应温度 b.充入
 气 c.充入
气 c.充入 d.用铁块代替铁粉
d.用铁块代替铁粉②
 内,用
内,用 表示的反应速率为
表示的反应速率为 的表达式)
的表达式)
③下列描述中能说明上述反应已达到化学平衡状态的是
a.

b.容器中混合气体的密度不随时间而变化
c.容器中混合气体的压强不随时间而变化
d单位时间内生成
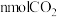 的同时生成
的同时生成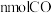
e.容器中混合气体的平均相对分子质量不随时间而变化
(3)近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子(就是
 )和水分子通过。其工作原理的示意图如图,请回答下列问题:
)和水分子通过。其工作原理的示意图如图,请回答下列问题:
①
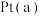 电极是电池的
电极是电池的 向
向②该电池工作时通入甲醇(
 )一极的电极反应式为
)一极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】乙烯的产量是衡量一个国家石油化工发展水平的标志,近几年各国都加大了乙烯制备的研发力度。回答下列问题:
(1)乙烷分解法
已知CO的燃烧热为 。以
。以 和
和 为原料可以协同制取
为原料可以协同制取 和CO,发生的反应如下:
和CO,发生的反应如下:
反应1: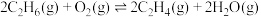
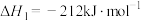
反应2:

①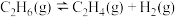 的
的
_____  。
。
②恒温条件下,下列能够提高反应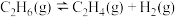 中乙烯产率的措施有
中乙烯产率的措施有______ (填标号)。
A.保持体积不变,通入氮气 B.保持压强不变,通入乙烷
C.保持体积不变,通入乙烷 D.及时分离出氢气
③恒温恒压(100kPa)下,在密闭容器中通入乙烷和稀有气体,平衡时各组分的体积分数分别为:乙烷5%、氢气20%、乙烯20%。该温度下反应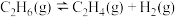 的平衡常数
的平衡常数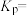
_____ kPa(用物质的平衡分压代替平衡浓度,平衡分压=总压强×体积分数)。
(2)二氧化碳转化法反应原理为 。在体积固定的密闭容器中,加入一定量的
。在体积固定的密闭容器中,加入一定量的 、
、 和催化剂,一段时间内测得二氧化碳的浓度变化如图1所示。在相同时间段内,测得乙烯的体积分数随温度变化如图2所示。
和催化剂,一段时间内测得二氧化碳的浓度变化如图1所示。在相同时间段内,测得乙烯的体积分数随温度变化如图2所示。
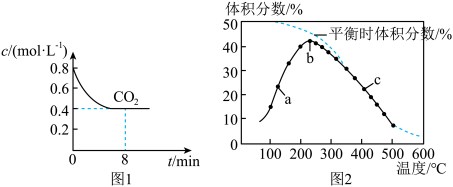
①由图1可知,0~8min用乙烯表示的平均反应速率为______  。
。
②图2中,a、b、c三点表示的化学平衡常数由大到小的顺序为______ ;b点的反应速率
___  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
③b点后乙烯的体积分数随温度升高逐渐减小的原因可能是_______ 、_______ (任写两条)。
④实验测定,反应中,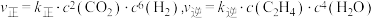 (
( 、
、 为速率常数,只与温度有关),精确实验表明,达到平衡时
为速率常数,只与温度有关),精确实验表明,达到平衡时 的值为
的值为 的2倍,则该反应的平衡常数
的2倍,则该反应的平衡常数
_______ 。
(1)乙烷分解法
已知CO的燃烧热为
 。以
。以 和
和 为原料可以协同制取
为原料可以协同制取 和CO,发生的反应如下:
和CO,发生的反应如下:反应1:
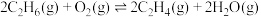
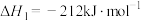
反应2:


①
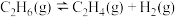 的
的
 。
。②恒温条件下,下列能够提高反应
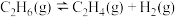 中乙烯产率的措施有
中乙烯产率的措施有A.保持体积不变,通入氮气 B.保持压强不变,通入乙烷
C.保持体积不变,通入乙烷 D.及时分离出氢气
③恒温恒压(100kPa)下,在密闭容器中通入乙烷和稀有气体,平衡时各组分的体积分数分别为:乙烷5%、氢气20%、乙烯20%。该温度下反应
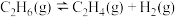 的平衡常数
的平衡常数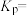
(2)二氧化碳转化法反应原理为
 。在体积固定的密闭容器中,加入一定量的
。在体积固定的密闭容器中,加入一定量的 、
、 和催化剂,一段时间内测得二氧化碳的浓度变化如图1所示。在相同时间段内,测得乙烯的体积分数随温度变化如图2所示。
和催化剂,一段时间内测得二氧化碳的浓度变化如图1所示。在相同时间段内,测得乙烯的体积分数随温度变化如图2所示。
①由图1可知,0~8min用乙烯表示的平均反应速率为
 。
。②图2中,a、b、c三点表示的化学平衡常数由大到小的顺序为

 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。③b点后乙烯的体积分数随温度升高逐渐减小的原因可能是
④实验测定,反应中,
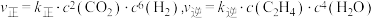 (
( 、
、 为速率常数,只与温度有关),精确实验表明,达到平衡时
为速率常数,只与温度有关),精确实验表明,达到平衡时 的值为
的值为 的2倍,则该反应的平衡常数
的2倍,则该反应的平衡常数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】水合硼酸锌(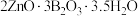 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为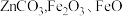 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下: 如下表所示:
如下表所示:
回答下列问题:
(1)“酸浸”时, 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为__________ 。为加快“酸浸”时的浸取速率,下列措施中无法达到目的是__________ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为__________ (填化学式)。
(3)“氧化”的目的是__________ (语言叙述), 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为__________ 。
(4)“一次调 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是__________ 。“二次调 ”时的
”时的 范围为
范围为__________ 。
(5)“制备”水合硼酸锌的化学方程式为__________ 。
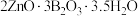 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为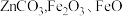 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下:
 如下表所示:
如下表所示:金属离子 |
|
|
|
|
|
开始沉淀 | 1.9 | 7.0 | 3.0 | 6.2 | 8.9 |
完全沉淀 | 3.2 | 9.0 | 4.7 | 8.0 | 10.9 |
(1)“酸浸”时,
 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为
(3)“氧化”的目的是
 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为(4)“一次调
 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是 ”时的
”时的 范围为
范围为(5)“制备”水合硼酸锌的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】完成下列问题。
(1)在一定温度下,向体积为2L的恒容密闭容器中充入一定量的A、B发生化学变化(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,回答下列问题:
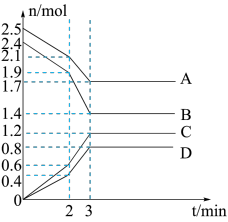
①写出该反应的化学方程式:___________ 。
② 内用D表示的化学反应速率
内用D表示的化学反应速率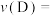
_______ 。
③该反应在 时改变了某一条件,则该条件可能为
时改变了某一条件,则该条件可能为___________ 。
(2)甲醇既是重要的化工原料,又可作为燃料,工业上将 催化加氢生产甲醇,发生如下反应:
催化加氢生产甲醇,发生如下反应:
反应Ⅰ: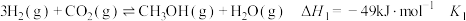
反应Ⅱ: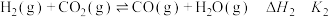
反应Ⅲ: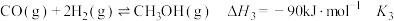
①
___________  ;相同条件下,反应Ⅲ的平衡常数
;相同条件下,反应Ⅲ的平衡常数
___________ (用平衡常数 、
、 表示)。
表示)。
②采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原 制备甲醇,该反应历程如图所示。
制备甲醇,该反应历程如图所示。
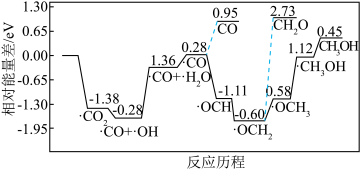
上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中___________ (填字母)的能量变化。
A. B.
B.
C. D.
D.
(1)在一定温度下,向体积为2L的恒容密闭容器中充入一定量的A、B发生化学变化(除物质D为固体外,其余的物质均为气体),各物质的含量随时间的变化情况如图所示,回答下列问题:

①写出该反应的化学方程式:
②
 内用D表示的化学反应速率
内用D表示的化学反应速率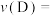
③该反应在
 时改变了某一条件,则该条件可能为
时改变了某一条件,则该条件可能为(2)甲醇既是重要的化工原料,又可作为燃料,工业上将
 催化加氢生产甲醇,发生如下反应:
催化加氢生产甲醇,发生如下反应:反应Ⅰ:
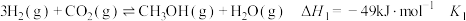
反应Ⅱ:
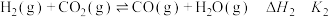
反应Ⅲ:
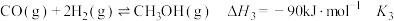
①

 ;相同条件下,反应Ⅲ的平衡常数
;相同条件下,反应Ⅲ的平衡常数
 、
、 表示)。
表示)。②采用真空封管法制备磷化硼纳米颗粒,成功实现了高选择性电催化还原
 制备甲醇,该反应历程如图所示。
制备甲醇,该反应历程如图所示。
上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】SO2、NOx是空气的主要污染物,有效去除大气中的SO2、NOx可以保护大气环境。含氮废水氨氮(以NH3、NH 存在)和硝态氮(以NO
存在)和硝态氮(以NO 、NO
、NO 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。
(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:
2Na2CO3(aq)+SO2(g)+H2O(l)=Na2SO3(aq)+2NaHCO3(aq) ΔH=akJ•mol-1
2NaHCO3(aq)+SO2(g)=Na2SO3(aq)+2CO2(g)+H2O(l) ΔH=bkJ•mol-1
Na2SO3(aq)+SO2(g)+H2O(l)=2NaHSO3(aq) ΔH=ckJ•mol-1
反应Na2CO3(aq)+SO2(g)=Na2SO3(aq)+CO2(g)的ΔH=___ kJ•mol-1。
(2)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图1所示,写出电解时铁电极发生的电极反应式:___ 。随后,铁电极附近有无色气体产生,写出有关反应的离子方程式:___ 。

(3)工业上以钛基氧化物涂层材料为阳极、碳纳米管修饰的石墨为阴极,电解硝酸钠和硫酸钠混合溶液,可使NO ,变为NH
,变为NH 。电极(电催化剂)所处的环境对其催化活性到重要作用。
。电极(电催化剂)所处的环境对其催化活性到重要作用。
①其他条件不变,向其中一份电解液中投加一定量NaCl,去除NH 的效果明显提高,溶液中氮元素含量显著降低。可能原因是
的效果明显提高,溶液中氮元素含量显著降低。可能原因是___ 。
②其他条件不变,只改变溶液的pH,NO 去除率如图2所示,pH升高时,去除率
去除率如图2所示,pH升高时,去除率___ (“升高”或“下降”),可能原因是___ 。
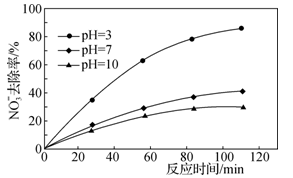
(4)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图所示。
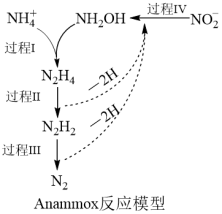
氨氮去除的过程可以描述为:___ 。
 存在)和硝态氮(以NO
存在)和硝态氮(以NO 、NO
、NO 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO2的相关反应的热化学方程式如下:
2Na2CO3(aq)+SO2(g)+H2O(l)=Na2SO3(aq)+2NaHCO3(aq) ΔH=akJ•mol-1
2NaHCO3(aq)+SO2(g)=Na2SO3(aq)+2CO2(g)+H2O(l) ΔH=bkJ•mol-1
Na2SO3(aq)+SO2(g)+H2O(l)=2NaHSO3(aq) ΔH=ckJ•mol-1
反应Na2CO3(aq)+SO2(g)=Na2SO3(aq)+CO2(g)的ΔH=
(2)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图1所示,写出电解时铁电极发生的电极反应式:

(3)工业上以钛基氧化物涂层材料为阳极、碳纳米管修饰的石墨为阴极,电解硝酸钠和硫酸钠混合溶液,可使NO
 ,变为NH
,变为NH 。电极(电催化剂)所处的环境对其催化活性到重要作用。
。电极(电催化剂)所处的环境对其催化活性到重要作用。①其他条件不变,向其中一份电解液中投加一定量NaCl,去除NH
 的效果明显提高,溶液中氮元素含量显著降低。可能原因是
的效果明显提高,溶液中氮元素含量显著降低。可能原因是②其他条件不变,只改变溶液的pH,NO
 去除率如图2所示,pH升高时,去除率
去除率如图2所示,pH升高时,去除率
(4)厌氧氨化法(Anammox)是一种新型的氨氮去除技术,反应模型如图所示。

氨氮去除的过程可以描述为:
您最近一年使用:0次








