根据有关知识,回答下列问题。
(1)符号 所代表的含义是_______(填字母)。
所代表的含义是_______(填字母)。
(2) 核外电子的运动状态有
核外电子的运动状态有_______ 种。
(3)短周期主族元素中,第一电离能最小的元素是_______ (填元素符号,下同),电负性最大的元素是_______ 。
(4)铜的原子序数是29,其价电子排布式为_______ 。
(5)元素的电负性和元素的化合价一样,也是元素的一种性质。表中给出了14种元素的电负性:
已知:两成键元素间电负性差值大于1.7时,一般形成离子键;两成键元素间电负性差值小于1.7时,一般形成共价键。
①请指出下列化合物中显正价的元素(填元素符号): :
:_______ 、 :
:_______ 。
②表中符合“对角线规则”的元素有 和
和 、B和
、B和 ,它们的性质分别有一定的相似性,写出
,它们的性质分别有一定的相似性,写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(1)符号
 所代表的含义是_______(填字母)。
所代表的含义是_______(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第三电子层 轨道有三个空间伸展方向 轨道有三个空间伸展方向 |
C.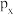 电子云有3个空间伸展方向 电子云有3个空间伸展方向 |
| D.第三电子层沿x轴方向伸展的p轨道 |
 核外电子的运动状态有
核外电子的运动状态有(3)短周期主族元素中,第一电离能最小的元素是
(4)铜的原子序数是29,其价电子排布式为
(5)元素的电负性和元素的化合价一样,也是元素的一种性质。表中给出了14种元素的电负性:
| 元素 |  | B |  | C |  | F | H |  | N |  | O | P | K |  |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 2.1 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 0.8 | 1.8 |
①请指出下列化合物中显正价的元素(填元素符号):
 :
: :
:②表中符合“对角线规则”的元素有
 和
和 、B和
、B和 ,它们的性质分别有一定的相似性,写出
,它们的性质分别有一定的相似性,写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:
21-22高二·全国·单元测试 查看更多[1]
更新时间:2022-08-22 19:40:05
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】磷及其化合物有许多用途。回答下列问题:
(1)基态磷原子核外共有_______ 种不同空间运动状态的电子,核外电子占据最高能层的符号是_______ ,占据该能层电子的能级最高的电子云轮廓图为_______ 形。
(2) 为三元中强酸,与
为三元中强酸,与 形成
形成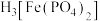 ,此性质常用于掩蔽溶液中的
,此性质常用于掩蔽溶液中的 。基态
。基态 价层电子的电子排布式为
价层电子的电子排布式为_______ ,该配合物中的配体是_______ ,1mol该配合物中含有_______ mol配位键。
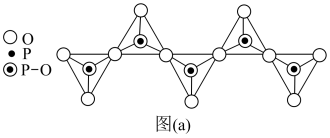
(3)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类。某直链多磷酸钠的阴离子呈如图(a)所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。该多磷酸钠中,磷、氧原子个数比为_______ 。
(1)基态磷原子核外共有
(2)
 为三元中强酸,与
为三元中强酸,与 形成
形成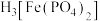 ,此性质常用于掩蔽溶液中的
,此性质常用于掩蔽溶液中的 。基态
。基态 价层电子的电子排布式为
价层电子的电子排布式为(3)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类。某直链多磷酸钠的阴离子呈如图(a)所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。该多磷酸钠中,磷、氧原子个数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】最近,妖“镍”横行,价格疯涨。镍是一种硬而有延展性并具有铁磁性的金属,在许多领域应用广泛。Ni-NTA-Nangold 可用于检测或定位 6x 组氨酸(His)或 Poly-His 标记的重组蛋白。Ni(II)-NTA 的结构简式如图所示。
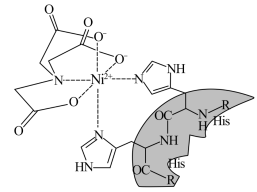
回答下列问题:
(1)基态Ni原子价电子排布式为_______ 。
(2)配体N(CH2COO-)3中 4 种元素的第一电离能 I1从大到小的顺序为_______ (用元素符号表示)。
(3)与 Ni2+配位的原子形成的空间构型为_______ 。
(4)已知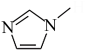 存在大π键,其结构中氮原子的杂化方式为
存在大π键,其结构中氮原子的杂化方式为_______ 。
(5)Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点Ni明显高于Ca,其原因是_______ 。
(6)某笼形包合物Ni(CN)a(NH3)b(C6H6)c的晶胞如图所示。
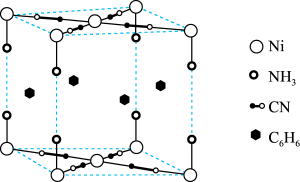
①该笼形包合物溶于酸能形成一种弱酸HCN,HCN中δ键和π键个数之比为_______ 。
②推测该包合物中氨与苯分子数目比,即b:c为_______ ,氨分子极易溶于水的原因是_______ 。
③若此晶胞体积为V nm3,阿伏加德罗常数为NA,晶胞的摩尔质量为M g/mol,则晶体密度为_______ g/cm3(例出计算表达式)。

回答下列问题:
(1)基态Ni原子价电子排布式为
(2)配体N(CH2COO-)3中 4 种元素的第一电离能 I1从大到小的顺序为
(3)与 Ni2+配位的原子形成的空间构型为
(4)已知
 存在大π键,其结构中氮原子的杂化方式为
存在大π键,其结构中氮原子的杂化方式为(5)Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点Ni明显高于Ca,其原因是
(6)某笼形包合物Ni(CN)a(NH3)b(C6H6)c的晶胞如图所示。

①该笼形包合物溶于酸能形成一种弱酸HCN,HCN中δ键和π键个数之比为
②推测该包合物中氨与苯分子数目比,即b:c为
③若此晶胞体积为V nm3,阿伏加德罗常数为NA,晶胞的摩尔质量为M g/mol,则晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)基态镍原子的价电子排布式________ ;铁的基态原子核外未成对电子数为________ 个。
(2)丁二酮肟(分子式为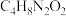 )所含的碳、氮、氧三种元素中第一电离能最大的是
)所含的碳、氮、氧三种元素中第一电离能最大的是________ (填元素符号)。在稀氨水介质中, 与丁二酮肟(分子式为
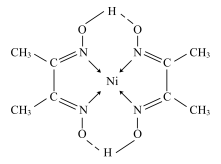
与丁二酮肟(分子式为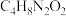 )反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
)反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为________ 。
(3)铁、镍易与CO作用形成羟基配合物 、
、 ,1个
,1个 分子中含有
分子中含有 键数目为
键数目为________ ;已知 分子为正四面体构型,下列溶剂能够溶解
分子为正四面体构型,下列溶剂能够溶解 的是
的是________ (填写字母)。
A.四氯化碳 B.苯 C.水 D.液氨
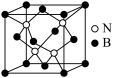
(4)氮化硼晶体有多种结构,其中立方氮化硼具有金刚石的结构(如图)。若晶胞边长为 ,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为
,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为________  。(用含有
。(用含有 和
和 的代数式表示)
的代数式表示)
(1)基态镍原子的价电子排布式
(2)丁二酮肟(分子式为
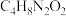 )所含的碳、氮、氧三种元素中第一电离能最大的是
)所含的碳、氮、氧三种元素中第一电离能最大的是 与丁二酮肟(分子式为
与丁二酮肟(分子式为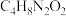 )反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
)反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
(3)铁、镍易与CO作用形成羟基配合物
 、
、 ,1个
,1个 分子中含有
分子中含有 键数目为
键数目为 分子为正四面体构型,下列溶剂能够溶解
分子为正四面体构型,下列溶剂能够溶解 的是
的是A.四氯化碳 B.苯 C.水 D.液氨
(4)氮化硼晶体有多种结构,其中立方氮化硼具有金刚石的结构(如图)。若晶胞边长为
 ,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为
,晶胞中N原子位于B原子所形成的正四面体的体心,这种氮化硼晶体的密度为 。(用含有
。(用含有 和
和 的代数式表示)
的代数式表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镍及其化合物在工业生产中有着广泛的运用,当前世界上镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。回答下列问题:
(1)镍元素在元素周期表中位于__________ ,在基态镍原子中,其核外电子有_______ 种不同运动状态,M层电子排布式为______________________ 。
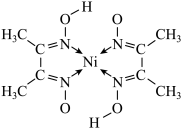
(2)在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。在该结构中,氮镍之间形成的化学键是__________ ,碳原子的杂化轨道类有_______________ ,非金属元素的电负性由大到小的顺序是_________________ 。
(3)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合18电子规则。如Cr可以与CO形成Cr(CO)6分子:价电子总数(18) =Cr的价电子数(6)+CO提供电子数(2×6)。Ni原子与CO形成配合物的化学式为______________ 。该配合物常温下为液态,易溶于CCl4、苯等有机溶剂,据此判断该分子属于____________ 分子(填“极性”或“非极性”)。
(4)甲醛在Ni催化作用下加氢可得甲醇。甲醇分子内的O-C-H键角_____________ (填“大于”、“等于”或“小于”)甲醛分子内的O-C-H键角;甲醇易溶于水的原因是______________ 。
(5)NixO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为a pm.晶胞中两个Ni原子之间的最短距离为_______ pm。若晶体中的Ni离子分别为Ni2+、Ni3+,此晶体中Ni2+与Ni3+的最简整数比为____________ 。
(1)镍元素在元素周期表中位于
(2)在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。在该结构中,氮镍之间形成的化学键是

(3)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合18电子规则。如Cr可以与CO形成Cr(CO)6分子:价电子总数(18) =Cr的价电子数(6)+CO提供电子数(2×6)。Ni原子与CO形成配合物的化学式为
(4)甲醛在Ni催化作用下加氢可得甲醇。甲醇分子内的O-C-H键角
(5)NixO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为a pm.晶胞中两个Ni原子之间的最短距离为
您最近一年使用:0次
【推荐2】回答下列问题
(1)基态Cr原子的核外电子排布式为___ 。
(2)基态S原子电子占据最高能级的电子云轮廓图为__ 形。
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式___ 。
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为___ 。
(5)下列状态的镁中,电离最外层一个电子所需能量最大的是___ 。
(6)利用CO可以合成化工原料COCl2,其中COCl2分子的结构式为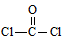 ,则COCl2分子内含有
,则COCl2分子内含有___ 。
(7)已知元素M的气态原子逐个失去第1至第4个电子所需能量如表所示:
元素M的常见化合价是___ 。
(1)基态Cr原子的核外电子排布式为
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(5)下列状态的镁中,电离最外层一个电子所需能量最大的是
A.[Ne]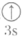 | B.[Ne]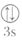 | C.[Ne] | D.[Ne]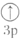 |
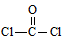 ,则COCl2分子内含有
,则COCl2分子内含有| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
| I1 | I2 | I3 | I4 | |
| 电离能/(kJ•mol-1) | 578 | 1817 | 2745 | 11578 |
元素M的常见化合价是
| A.+1 | B.+2 | C.+3 | D.+4 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl2•2CO•2H2O。回答下列问题:
(1)Cu在元素周期表中属于______ (选填“s”、“p”、“d”或“ds”)区元素。
(2)C、N、O三种原子中的第一电离能最大的是____________ 。NO3- 离子的空间构型是______ 。
(3)CO与N2互称等电子体。下表为CO和N2的有关信息。
根据表中数据,说明CO比N2活泼的原因是________________________ 。
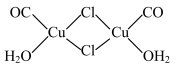
(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:
①该配合物中氯原子的杂化方式为_________________________ 。
②该配合物中,CO作配体时配位原子是C而不是O的原因是______________________ 。
③1molCu2Cl2•2CO•2H2O含有的______________ 个σ键。
(1)Cu在元素周期表中属于
(2)C、N、O三种原子中的第一电离能最大的是
(3)CO与N2互称等电子体。下表为CO和N2的有关信息。
| 键的类型 | A-B(单键) | A=B(双键) | A≡B(叁键) | |
| 键能(kJ/mol) | CO | 351 | 803 | 1071 |
| N2 | 159 | 418 | 946 | |
根据表中数据,说明CO比N2活泼的原因是
(4)Cu2Cl2•2CO•2H2O是一种配合物,其结构如图所示:

①该配合物中氯原子的杂化方式为
②该配合物中,CO作配体时配位原子是C而不是O的原因是
③1molCu2Cl2•2CO•2H2O含有的
您最近一年使用:0次



