室温下,向0.01mol·L-1的CH3COOH溶液中不断加水稀释,其溶液的pH变化如图所示[已知:Ka(CH3COOH)=1.6×10-5,lg2=0.3,电离度= ×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是

 ×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
×100%,pH=-lgc(H+),忽略溶液体积和温度的变化],下列说法正确的是
| A.x点的pH为3.2 |
| B.x点与y点CH3COOH的电离平衡常数:Kx>Ky |
| C.室温下,0.01mol·L-1的CH3COOH溶液中,CH3COOH的电离度约为4% |
| D.升高温度,c(H+)增大,Ka的大小保持不变 |
更新时间:2022-09-02 06:21:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各组物质反应时,可用离子方程式 表示的是
表示的是
 表示的是
表示的是| A.盐酸与氨水 | B.硝酸与氢氧化镁溶液 |
| C.氢碘酸与氢氧化钠溶液 | D.硫酸与氢氧化钡溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向 氨水中逐滴加入
氨水中逐滴加入 的
的 溶液,溶液的导电能力和
溶液,溶液的导电能力和 变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
 氨水中逐滴加入
氨水中逐滴加入 的
的 溶液,溶液的导电能力和
溶液,溶液的导电能力和 变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
变化如图所示(忽略反应过程中溶液温度变化),下列说法错误的是
A.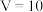 |
B.常温下,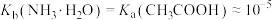 |
C. 点溶液中存在关系: 点溶液中存在关系: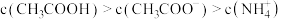 |
D. 点溶液中存在关系: 点溶液中存在关系: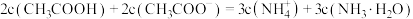 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列溶液显酸性,解释其原因的化学用语错误的是
A.碳酸溶液:H2CO3⇌2H++ |
B.硫酸溶液:H2SO4=2H++ |
C.硫酸氢钠溶液:NaHSO4=Na++H++ |
D.NH4Cl溶液: +H2O⇌NH3∙H2O+H+ +H2O⇌NH3∙H2O+H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列方程式不正确的是
| A.氢氧化亚铁在空气中最终变为红褐色的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
B.乙醇的催化氧化反应的化学方程式:2CH3CH2OH+O2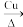 2CH3CHO+2H2O 2CH3CHO+2H2O |
| C.碳酸镁与稀硫酸反应的离子方程式:MgCO3+2H+=Mg2++H2O+CO2↑ |
D.碳酸的电离方程式:H2CO3 CO CO +2H+ +2H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列表述正确的是
A.碳酸氢钠溶液的水解反应: |
B.用铜电极电解饱和氯化钠溶液: |
C.氢硫酸的电离方程式: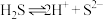 |
D.向氢氧化镁饱和溶液中滴加氯化铁溶液,出现红褐色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】醋酸的电离方程式为CH3COOH(aq) CH3COO-(aq)+H+(aq)△H>0,25°C时,Ka=1.75×10-5。下列说法不正确的是
CH3COO-(aq)+H+(aq)△H>0,25°C时,Ka=1.75×10-5。下列说法不正确的是
 CH3COO-(aq)+H+(aq)△H>0,25°C时,Ka=1.75×10-5。下列说法不正确的是
CH3COO-(aq)+H+(aq)△H>0,25°C时,Ka=1.75×10-5。下列说法不正确的是| A.向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小 |
| B.向该溶液中加少量水,c(OH-)增大 |
| C.该温度下0.01mol/L醋酸溶液Ka=1.75×10-5 |
| D.升高温度,c(H+)增大,Ka变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】液氨与纯水类似,也存在微弱的电离: ,该过程吸热。定义T℃时,液氨的离子积常数
,该过程吸热。定义T℃时,液氨的离子积常数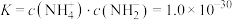 ,若用定义pH的方式来规定
,若用定义pH的方式来规定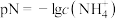 ,下列叙述正确的是
,下列叙述正确的是
 ,该过程吸热。定义T℃时,液氨的离子积常数
,该过程吸热。定义T℃时,液氨的离子积常数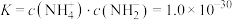 ,若用定义pH的方式来规定
,若用定义pH的方式来规定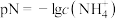 ,下列叙述正确的是
,下列叙述正确的是| A.其他条件不变,增加液氨的量,电离平衡正向移动 |
B.纯液氨达到电离平衡时,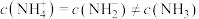 |
C.温度高于T℃时的纯液氨中,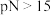 |
| D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知 。常温下,用
。常温下,用 氨水滴定
氨水滴定 浓度均为
浓度均为 的
的 和
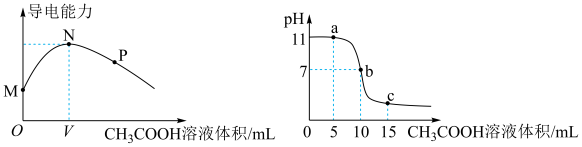
和 混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述正确的是
混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述正确的是

 。常温下,用
。常温下,用 氨水滴定
氨水滴定 浓度均为
浓度均为 的
的 和
和 混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述正确的是
混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述正确的是
A.a点的混合溶液中 约为 约为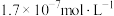 |
| B.b点时的混合溶液恰好成中性 |
C.当混合溶液 时,加入氨水体积一定 时,加入氨水体积一定 |
D. 点的混合溶液中: 点的混合溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,某 溶液中各含磷微粒的浓度之和为
溶液中各含磷微粒的浓度之和为 ,各含磷微粒的pc−pOH关系如图所示[ pc表示各含磷微粒浓度的负对数,即
,各含磷微粒的pc−pOH关系如图所示[ pc表示各含磷微粒浓度的负对数,即 ;pOH表示
;pOH表示 浓度的负对数,即
浓度的负对数,即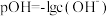 ]。已知:
]。已知: ,
, 。下列说法正确的是
。下列说法正确的是

 溶液中各含磷微粒的浓度之和为
溶液中各含磷微粒的浓度之和为 ,各含磷微粒的pc−pOH关系如图所示[ pc表示各含磷微粒浓度的负对数,即
,各含磷微粒的pc−pOH关系如图所示[ pc表示各含磷微粒浓度的负对数,即 ;pOH表示
;pOH表示 浓度的负对数,即
浓度的负对数,即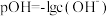 ]。已知:
]。已知: ,
, 。下列说法正确的是
。下列说法正确的是
A.曲线①表示 随pOH的变化 随pOH的变化 |
B. 的溶液中, 的溶液中, |
C. 的平衡常数 的平衡常数 |
D.向该 溶液中滴加少量 溶液中滴加少量 溶液,化学方程式为 溶液,化学方程式为  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】化学中常用AG表示溶液的酸度[ ]。室温下,向20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法错误的是
]。室温下,向20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法错误的是

 ]。室温下,向20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法错误的是
]。室温下,向20.00mL0.1000mol•L-1的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。下列说法错误的是
| A.稀硫酸的物质的量浓度为0.0500mol•L-1 |
| B.a、b、c三点对应的溶液中,水的电离程度大小关系:c>b>a |
C.当AG=0时,溶液中存在c( )>c( )>c( )>c(H+)=c(OH-) )>c(H+)=c(OH-) |
D.室温下 的电离常数Kb=1.0×10-6 的电离常数Kb=1.0×10-6 |
您最近一年使用:0次


 10-7,次氯酸的K=2.98
10-7,次氯酸的K=2.98

