根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同条件下,分别测量0.1mol/L和0.01mol/L醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| B | 常温下,分别测定浓度均为0.1mol/LNaF和NaClO溶液的pH,后者的pH大 | 酸性:HF<HClO |
| C | KNO3和KOH的混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸,试纸变为蓝色 | NO 被还原为NH3 被还原为NH3 |
| D | CuS的悬浊液中加入饱和MnSO4溶液可生成浅红色沉淀(MnS为浅红色) | Ksp(MnS)<Ksp(CuS) |
| A.A | B.B | C.C | D.D |
更新时间:2022-09-14 23:30:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知HF的酸性强于CH3COOH,常温下有下列三种溶液,有关叙述中不正确的是
| 编号 | ① | ② | ③ |
| pH | 11 | 3 | 3 |
| 溶液 | NaOH溶液 | CH3COOH溶液 | HF溶液 |
| A.②、③混合后: c(H+)=c(F-)+c(CH3COO-)+c(OH-) |
| B.①、②等体积混合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C.中和相同体积的②、③,需消耗相同体积的① |
| D.向③中加入CH3COONa固体,HF的电离平衡向右移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有体积相同,浓度均为 的三种溶液①
的三种溶液① 、②HCl、③
、②HCl、③ ,下列说法中正确的是
,下列说法中正确的是
 的三种溶液①
的三种溶液① 、②HCl、③
、②HCl、③ ,下列说法中正确的是
,下列说法中正确的是| A.溶液的pH:①>②=③ |
| B.溶液的导电性:③>②=① |
| C.中和NaOH的能力:①>②>③ |
| D.加入足量Zn粉,产生H2的体积:①>②=③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作和现象能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向Na2S溶液中通入足量CO2,然后再将产生的气体导入CuSO4溶液中,产生黑色沉淀 | Ka1(H2CO3)>Ka1(H2S) |
| B | 向KBrO3溶液中通入少量氯气,然后再加入少量苯,有机层呈橙红色 | 氧化性:Cl2>Br2 |
| C | 常温下,用pH计分别测定等体积1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH,测的pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| D | 将炽热的木炭与浓硝酸混合,产生红棕色气体 | 加热条件下,浓硝酸被木炭还原成NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列各组离子一定能在指定溶液中共存的是
A.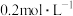 的 的 溶液中: 溶液中: 、 、 、 、 、 、 |
B. 的 的 溶液中: 溶液中: 、 、 、 、 、 、 |
C. 的 的 溶液中: 溶液中: 、 、 、 、 、 、 |
D. 的 的 溶液中: 溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验的原理、方法和结论都正确的是
| A.将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B.用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C.向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中,正确的是
| A.难溶电解质达到沉淀溶解平衡时,保持温度不变增加难溶电解质的量,平衡向溶解方向移动 |
| B.难溶电解质都是弱电解质 |
C.在白色 沉淀上滴加 沉淀上滴加 溶液,沉淀变黑,说明 溶液,沉淀变黑,说明 比 比 更难溶于水 更难溶于水 |
D. 在水中的溶解度大于在饱和 在水中的溶解度大于在饱和 溶液中的溶解度 溶液中的溶解度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列方案设计、现象和结论有不正确的是
选项 | 实验 | 现象 | 结论 |
A | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量新制氯水,充分反应后加入1~2滴淀粉溶液 | 溶液变蓝 | 海带中含有碘元素 |
B | 分别向饱和硼酸( )溶液和稀硫酸溶液中加入少量 )溶液和稀硫酸溶液中加入少量 粉末 粉末 | 前者无气泡冒出,后者有气泡冒出 | 非金属性:S>C>B |
C | 取少量乙酰水杨酸晶体,加入盛有3mL蒸馏水的试管中,加1~2滴1%氯化铁溶液 | 溶液出现紫色 | 乙酰水杨酸中含有水杨酸 |
D | 将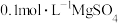 溶液滴入NaOH溶液中至不再有沉淀产生,再滴加 溶液滴入NaOH溶液中至不再有沉淀产生,再滴加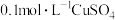 溶液 溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | 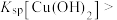 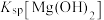 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氨气还原氧化铁的反应为Fe2O3+2NH3 2Fe+N2+3H2O,某学生拟用如图装置完成该实验并验证部分产物,下列说法错误的是
2Fe+N2+3H2O,某学生拟用如图装置完成该实验并验证部分产物,下列说法错误的是

 2Fe+N2+3H2O,某学生拟用如图装置完成该实验并验证部分产物,下列说法错误的是
2Fe+N2+3H2O,某学生拟用如图装置完成该实验并验证部分产物,下列说法错误的是
| A.装置a中药品可为无水CaCl2 |
| B.装置b盛放的试剂是无水硫酸铜 |
| C.装置C可以防止倒吸,同时吸收未反应的氨气 |
| D.装置D中收集的气体主要是N2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将铜币置于盛有20mL 0.1mol•L―1 AgNO3溶液的烧杯中,可观察到
| A.溶液变红 | B.溶液颜色不变 | C.铜币表面变色 | D.有大量气泡逸出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A的一种核素的原子核内无中子,B 的一种核素被考古学家用于测定文物的年代,D原子的最外层电子数比次外层多4,D的阴离子与E的阳离子具有相同的电子排布,两元素可形成化合物E2D,D、F同主族。用化学用语回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)G的离子结构示意图为_____ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为___________ 。
(4)由 A、C、D三元素按原子个数4∶2∶3之比形成物质的化学式为_____ ,其中所含化学键的类型有_____ 。
(5)B、D、F 可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为___________ 。
(6)下列实验操作对应的实验现象中,不正确的是___________ 。
(1)D在元素周期表中的位置为
(2)G的离子结构示意图为
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为
(4)由 A、C、D三元素按原子个数4∶2∶3之比形成物质的化学式为
(5)B、D、F 可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为
(6)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| a | 将E单质投入到CuSO4溶液中 | 有红色固体析出 |
| b | 向AlCl3溶液中通入过量C的气态氢化物 | 先产生白色沉淀,后沉淀溶解 |
| c | 将G的单质通入到NaBr溶液中充分反应后,加入四氯化碳,振荡,静置 | 下层溶液变为橙色 |
| d | 将过量B的最高价氧化物通入到NaAlO2溶液中 | 产生白色沉淀 |
您最近一年使用:0次

 的数目小于0.3NA
的数目小于0.3NA 、
、 个数之和小于0.1NA
个数之和小于0.1NA

