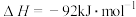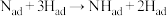黄铁矿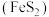 是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化:
是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化: 。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有:
。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有: ;
; 。
。 的反应机理如下:
的反应机理如下:
反应Ⅰ: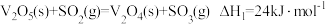
反应Ⅱ:
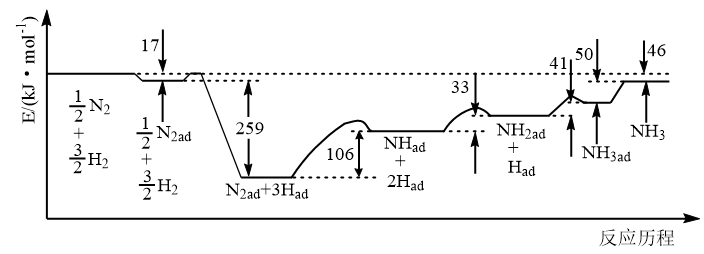
反应中的能量变化如题图,下列说法不正确的是

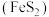 是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化:
是一种重要的含铁矿物,在潮湿空气中会被缓慢氧化: 。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有:
。工业上常选择黄铁矿为原料制备硫酸,其中发生的反应有: ;
; 。
。 的反应机理如下:
的反应机理如下:反应Ⅰ:
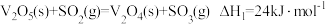
反应Ⅱ:

反应中的能量变化如题图,下列说法不正确的是

A. | B.反应Ⅰ的 |
C.通入过量空气,可提高 的平衡转化率 的平衡转化率 | D.反应速率由反应Ⅰ决定 |
更新时间:2022-09-13 17:14:45
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】某反应可有效降低汽车尾气污染物的排放,其反应热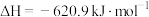 。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
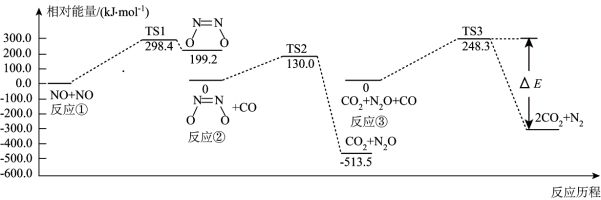
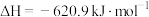 。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法正确的是
A.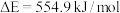 |
| B.三个基元反应中只有③是放热反应 |
| C.该化学反应的速率主要由反应②决定 |
D.该过程的总反应为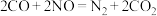 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法或表示方法正确的是
| A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| B.放热反应的反应速率大于吸热反应的反应速率 |
| C.盖斯定律实质上是能量守恒的体现 |
| D.H2的燃烧热为ΔH=-285.8 kJ/mol,2H2O(l)=2H2(g)+O2(g)△H= +285.8 kJ/mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】酸雨的形成是一种复杂的大气化学和光学化学过程,在清洁空气、污染空气中形成硫酸型酸雨的过程如图,下列有关说法错误的是

| A.光照能引发酸雨的形成 | B.所涉及的变化均为氧化还原反应 |
| C.污染空气能加快酸雨的形成 | D. 的能量比 的能量比 的低 的低 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列图示所得出的结论正确的是
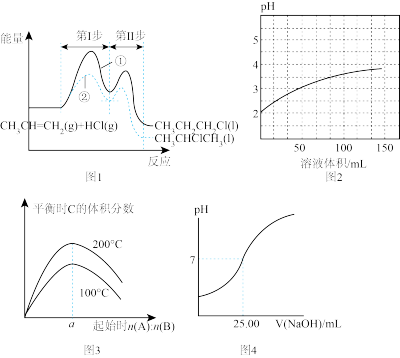

| A.由图1可知反应②的第I步比第Ⅱ步反应速率快 |
| B.若图2为1 mL pH=2某一元酸溶液加水稀释时pH随溶液总体积的变化曲线,则说明该酸是弱酸 |
| C.由图3知反应3A(g)+2B⇌2C(g)的ΔH>0,且a=1.5 |
| D.若图4表示常温下用0.1000 mol/L NaOH溶液滴定25.00mLCH3COOH溶液的滴定曲线,则c(CH3COOH)=0.1000 mol/L |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】对于反应N2 + 3H2 2NH3 ,下列判断正确的是( )
2NH3 ,下列判断正确的是( )
 2NH3 ,下列判断正确的是( )
2NH3 ,下列判断正确的是( )| A.3体积H2和足量N2反应,必定生成2体积NH3 |
| B.工业上采用氮氢循环操作的主要目的是提高H2和N2的利用率 |
| C.500℃左右比室温更有利于向合成氨的方向进行 |
| D.其他条件不变,增大压强,平衡必定向右移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】将 放入密闭的真空容器中,反应
放入密闭的真空容器中,反应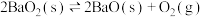 达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
 放入密闭的真空容器中,反应
放入密闭的真空容器中,反应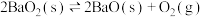 达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同
达到平衡。下列哪些改变可使平衡移动,且新平衡时氧气的浓度与原平衡相同| A.保持温度和体积不变,充入一定量的氧气 |
B.保持温度和体积不变,加入一定量的 |
| C.保持温度不变,缩小容器的体积 |
| D.保持体积不变,升高温度 |
您最近一年使用:0次
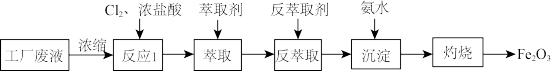
【推荐3】某电子厂排放的酸性废液中含有Fe3+、Cu2+、Fe2+和Cl-等离子,以这种废液为原料设计制备高纯Fe2O3的工艺流程如图所示(部分操作和条件略)。已知:①HCl(浓)+FeCl3 HFeCl4 (易溶于有机溶剂);②
HFeCl4 (易溶于有机溶剂);②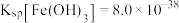 ,
,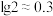 。下列说法不正确的是
。下列说法不正确的是
 HFeCl4 (易溶于有机溶剂);②
HFeCl4 (易溶于有机溶剂);②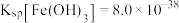 ,
,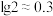 。下列说法不正确的是
。下列说法不正确的是
| A.反应1所发生的反应中存在氧化还原反应 |
| B.在反萃取过程中利用了平衡移动原理,水不可以作为反萃取剂 |
| C.氨水的作用是调节pH使Fe3+沉淀,相关反应离子方程式为:Fe3++3OH-=Fe(OH)3↓ |
| D.为使Fe3+沉淀完全(浓度小于1×10-5 mol/L),需调节溶液pH>3.3 |
您最近一年使用:0次

 的
的