硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关反应2SO2+O2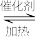 2SO3的说法中不正确的是
2SO3的说法中不正确的是
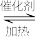 2SO3的说法中不正确的是
2SO3的说法中不正确的是| A.实际生产中,SO2、O2再循环使用提高原料利用率 |
| B.实际生产中,为了提高经济效率压强越高越好 |
| C.在生产中,通入过量空气的目的是提高SO2的转化率 |
| D.实际生产中,选定400~500 ℃作为操作温度的主要原因是催化剂的活性最高 |
更新时间:2022-09-21 18:23:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】从下列实验事实或者操作所引出的相应结论不正确的是
| 选项 | 实验事实或者操作 | 结论 |
| A | 将充满NO2的密闭玻璃球完全浸入热水中,球内红棕色变深 | 反应:2NO2 N2O4, N2O4,ΔH<0 |
| B | 向两支装有KI3溶液试管分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀生成 | KI3溶液中存在平衡: I3-  I- + I2 I- + I2 |
| C | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参加反应,只改变化学反应速率 |
| D | 相同温度、相同体积、相同pH的盐酸和醋酸分别与足量的、形状相同的锌粒充分反应 | 开始时的反应速率相同,排水法收集到氢气体积不同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】我国计划在2030年前实现“碳达峰”,在2060年前实现碳中和。下列说法不正确的是
A.我国科学家首次在实验室中实现 到淀粉的合成,有望促进“碳中和”的达成 到淀粉的合成,有望促进“碳中和”的达成 |
B.光催化 和H2O合成甲醇技术是实现“碳中和”的有效手段 和H2O合成甲醇技术是实现“碳中和”的有效手段 |
| C.大量开采海底中的可燃冰作为清洁能源,有助于实现“碳达峰” |
| D.实现二氧化碳的资源再利用,对于“碳达峰”有重要意义 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作能达到实验目的正确的是
| 选项 | 实验操作 | 实验目的 |
| A | 向盛有1ml硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种更难溶的沉淀 |
| B | 在两支试管中分别加入相同体积相同浓度的H2O2溶液,再向其中一支试管中加入适量FeCl3溶液 | 研究催化剂对反应速率影响的 |
| C | 向沸腾的蒸馏水中逐滴滴入适量FeCl3饱和溶液,边滴边用玻璃棒搅拌,继续煮沸 | 制备Fe(OH)3胶体 |
| D | 将铜片和锌片用导线连接后同时插入稀硫酸溶液中 | 比较锌和铜的金属活泼性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知甲为恒温、恒压容器,乙为恒温、恒容容器。两容器中均充入1 mol N2、3 mol H2,初始时两容器的温度、体积相同。一段时间后反应达到平衡,为使两容器中的N2在平衡混合物中的物质的量分数相同,下列措施中可行的是
| A.向甲容器中充入一定量的氦气 |
| B.向乙容器中充入一定量的N2 |
| C.升高乙容器的温度 |
| D.增大甲容器的压强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
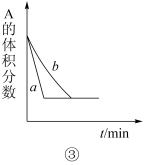
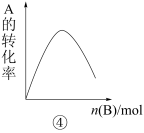
【推荐2】下列是有关外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是
 |  |
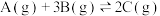 |  |
 |  |
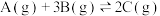 | 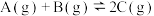 |
A.①是其他条件一定时,反应速率随温度变化的图像,则正反应 |
| B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像 |
| C.③是在有无催化剂存在条件下,建立平衡过程的图像,a是使用催化剂时的曲线 |
| D.④是一定条件下,向含有一定量A的恒容密闭容器中逐渐加入B,达平衡时A的转化率的图像 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论或解释 |
| A | 取一支试管装入2mL2mol/LNaOH溶液,先滴加1mL1mol/LMgCl2溶液,再滴几滴1mol/LCuCl2溶液 | 先生成白色沉淀,后沉淀变为蓝色 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| B | 在FeCl3+3KSCN⇌Fe(SCN)3+3KCl平衡体系中加入KCl固体 | 溶液颜色变浅 | 加入生成物该化学平衡向逆反应方向移动 |
| C | 常温下,用pH计测定1mol/LCH3COONH4溶液 | 测得pH=7 | CH3COONH4溶液对水的电离程度无影响 |
| D | 滴有酚酞的Na2CO3溶液中加入BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
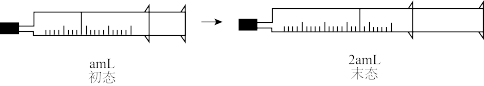
【推荐1】已知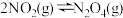 ,用如图针筒装入一定量的
,用如图针筒装入一定量的 和
和 并进行如下实验。下列说法正确的是
并进行如下实验。下列说法正确的是
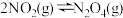 ,用如图针筒装入一定量的
,用如图针筒装入一定量的 和
和 并进行如下实验。下列说法正确的是
并进行如下实验。下列说法正确的是
| A.初态到末态颜色变浅,平衡正向移动 |
| B.平均摩尔质量:末态大于初态 |
C.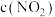 :初态比末态2倍稍大 :初态比末态2倍稍大 |
D.初态到末态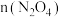 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.0 kJ·mol-1,下列有关说法正确的是
A.增大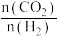 的值,可提高H2的转化率 的值,可提高H2的转化率 |
| B.升高温度能提高 CO2的反应速率和转化率 |
| C.达平衡时缩小容器体积,v(正)增大,v(逆)减小 |
| D.1 mol CO2和3 mol H2充分反应时放出的热量为 49.0 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在“宏观——微观——符号”之间建立联系是化学学科特有的思维方式。如图是科研人员提出的HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程示意图(图中只画出了HAP的部分结构)。下列说法不正确的是
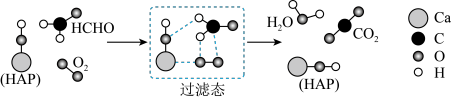

| A.HAP能降低HCHO与O2反应的活化能 |
B.该反应的化学方程式为HCHO+O2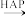 CO2+H2O CO2+H2O |
| C.反应过程中断裂或生成的的化学键类型均为极性共价键 |
| D.产物CO2分子中的氧原子不仅仅来源于O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于工业合成氨的说法正确的是
| A.工业合成氨采用10~30MPa,是因为该条件下催化剂的活性最好 |
| B.选择不同的催化剂会改变此反应△H的数值 |
| C.合成氨工业中采用低温以提高平衡转化率 |
| D.合成氨工业中采用循环操作,主要是为了提高氮气和氢气的利用率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸工业中通过 氧化氧化为
氧化氧化为 :
: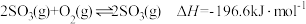
根据反应原理和上表中数据分析下列叙述错误的是
 氧化氧化为
氧化氧化为 :
: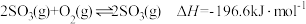
| 温度/℃ | 平衡时 的转化率 的转化率 | ||||
 | 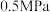 |  | 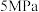 | 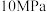 | |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.实际生产中可以通过通入大量的空气来提高 的转化率 的转化率 |
B.常压下 的转化率已经比较大了,所以实际生产中没必要增大成本采用高压 的转化率已经比较大了,所以实际生产中没必要增大成本采用高压 |
C.生产中采用温度 主要是考虑催化剂的活性温度从而提高反应物的转化率 主要是考虑催化剂的活性温度从而提高反应物的转化率 |
D.尾气中的 必须回收循环利用防止污染环境并提高原料的利用率 必须回收循环利用防止污染环境并提高原料的利用率 |
您最近一年使用:0次


 ,下列有关说法正确的是
,下列有关说法正确的是
 减小
减小 的量,平衡正向移动
的量,平衡正向移动

