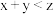已知反应3A(g)+B(g) 2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是
2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是
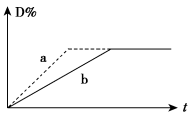
①增大A的浓度 ②升高温度 ③增大D浓度 ④加入催化剂 ⑤恒温下,缩小反应容器体积 ⑥加入稀有气体,保持容器内压强不变
 2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是
2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是 
①增大A的浓度 ②升高温度 ③增大D浓度 ④加入催化剂 ⑤恒温下,缩小反应容器体积 ⑥加入稀有气体,保持容器内压强不变
| A.①②③ | B.④⑤ | C.③④⑤ | D.④⑤⑥ |
更新时间:2016-12-09 04:34:56
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】研究表明N2O与CO在Fe+作用下发生反应,下列说法正确的是
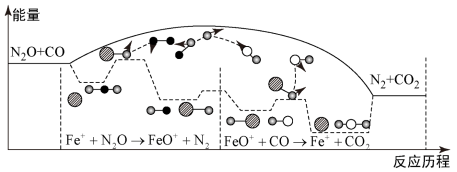

| A.反应总过程△H>0 |
| B.其他条件保持不变,升高温度可以提高反应速率 |
| C.Fe+、FeO+都是该反应催化剂,能降低反应的活化能 |
| D.Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为吸热反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】最新研究表明,在多孔炭材料,上搭载活性组分催化氧化脱硫效果明显优于传统方法,其反应机理如图所示,此时 在水中浓度为0.34g/100mL。下列有关说法正确的是
在水中浓度为0.34g/100mL。下列有关说法正确的是

 在水中浓度为0.34g/100mL。下列有关说法正确的是
在水中浓度为0.34g/100mL。下列有关说法正确的是
| A.温度过高不利于脱硫的效果 | B.活性炭作用是降低反应物的总能量 |
| C.该反应的总反应是吸热过程 | D.该温度下, 的 的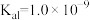 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关推断中,不正确的是( )
| 事实 | 结论 | |
| A | CaCO3+2CH3COOH=(CH3COO)2Ca +CO2↑+H2O | 酸性: CH3COOH>H2CO3 |
| B | 氢硫酸(H2S)放置在空气中变浑浊 | 氧化性:O2>S |
| C | Al(OH)3既溶于强酸又溶于强碱 | Al元素既有金属性也有非金属性 |
| D | 反应A+2B C达平衡后,升高温度平衡正向移动 C达平衡后,升高温度平衡正向移动 | 升高温度,使v正增大、v逆减小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中,不能用勒夏特列原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成SO3的反应 |
| C.Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| D.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用活性炭可还原NO2防止空气污染。其反应原理为2C(s)+2NO2(g) N2(g)+2CO2(g) ΔH=-850kJ·mol-1。一定温度下,向2L恒容密闭容器中加入足量的C和一定物质的量的NO2发生上述反应,测得CO2的物质的量浓度随时间的变化如曲线M所示:
N2(g)+2CO2(g) ΔH=-850kJ·mol-1。一定温度下,向2L恒容密闭容器中加入足量的C和一定物质的量的NO2发生上述反应,测得CO2的物质的量浓度随时间的变化如曲线M所示:
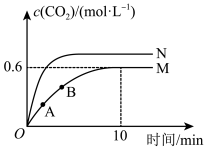
下列叙述错误的是
 N2(g)+2CO2(g) ΔH=-850kJ·mol-1。一定温度下,向2L恒容密闭容器中加入足量的C和一定物质的量的NO2发生上述反应,测得CO2的物质的量浓度随时间的变化如曲线M所示:
N2(g)+2CO2(g) ΔH=-850kJ·mol-1。一定温度下,向2L恒容密闭容器中加入足量的C和一定物质的量的NO2发生上述反应,测得CO2的物质的量浓度随时间的变化如曲线M所示:
下列叙述错误的是
| A.A点的正反应速率大于B点的逆反应速率 |
| B.达到平衡状态时,该反应放出510kJ的热量 |
| C.其他条件不变,若该反应在1L的恒容密闭容器中进行,则图象变化如曲线N所示 |
| D.其他条件不变,若向该容器中再通入一定量的NO2,NO2的平衡转化率增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
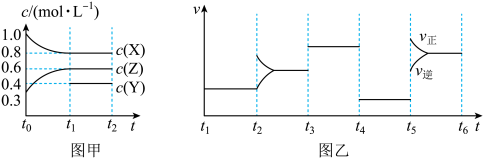

| A.Y的起始物质的量为0.5mol |
B.该反应的化学方程式为2X(g)+Y(g) 3Z(g) ΔH<0 3Z(g) ΔH<0 |
| C.若t0=0,t1=10s,则t0~t1阶段的平均反应速率为v(Z)=0.03mol·L-1·s-1 |
| D.反应物X的转化率t6点比t3点高 |
您最近半年使用:0次