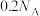下列叙述正确的是
A.价层电子排布式为 和 和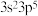 的两原子能形成离子化合物 的两原子能形成离子化合物 |
| B.三氟化氮和甲烷中的N、C杂化方式相同 |
| C.元素Se位于第四周期第IVA族,属于p区 |
| D.基态原子4s轨道半充满的元素一定位于第IA族和第IB族 |
22-23高三上·山东淄博·阶段练习 查看更多[3]
山东省淄博第四中学2022-2023学年高三上学期第一次阶段性检测化学试题重庆市二0三中学2022-2023学年高三上学期第一次月考化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题1-5)
更新时间:2022-09-29 19:27:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】短周期元素X、Y、Z、W原子序数依次增大。X的原子核外有一个电子,基态Y原子核外s轨道与p轨道电子数相等;Z元素单质常用作半导体材料;W元素原子是同周期元素原子半径最小的。下列说法正确 的是
| A.X位于元素周期表的p区 |
| B.X,Y可组成原子个数比为1:1的共价化合物 |
| C.简单氢化物稳定性:W<Z |
| D.元素电负性:X<Y<Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】硫元素与氯元素可形成 两种化合物,两种物质中各原子均满足最外层8电子稳定结构。下列说法
两种化合物,两种物质中各原子均满足最外层8电子稳定结构。下列说法错误 的是
 两种化合物,两种物质中各原子均满足最外层8电子稳定结构。下列说法
两种化合物,两种物质中各原子均满足最外层8电子稳定结构。下列说法| A.硫元素与氯元素均属于p区元素 | B. 与 与 分子中共价键的类型不完全相同 分子中共价键的类型不完全相同 |
C. 中S的化合价为 中S的化合价为 价 价 | D. 分子中的硫原子采取 分子中的硫原子采取 杂化 杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】d轨道中电子排布成 而不是排布成
而不是排布成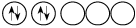 其最直接的根据是
其最直接的根据是
 而不是排布成
而不是排布成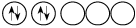 其最直接的根据是
其最直接的根据是| A.洪特规则 | B.泡利不相容原理 | C.能量最低原则 | D.能量守恒原理 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质的组成、结构或性质的叙述中,正确的是
①HF的稳定性很强,是因为其分子间能形成氢键
②基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族
③能层为1时,有自旋方向相反的两个轨道
④“量子化”就是连续的意思,微观粒子运动均有此特点
⑤前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有5种
⑥次氯酸分子的电子式:
⑦氯离子与硫离子的核外电子排布相同,都是1s22s22p63s23p6,两粒子的3p能级上的电子离核的距离相同
⑧S2-、Cl-、K+、Na+半径逐渐减小
⑨最外层有3个未成对电子的原子一定属于主族元素
①HF的稳定性很强,是因为其分子间能形成氢键
②基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族
③能层为1时,有自旋方向相反的两个轨道
④“量子化”就是连续的意思,微观粒子运动均有此特点
⑤前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有5种
⑥次氯酸分子的电子式:

⑦氯离子与硫离子的核外电子排布相同,都是1s22s22p63s23p6,两粒子的3p能级上的电子离核的距离相同
⑧S2-、Cl-、K+、Na+半径逐渐减小
⑨最外层有3个未成对电子的原子一定属于主族元素
| A.①③④⑦⑧ | B.⑤⑧⑨ | C.②③⑤⑥⑦⑨ | D.②⑦⑧⑨ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示。下列说法正确的是
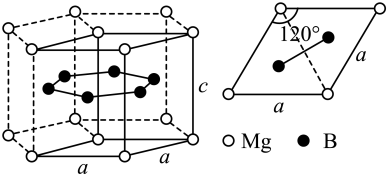
A. 的价电子轨道表示式为3s2 的价电子轨道表示式为3s2 |
B.该晶体的化学式为 |
C.该晶体中 最近距离为 最近距离为 |
D. 原子的配位数为6 原子的配位数为6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列状态的磷微粒中,失去最外层一个电子所需能量最大的是
| A.[Ne]3s23p3 | B.[Ne]3s23p2 | C.[Ne]3s23p24s1 | D.[Ne]3s23p14s1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯,如图所示,在
分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯,如图所示,在 分子中每个碳原子均与周围相邻的其他3个碳原子相连,60个碳原子组成若干个正六边形和正五边形,碳均为
分子中每个碳原子均与周围相邻的其他3个碳原子相连,60个碳原子组成若干个正六边形和正五边形,碳均为 价。则下列有关说法中不正确的是
价。则下列有关说法中不正确的是

 分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯,如图所示,在
分子是一种由60个碳原子构成的分子,它形似足球,因此又名足球烯,如图所示,在 分子中每个碳原子均与周围相邻的其他3个碳原子相连,60个碳原子组成若干个正六边形和正五边形,碳均为
分子中每个碳原子均与周围相邻的其他3个碳原子相连,60个碳原子组成若干个正六边形和正五边形,碳均为 价。则下列有关说法中不正确的是
价。则下列有关说法中不正确的是
A. 的熔点比石墨的熔点低 的熔点比石墨的熔点低 |
B. 分子中碳原子的杂化方式与甲烷中碳原子的不完全相同 分子中碳原子的杂化方式与甲烷中碳原子的不完全相同 |
C. 分子中只含 分子中只含 键、不含 键、不含 键 键 |
| D.影响足球烯的熔、沸点的是分子间作用力 |
您最近一年使用:0次
【推荐2】有机物M具有解痉和抗胆碱作用,其结构简式如图所示.下列说法错误的是
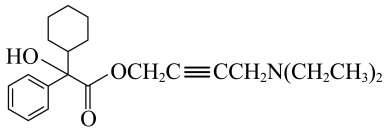
| A.M分子中碳原子的杂化方式有3种 | B.1molM最多可与6molH2发生加成反应 |
| C.M能发生消去反应 | D.M具有碱性 |
您最近一年使用:0次

 (晶胞中的其他
(晶胞中的其他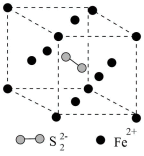
 有8个
有8个 (相对分子质量为248)、
(相对分子质量为248)、 均为
均为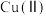 配合物,可发生如下图所示的构型互转,当配位构型由八面体转变为平面四边形时,颜色由紫色变为橙色。下列说法正确的是
配合物,可发生如下图所示的构型互转,当配位构型由八面体转变为平面四边形时,颜色由紫色变为橙色。下列说法正确的是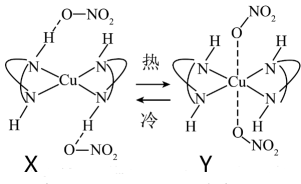
 原子的价层电子排布式为
原子的价层电子排布式为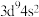
 的
的